| Ricin | |||||
|---|---|---|---|---|---|

Ricin structure (PDB: 2AAI). The A chain is shown in blue and the B chain in orange. |
|||||
| Identifiers | |||||
| Organism | Ricinus communis | ||||
| Symbol | RCOM_2159910 | ||||
| Entrez | 8287993 | ||||
| RefSeq (mRNA) | XM_002534603.1 | ||||
| RefSeq (Prot) | XP_002534649.1 | ||||
| UniProt | P02879 | ||||
| Other data | |||||
| EC number | 3.2.2.22 | ||||
| Chromosome | whole genome: 0 — 0.01 Mb | ||||
|
| Ribosome-inactivating protein (Ricin A chain) | |||||||
|---|---|---|---|---|---|---|---|
| Identifiers | |||||||
| Symbol | RIP | ||||||
| Pfam | PF00161 | ||||||
| InterPro | IPR001574 | ||||||
| PROSITE | PDOC00248 | ||||||
| SCOP2 | 1paf / SCOPe / SUPFAM | ||||||
|
| Ricin-type beta-trefoil lectin domain (Ricin B chain) | |||||||
|---|---|---|---|---|---|---|---|
| Identifiers | |||||||
| Symbol | N/A | ||||||
| Pfam | PF00652 | ||||||
| Pfam clan | CL0066 | ||||||
| PROSITE | IPR000772 | ||||||
| SCOP2 | 1abr / SCOPe / SUPFAM | ||||||
| CAZy | CBM13 | ||||||
| CDD | cd00161 | ||||||
|
Ricin ( RY-sin) is a lectin (a carbohydrate-binding protein) and a highly potent toxin produced in the seeds of the castor oil plant, Ricinus communis. The median lethal dose (LD50) of ricin for mice is around 22 micrograms per kilogram of body weight via intraperitoneal injection. Oral exposure to ricin is far less toxic. An estimated lethal oral dose in humans is approximately 1 milligram per kilogram of body weight.[1]
Ricin is a toxalbumin and was first described by Peter Hermann Stillmark, the founder of lectinology.
Biochemistry[edit]
Ricin is classified as a type 2 ribosome-inactivating protein (RIP). Whereas type 1 RIPs are composed of a single protein chain that possesses catalytic activity, type 2 RIPs, also known as holotoxins, are composed of two different protein chains that form a heterodimeric complex. Type 2 RIPs consist of an A chain that is functionally equivalent to a type 1 RIP, covalently connected by a single disulfide bond to a B chain that is catalytically inactive, but serves to mediate transport of the A-B protein complex from the cell surface, via vesicle carriers, to the lumen of the endoplasmic reticulum (ER). Both type 1 and type 2 RIPs are functionally active against ribosomes in vitro; however, only type 2 RIPs display cytotoxicity due to the lectin-like properties of the B chain. To display its ribosome-inactivating function, the ricin disulfide bond must be reductively cleaved.[2]
Biosynthesis[edit]
Ricin is synthesized in the endosperm of castor oil plant seeds.[3] The ricin precursor protein is 576 amino acid residues in length and contains a signal peptide (residues 1–35), the ricin A chain (36–302), a linker peptide (303–314), and the ricin B chain (315–576).[4] The N-terminal signal sequence delivers the prepropolypeptide to the endoplasmic reticulum (ER) and then the signal peptide is cleaved off. Within the lumen of the ER the propolypeptide is glycosylated and a protein disulfide isomerase catalyzes disulfide bond formation between cysteines 294 and 318. The propolypeptide is further glycosylated within the Golgi apparatus and transported to protein storage bodies. The propolypeptide is cleaved within protein bodies by an endopeptidase to produce the mature ricin protein that is composed of a 267 residue A chain and a 262 residue B chain that are covalently linked by a single disulfide bond.[3]
Structure[edit]
In terms of structure, ricin closely resembles abrin-a, an isotoxin of abrin. The quaternary structure of ricin is a globular, glycosylated heterodimer of approximately 60–65 kDa.[5] Ricin toxin A chain and ricin toxin B chain are of similar molecular weights, approximately 32 kDa and 34 kDa, respectively.
- Ricin toxin A chain (RTA) is an N-glycoside hydrolase composed of 267 amino acids.[6] It has three structural domains with approximately 50% of the polypeptide arranged into alpha-helices and beta-sheets.[7] The three domains form a pronounced cleft that is the active site of RTA.
- Ricin toxin B chain (RTB) is a lectin composed of 262 amino acids that is able to bind terminal galactose residues on cell surfaces.[8] RTB forms a bilobal, barbell-like structure lacking alpha-helices or beta-sheets where individual lobes contain three subdomains. At least one of these three subdomains in each homologous lobe possesses a sugar-binding pocket that gives RTB its functional character.
A comparison of the similar structures of abrin-a (red) and ricin (blue)
While other plants contain the protein chains found in ricin, both protein chains must be present to produce toxic effects. For example, plants that contain only protein chain A, such as barley, are not toxic because without the link to protein chain B, protein chain A cannot enter the cell and do damage to ribosomes.[9]
Entry into the cytoplasm[edit]
Ricin B chain binds complex carbohydrates on the surface of eukaryotic cells containing either terminal N-acetylgalactosamine or beta-1,4-linked galactose residues. In addition, the mannose-type glycans of ricin are able to bind to cells that express mannose receptors.[10] RTB has been shown to bind to the cell surface on the order of 106–108 ricin molecules per cell surface.[11]
The profuse binding of ricin to surface membranes allows internalization with all types of membrane invaginations. The holotoxin can be taken up by clathrin-coated pits, as well as by clathrin-independent pathways including caveolae and macropinocytosis.[12][13] Intracellular vesicles shuttle ricin to endosomes that are delivered to the Golgi apparatus. The active acidification of endosomes is thought to have little effect on the functional properties of ricin. Because ricin is stable over a wide pH range, degradation in endosomes or lysosomes offers little or no protection against ricin.[14] Ricin molecules are thought to follow retrograde transport via early endosomes, the trans-Golgi network, and the Golgi to enter the lumen of the endoplasmic reticulum (ER).[15]
For ricin to function cytotoxically, RTA must be reductively cleaved from RTB to release a steric block of the RTA active site. This process is catalysed by the protein PDI (protein disulphide isomerase) that resides in the lumen of the ER.[16][17] Free RTA in the ER lumen then partially unfolds and partially buries into the ER membrane, where it is thought to mimic a misfolded membrane-associated protein.[18] Roles for the ER chaperones GRP94,[19] EDEM[20] and BiP[21] have been proposed prior to the ‘dislocation’ of RTA from the ER lumen to the cytosol in a manner that uses components of the endoplasmic reticulum-associated protein degradation (ERAD) pathway. ERAD normally removes misfolded ER proteins to the cytosol for their destruction by cytosolic proteasomes. Dislocation of RTA requires ER membrane-integral E3 ubiquitin ligase complexes,[22] but RTA avoids the ubiquitination that usually occurs with ERAD substrates because of its low content of lysine residues, which are the usual attachment sites for ubiquitin.[23] Thus, RTA avoids the usual fate of dislocated proteins (destruction that is mediated by targeting ubiquitinylated proteins to the cytosolic proteasomes). In the mammalian cell cytosol, RTA then undergoes triage by the cytosolic molecular chaperones Hsc70 and Hsp90 and their co-chaperones, as well as by one subunit (RPT5) of the proteasome itself, that results in its folding to a catalytic conformation,[19][24] which de-purinates ribosomes, thus halting protein synthesis.
Ribosome inactivation[edit]
RTA has rRNA N-glycosylase activity that is responsible for the cleavage of a glycosidic bond within the large rRNA of the 60S subunit of eukaryotic ribosomes.[25] RTA specifically and irreversibly hydrolyses the N-glycosidic bond of the adenine residue at position 4324 (A4324) within the 28S rRNA, but leaves the phosphodiester backbone of the RNA intact.[26] The ricin targets A4324 that is contained in a highly conserved sequence of 12 nucleotides universally found in eukaryotic ribosomes. The sequence, 5′-AGUACGAGAGGA-3′, termed the sarcin-ricin loop, is important in binding elongation factors during protein synthesis.[27] The depurination event rapidly and completely inactivates the ribosome, resulting in toxicity from inhibited protein synthesis. A single RTA molecule in the cytosol is capable of depurinating approximately 1500 ribosomes per minute.
Depurination reaction[edit]
Within the active site of RTA, there exist several invariant amino acid residues involved in the depurination of ribosomal RNA.[14] Although the exact mechanism of the event is unknown, key amino acid residues identified include tyrosine at positions 80 and 123, glutamic acid at position 177, and arginine at position 180. In particular, Arg180 and Glu177 have been shown to be involved in the catalytic mechanism, and not substrate binding, with enzyme kinetic studies involving RTA mutants. The model proposed by Mozingo and Robertus,[7] based on X-ray structures, is as follows:
- Sarcin-ricin loop substrate binds RTA active site with target adenine stacking against tyr80 and tyr123.
- Arg180 is positioned such that it can protonate N-3 of adenine and break the bond between N-9 of the adenine ring and C-1′ of the ribose.
- Bond cleavage results in an oxycarbonium ion on the ribose, stabilized by Glu177.
- N-3 protonation of adenine by Arg180 allows deprotonation of a nearby water molecule.
- Resulting hydroxyl attacks ribose carbonium ion.
- Depurination of adenine results in a neutral ribose on an intact phosphodiester RNA backbone.
Toxicity[edit]
Castor oil seeds in the Royal Botanic Gardens, Kew Economic Botany Collection
Ricin is very toxic if inhaled, injected, or ingested. It can also be toxic if dust contacts the eyes or if it is absorbed through damaged skin. It acts as a toxin by inhibiting protein synthesis.[28][29] It prevents cells from assembling various amino acids into proteins according to the messages it receives from messenger RNA in a process conducted by the cell’s ribosome (the protein-making machinery) – that is, the most basic level of cell metabolism, essential to all living cells and thus to life itself. Ricin is resistant, but not impervious, to digestion by peptidases. By ingestion, the pathology of ricin is largely restricted to the gastrointestinal tract, where it may cause mucosal injuries. With appropriate treatment, most patients will make a good recovery.[30][31]
Symptoms[edit]
Because the symptoms are caused by failure to make protein, they may take anywhere from hours to days to appear, depending on the route of exposure and the dose. When ingested, gastrointestinal symptoms can manifest within six hours; these symptoms do not always become apparent. Within two to five days of exposure to ricin, its effects on the central nervous system, adrenal glands, kidneys, and liver appear.[29]
Ingestion of ricin causes pain, inflammation, and hemorrhage in the mucosal membranes of the gastrointestinal system. Gastrointestinal symptoms quickly progress to severe nausea, vomiting, diarrhea, and difficulty swallowing (dysphagia). Haemorrhage causes bloody feces (melena) and vomiting blood (hematemesis). The low blood volume (hypovolemia) caused by gastrointestinal fluid loss can lead to organ failure in the pancreas, kidney, liver, and GI tract and progress to shock. Shock and organ failure are indicated by disorientation, stupor, weakness, drowsiness, excessive thirst (polydipsia), low urine production (oliguria), and bloody urine (hematuria).[29]
Symptoms of ricin inhalation are different from those caused by ingestion. Early symptoms include a cough and fever.[29]
When skin or inhalation exposure occur, ricin can cause an allergy to develop. This is indicated by swelling (edema) of the eyes and lips; asthma; bronchial irritation; dry, sore throat; congestion; skin redness (erythema); skin blisters (vesication); wheezing; itchy, watery eyes; chest tightness; and skin irritation.[29]
Treatment[edit]
An antidote has been developed by the UK military, although as of 2006 it has not yet been tested on humans.[32][33] As of 2005 another antidote developed by the US military has been shown to be safe and effective in lab mice injected with antibody-rich blood mixed with ricin, and has had some human testing.[34] Monoclonal antibodies are under scientific investigation as a possible treatment for ricin poisoning.[35]
Symptomatic and supportive treatments are available for ricin poisoning. Existing treatments emphasize minimizing the effects of the poison. Possible treatments include intravenous fluids or electrolytes, airway management, assisted ventilation, or giving medications to remedy seizures and low blood pressure. If the ricin has been ingested recently, the stomach can be flushed by ingesting activated charcoal or by performing gastric lavage. Survivors often develop long-term organ damage. Ricin causes severe diarrhea and vomiting, and victims can die of circulatory shock or organ failure; inhaled ricin can cause fatal pulmonary edema or respiratory failure. Death typically occurs within 3–5 days of exposure.[29]
Prevention[edit]
Vaccination is possible by injecting an inactive form of protein chain A.[9] This vaccination is effective for several months due to the body’s production of antibodies to the foreign protein. In 1978 Bulgarian defector Vladimir Kostov survived a ricin attack similar to the one on Georgi Markov, probably due to his body’s production of antibodies. When a ricin-laced pellet was removed from the small of his back it was found that some of the original wax coating was still attached. For this reason only small amounts of ricin had leaked out of the pellet, producing some symptoms but allowing his body to develop immunity to further poisoning.[9]
Sources[edit]
The seeds of Ricinus communis are commonly crushed to extract castor oil. As ricin is not oil-soluble, little is found in the extracted castor oil.[9] The extracted oil is also heated to more than 80 °C (176 °F) to denature any ricin that may be present.[9] The remaining spent crushed seeds, called variously the «cake», «oil cake», and «press cake», can contain up to 5% ricin.[36] While the oil cake from coconut, peanuts, and sometimes cotton seeds can be used as cattle feed or fertilizer, the toxic nature of castor beans precludes their oil cake from being used as feed unless the ricin is first deactivated by autoclaving.[37] Accidental ingestion of Ricinus communis cake intended for fertilizer has been reported to be responsible for fatal ricin poisoning in animals.[28][38]
Deaths from ingesting castor plant seeds are rare, partly because of their indigestible seed coat, and because some of the ricin is deactivated in the stomach.[5] The pulp from eight beans is considered dangerous to an adult.[39] Rauber and Heard have written that close examination of early 20th century case reports indicates that public and professional perceptions of ricin toxicity «do not accurately reflect the capabilities of modern medical management».[40]
Most acute poisoning episodes in humans are the result of oral ingestion of castor beans, 5–20 of which could prove fatal to an adult. Swallowing castor beans rarely proves to be fatal unless the bean is thoroughly chewed. The survival rate of castor bean ingestion is 98%.[9] In 2013 a 37-year-old woman in the United States survived after ingesting 30 beans.[41] Victims often manifest nausea, diarrhea, fast heart rate, low blood pressure, and seizures persisting for up to a week.[28] Blood, plasma, or urine ricin or ricinine concentrations may be measured to confirm diagnosis. The laboratory testing usually involves immunoassay or liquid chromatography-mass spectrometry.[42]
Therapeutic applications[edit]
Although no approved therapeutics are currently based on ricin, it does have the potential to be used in the treatment of tumors, as a «magic bullet» to destroy targeted cells.[14] Because ricin is a protein, it can be linked to a monoclonal antibody to target cancerous cells recognized by the antibody. The major problem with ricin is that its native internalization sequences are distributed throughout the protein. If any of these native internalization sequences are present in a therapeutic agent, the drug will be internalized by, and kill, untargeted non-tumorous cells as well as targeted cancerous cells.
Modifying ricin may sufficiently lessen the likelihood that the ricin component of these immunotoxins will cause the wrong cells to internalize it, while still retaining its cell-killing activity when it is internalized by the targeted cells. However, bacterial toxins, such as diphtheria toxin, which is used in denileukin diftitox, an FDA-approved treatment for leukemia and lymphoma, have proven to be more practical. A promising approach for ricin is to use the non-toxic B subunit (a lectin) as a vehicle for delivering antigens into cells, thus greatly increasing their immunogenicity. Use of ricin as an adjuvant has potential implications for developing mucosal vaccines.
Regulation[edit]
In the US, ricin appears on the select agents list of the Department of Health and Human Services,[43] and scientists must register with HHS to use ricin in their research. However, investigators under the control of less than 1000 mg are exempt from regulation.[44]
Ricin is classified as an extremely hazardous substance in the United States as defined in Section 302 of the US Emergency Planning and Community Right-to-Know Act (42 U.S.C. 11002), and is subject to strict reporting requirements by facilities that produce, store, or use it in significant quantities.[45]
Chemical or biological warfare agent[edit]
The United States investigated ricin for its military potential during World War I.[46] At that time it was being considered for use either as a toxic dust or as a coating for bullets and shrapnel. The dust cloud concept could not be adequately developed, and the coated bullet/shrapnel concept would violate the Hague Convention of 1899 (adopted in U.S. law at 32 Stat. 1903), specifically Annex §2, Ch.1, Article 23, stating «… it is especially prohibited … [t]o employ poison or poisoned arms».[47] World War I ended before the United States weaponized ricin.
During World War II the United States and Canada undertook studying ricin in cluster bombs.[48] Though there were plans for mass production and several field trials with different bomblet concepts, the end conclusion was that it was no more economical than using phosgene. This conclusion was based on comparison of the final weapons, rather than ricin’s toxicity (LCt50 ~10 mg/min·m3). Ricin was given the military symbol W or later WA. Interest in it continued for a short period after World War II, but soon subsided when the US Army Chemical Corps began a program to weaponize sarin.[49]
The Soviet Union also possessed weaponized ricin. The KGB developed weapons using ricin which were used outside the Soviet bloc, most famously in the Markov assassination.[50][51]
In spite of ricin’s extreme toxicity and utility as an agent of chemical/biological warfare, production of the toxin is difficult to limit. The castor bean plant from which ricin is derived is a common ornamental and can be grown at home without any special care.
Under both the 1972 Biological Weapons Convention and the 1997 Chemical Weapons Convention, ricin is listed as a schedule 1 controlled substance. Despite this, more than 1 million metric tons (1,100,000 short tons) of castor beans are processed each year, and approximately 5% of the total is rendered into a waste containing negligible concentrations of undenatured ricin toxin.[52]
Ricin is several orders of magnitude less toxic than botulinum or tetanus toxin, but the latter are harder to come by. Compared to botulinum or anthrax as biological weapons or chemical weapons, the quantity of ricin required to achieve LD50 over a large geographic area is significantly more than an agent such as anthrax (tons of ricin vs. only kilogram quantities of anthrax).[53] Ricin is easy to produce, but is not as practical or likely to cause as many casualties as other agents.[30] Ricin is easily denatured by temperatures over 80 °C (176 °F) meaning many methods of deploying ricin would generate enough heat to denature it.[36] Once deployed, an area contaminated with ricin remains dangerous until the bonds between chain A or B have been broken, a process that takes two or three days.[9] In contrast, anthrax spores may remain lethal for decades. Jan van Aken, a German expert on biological weapons, explained in a report for The Sunshine Project that Al Qaeda’s experiments with ricin suggest their inability to produce botulinum or anthrax.[54]
Developments[edit]
A biopharmaceutical company called Soligenix, Inc. licensed an anti-ricin vaccine called RiVax from Vitetta et al. at UT Southwestern. The vaccine was found safe and immunogenic in mice, rabbits, and humans. Two successful clinical trials were completed.[55] Soligenix was issued a US patent for Rivax. The ricin vaccine candidate was granted orphan drug status in the US and the EEC and, as of 2019, was in clinical trials in the US. Grants from the National Institute of Allergy and Infectious Diseases and the US Food and Drug Administration supported development of the vaccine candidate.[56]
Synthesis[edit]
The first isolation of ricin is attributed to the Baltic-German microbiologist Peter Hermann Stillmark (1860–1923) in 1888.[57][58][59]
Terrorist use[edit]
Ricin has been involved in a number of actual or planned attacks on individuals. In 1978, the Bulgarian dissident Georgi Markov was assassinated by Bulgarian secret police who surreptitiously shot him on a London street with what was later found to have been a modified umbrella using compressed gas to fire a tiny pellet containing ricin into his leg.[30][60] He died in a hospital a few days later; his body was passed to a special poison branch of the British Ministry of Defence that discovered the pellet during an autopsy. The prime suspects were the Bulgarian secret police: Georgi Markov had defected from Bulgaria some years previously and had subsequently written books and made radio broadcasts that were highly critical of the Bulgarian communist regime. However, it was believed at the time that Bulgaria would not have been able to produce the pellet, and it was also believed that the KGB had supplied it. The KGB denied any involvement, although high-profile KGB defectors Oleg Kalugin and Oleg Gordievsky later confirmed the KGB’s involvement. Soviet dissident Aleksandr Solzhenitsyn had (but survived) ricin-like symptoms after an encounter in 1971 with KGB agents.[61]
Ten days before the attack on Georgi Markov another Bulgarian defector, Vladimir Kostov, survived a similar attack. Kostov was standing on an escalator of the Paris metro when he felt a sting in his lower back above the belt of his trousers. He developed a fever, but recovered. After Markov’s death the wound on Kostov’s back was examined and a ricin-laced pellet identical to the one used against Markov was removed.[9]
Several terrorist individuals and groups have experimented with ricin or planned to use it.[62] There have been incidents of the poison being mailed to US politicians. For example, on 29 May 2013 two anonymous letters sent to New York City Mayor Michael Bloomberg contained traces of it.[63] Another was sent to the offices of Mayors Against Illegal Guns in Washington, D.C. A letter containing ricin was also reported to have been sent to American President Barack Obama at the same time. Shannon Richardson, an actress, was later charged with the crime, and pleaded guilty that December;[64] she sentenced to 18 years in prison plus a restitution fine of US$367,000.[65] On 2 October 2018, two letters suspected of containing ricin were sent to The Pentagon, one addressed to Secretary of Defense James Mattis, and the other to Chief of Naval Operations, Admiral John Richardson.[66] A letter was received on 23 July 2019 at Pelican Bay State Prison in California which claimed to contain a suspicious substance. Authorities later confirmed it contained ricin; no detrimental exposures were identified.[67]
In 2020, some media in the Czech Republic reported, based on intelligence information, that a person carrying a Russian diplomatic passport and ricin had arrived in Prague with the intention of assassinating three politicians. Russian president Vladimir Putin denied the reports. The targets were said to have been Zdeněk Hřib, the mayor of Prague (capital of the Czech Republic), who was involved in renaming a square in Prague, «Pod Kaštany», where the Russian embassy is situated, to the Square of Boris Nemtsov, an opposition politician assassinated in the Kremlin in 2015; Ondřej Kolář, the mayor of Prague 6 municipal district, who was involved in removing the controversial statue to the Soviet-era Marshal Konev; and Pavel Novotný, the mayor of Prague’s southwestern Řeporyje district. They all received police protection.[68][69] Czech president Miloš Zeman later described the police protection of Zdeněk Hřib as an attempt by an insignificant politician to gain attention. Zeman also confused ricin with non-poisonous laxative castor oil.[70]
In 2018[71] and 2023 German police thwarted attempted ricin attacks by people supporting Islamist terrorist organisation Daesh (also calling itself Islamic State, IS), after tip-offs believed to have come from the US FBI.[72]
In popular culture[edit]
Ricin has been used as a plot device, such as in the television series Breaking Bad.[73]
The popularity of Breaking Bad inspired several real-life criminal cases involving ricin or similar substances. Kuntal Patel from London attempted to poison her mother with abrin after the latter interfered with her marriage plans.[74] Daniel Milzman, a 19-year-old former Georgetown University student, was charged with manufacturing ricin in his dorm room, as well as the intent of «[using] the ricin on another undergraduate student with whom he had a relationship».[75] Mohammed Ali from Liverpool, England, was convicted after attempting to purchase 500 mg of ricin over the dark web from an undercover FBI agent. He was sentenced, on 18 September 2015, to eight years imprisonment.[76]
In the 2013 movie The Good Mother, a mother injects and feeds her daughters with ricin in a case of Munchausen by proxy; she is caught after a daughter dies.
In the 2014 movie The Interview, a transdermal strip carrying ricin is used in a CIA plot to assassinate North Korean dictator Kim Jong-un via handshake.
See also[edit]
- List of poisonous plants
References[edit]
- ^ European Food Safety Authority (EFSA) (September 2008). «Ricin (from Ricinus communis) as undesirable substances in animal feed‐Scientific Opinion of the Panel on Contaminants in the Food Chain». EFSA Journal. 6 (9): 726. doi:10.2903/j.efsa.2008.726.
- ^ Wright HT, Robertus JD (July 1987). «The intersubunit disulfide bridge of ricin is essential for cytotoxicity». Arch. Biochem. Biophys. 256 (1): 280–284. doi:10.1016/0003-9861(87)90447-4. PMID 3606124.
- ^ a b Lord MJ, Roberts LM (2005). «Ricin: structure, synthesis, and mode of action». In Raffael S, Schmitt M (eds.). Microbial Protein Toxins. Topics in Current Genetics. Vol. 11. Berlin: Springer. pp. 215–233. doi:10.1007/b100198. ISBN 978-3-540-23562-0.
- ^ «P02879 Ricin precursor – Ricinus communis (Castor bean)». UniProtKB. UniProt Consortium.
- ^ a b Aplin PJ, Eliseo T (September 1997). «Ingestion of castor oil plant seeds». Med. J. Aust. 167 (5): 260–261. doi:10.5694/j.1326-5377.1997.tb125050.x. PMID 9315014. S2CID 42009654.
- ^ Olsnes S, Pihl A (July 1973). «Different biological properties of the two constituent polypeptide chains of ricin, a toxic protein inhibiting protein synthesis». Biochemistry. 12 (16): 3121–3126. doi:10.1021/bi00740a028. PMID 4730499.
- ^ a b Weston SA, Tucker AD, Thatcher DR, Derbyshire DJ, Pauptit RA (December 1994). «X-ray structure of recombinant ricin A-chain at 1.8 A resolution». J. Mol. Biol. 244 (4): 410–422. doi:10.1006/jmbi.1994.1739. PMID 7990130.
- ^ Wales R, Richardson PT, Roberts LM, Woodland HR, Lord JM (October 1991). «Mutational analysis of the galactose binding ability of recombinant ricin B chain». J. Biol. Chem. 266 (29): 19172–19179. doi:10.1016/S0021-9258(18)54978-4. PMID 1717462.
- ^ a b c d e f g h Harkup K (2015). A is For Arsenic: The poisons of Agatha Christie. London: Bloomsbury Sigma. pp. 222–236. ISBN 978-1-4729-1130-8.
- ^ Magnusson S, Kjeken R, Berg T (March 1993). «Characterization of two distinct pathways of endocytosis of ricin by rat liver endothelial cells». Exp. Cell Res. 205 (1): 118–125. doi:10.1006/excr.1993.1065. PMID 8453986.
- ^ Sphyris N, Lord JM, Wales R, Roberts LM (September 1995). «Mutational analysis of the Ricinus lectin B-chains. Galactose-binding ability of the 2 gamma subdomain of Ricinus communis agglutinin B-chain». J. Biol. Chem. 270 (35): 20292–20297. doi:10.1074/jbc.270.35.20292. PMID 7657599.
- ^ Moya M, Dautry-Varsat A, Goud B, Louvard D, Boquet P (August 1985). «Inhibition of coated pit formation in Hep2 cells blocks the cytotoxicity of diphtheria toxin but not that of ricin toxin». J. Cell Biol. 101 (2): 548–559. doi:10.1083/jcb.101.2.548. PMC 2113662. PMID 2862151.
- ^ Nichols BJ, Lippincott-Schwartz J (October 2001). «Endocytosis without clathrin coats». Trends Cell Biol. 11 (10): 406–412. doi:10.1016/S0962-8924(01)02107-9. PMID 11567873.
- ^ a b c Lord MJ, Jolliffe NA, Marsden CJ, Pateman CS, Smith DC, Spooner RA, Watson PD, Roberts LM (2003). «Ricin. Mechanisms of cytotoxicity». Toxicol Rev. 22 (1): 53–64. doi:10.2165/00139709-200322010-00006. PMID 14579547.
- ^ Spooner RA, Smith DC, Easton AJ, Roberts LM, Lord JM (2006). «Retrograde transport pathways utilised by viruses and protein toxins». Virol. J. 3: 26. doi:10.1186/1743-422X-3-26. PMC 1524934. PMID 16603059.
- ^ Spooner RA, Watson PD, Marsden CJ, Smith DC, Moore KA, Cook JP, Lord JM, Roberts LM (October 2004). «Protein disulphide-isomerase reduces ricin to its A and B chains in the endoplasmic reticulum». Biochem. J. 383 (Pt 2): 285–293. doi:10.1042/BJ20040742. PMC 1134069. PMID 15225124.
- ^ Bellisola G, Fracasso G, Ippoliti R, Menestrina G, Rosén A, Soldà S, Udali S, Tomazzolli R, Tridente G, Colombatti M (May 2004). «Reductive activation of ricin and ricin A-chain immunotoxins by protein disulfide isomerase and thioredoxin reductase». Biochem. Pharmacol. 67 (9): 1721–1731. doi:10.1016/j.bcp.2004.01.013. PMID 15081871.
- ^ Mayerhofer PU, Cook JP, Wahlman J, Pinheiro TT, Moore KA, Lord JM, Johnson AE, Roberts LM (April 2009). «Ricin A chain insertion into endoplasmic reticulum membranes is triggered by a temperature increase to 37 {degrees}C». J. Biol. Chem. 284 (15): 10232–10242. doi:10.1074/jbc.M808387200. PMC 2665077. PMID 19211561.
- ^ a b Spooner RA, Hart PJ, Cook JP, Pietroni P, Rogon C, Höhfeld J, Roberts LM, Lord JM (November 2008). «Cytosolic chaperones influence the fate of a toxin dislocated from the endoplasmic reticulum». Proc. Natl. Acad. Sci. U.S.A. 105 (45): 17408–17413. Bibcode:2008PNAS..10517408S. doi:10.1073/pnas.0809013105. JSTOR 25465291. PMC 2580750. PMID 18988734.
- ^ Slominska-Wojewodzka M, Gregers TF, Wälchli S, Sandvig K (April 2006). «EDEM is involved in retrotranslocation of ricin from the endoplasmic reticulum to the cytosol». Mol. Biol. Cell. 17 (4): 1664–1675. doi:10.1091/mbc.E05-10-0961. PMC 1415288. PMID 16452630.
- ^ Gregers TF, Skånland SS, Wälchli S, Bakke O, Sandvig K (May 2013). «BiP negatively affects ricin transport». Toxins (Basel). 5 (5): 969–982. doi:10.3390/toxins5050969. PMC 3709273. PMID 23666197.
- ^ Li S, Spooner RA, Allen SC, Guise CP, Ladds G, Schnöder T, Schmitt MJ, Lord JM, Roberts LM (August 2010). «Folding-competent and folding-defective forms of ricin A chain have different fates after retrotranslocation from the endoplasmic reticulum». Mol. Biol. Cell. 21 (15): 2543–2554. doi:10.1091/mbc.E09-08-0743. PMC 2912342. PMID 20519439.
- ^ Deeks ED, Cook JP, Day PJ, Smith DC, Roberts LM, Lord JM (March 2002). «The low lysine content of ricin A chain reduces the risk of proteolytic degradation after translocation from the endoplasmic reticulum to the cytosol». Biochemistry. 41 (10): 3405–3413. doi:10.1021/bi011580v. PMID 11876649.
- ^ Pietroni P, Vasisht N, Cook JP, Roberts DM, Lord JM, Hartmann-Petersen R, Roberts LM, Spooner RA (April 2013). «The proteasome cap RPT5/Rpt5p subunit prevents aggregation of unfolded ricin A chain». Biochem. J. 453 (3): 435–445. doi:10.1042/BJ20130133. PMC 3778710. PMID 23617410.
- ^ Endo Y, Tsurugi K (June 1987). «RNA N-glycosidase activity of ricin A-chain. Mechanism of action of the toxic lectin ricin on eukaryotic ribosomes» (PDF). J. Biol. Chem. 262 (17): 8128–8130. doi:10.1016/S0021-9258(18)47538-2. PMID 3036799.
- ^ Endo Y, Tsurugi K (June 1988). «The RNA N-glycosidase activity of ricin A-chain. The characteristics of the enzymatic activity of ricin A-chain with ribosomes and with rRNA» (PDF). J. Biol. Chem. 263 (18): 8735–8739. doi:10.1016/S0021-9258(18)68367-X. PMID 3288622.
- ^ Sperti S, Montanaro L, Mattioli A, Stirpe F (November 1973). «Inhibition by ricin of protein synthesis in vitro: 60 S ribosomal subunit as the target of the toxin». Biochem. J. 136 (3): 813–815. doi:10.1042/bj1360813. PMC 1166019. PMID 4360718.
- ^ a b c Ujváry I (2010). Krieger R (ed.). Hayes´ Handbook of Pesticide Toxicology (Third ed.). Elsevier, Amsterdam. pp. 119–229. ISBN 978-0-12-374367-1.
- ^ a b c d e f «CDC – The Emergency Response Safety and Health Database: Biotoxin: RICIN – NIOSH». cdc.gov. Retrieved 31 December 2015.
- ^ a b c Schep LJ, Temple WA, Butt GA, Beasley MD (November 2009). «Ricin as a weapon of mass terror – separating fact from fiction». Environ Int. 35 (8): 1267–1271. doi:10.1016/j.envint.2009.08.004. PMID 19767104. Archived from the original on 5 November 2020. Retrieved 12 December 2019.
- ^ Kopferschmitt J, Flesch F, Lugnier A, Sauder P, Jaeger A, Mantz JM (April 1983). «Acute voluntary intoxication by ricin». Hum Toxicol. 2 (2): 239–242. doi:10.1177/096032718300200211. PMID 6862467. S2CID 21965711.
- ^ Rincon P (11 November 2009). «Ricin ‘antidote’ to be produced». BBC News. Retrieved 1 September 2010.
- ^ «Human trial proves ricin vaccine safe, induces neutralizing antibodies; further tests planned». University of Texas Southwestern Medical Center. 30 January 2006. Archived from the original on 27 September 2011. Retrieved 7 May 2012.
- ^ Fleming-Michael K (1 September 2005). «Vaccine for ricin toxin developed at Detrick lab». Dcmilitary.com. Archived from the original on 24 May 2012. Retrieved 1 September 2010.
- ^ Delgado M, Avril A, Prigent J, Dano J (29 January 2021). «Ricin Antibodies’ Neutralizing Capacity against Different Ricin Isoforms and Cultivars». Toxins. 13 (2): 100. doi:10.3390/toxins13020100. PMC 7911099. PMID 33573016.
- ^ a b Levy J (2011). Poison: An Illustrated History. Guilford, Connecticut: Lyons Press. p. 133. ISBN 978-0-7627-7056-4.
- ^ «Oil cake (chemistry)». Encyclopædia Britannica.
- ^ Soto-Blanco B, Sinhorini IL, Gorniak SL, Schumaher-Henrique B (June 2002). «Ricinus communis cake poisoning in a dog». Vet Hum Toxicol. 44 (3): 155–156. PMID 12046967.
- ^ Wedin GP, Neal JS, Everson GW, Krenzelok EP (May 1986). «Castor bean poisoning». Am J Emerg Med. 4 (3): 259–261. doi:10.1016/0735-6757(86)90080-X. PMID 3964368.
- ^ Rauber A, Heard J (December 1985). «Castor bean toxicity re-examined: a new perspective». Vet Hum Toxicol. 27 (6): 498–502. PMID 4082461.
- ^ «Survived after ingesting 30 castor beans». The Salt Lake Tribune. 3 October 2013. Retrieved 3 August 2014.
- ^ Baselt RC (2011). Disposition of Toxic Drugs and Chemicals in Man (Ninth ed.). Seal Beach, California: Biomedical Publications. pp. 1497–1499. ISBN 978-0-9626523-8-7.
- ^ «HHS and USDA Select Agents and Toxins 7 CFR Part 331, 9 CFR Part 121, and 42 CFR Part 73» (PDF). cdc.gov. Archived from the original (PDF) on 17 January 2009.
- ^ «Permissible Toxin Amounts». National Select Agent Registry. 10 September 2020.
- ^ «40 C.F.R.: Appendix A to Part 355 – The List of Extremely Hazardous Substances and Their Threshold Planning Quantities» (PDF). Code of Federal Regulations (1 July 2008 ed.). Government Printing Office. Archived from the original (PDF) on 25 February 2012. Retrieved 29 October 2011.
- ^ Augerson WS, Spektor DM (2000). A Review of the Scientific Literature as it Pertains to Gulf War Illnesses. Rand Corporation (Report). Chemical and Biological Warfare Agents. Vol. 5. United States Dept. of Defense, Office of the Secretary of Defense, National Defense Research Institute (U.S.). doi:10.7249/MR1018.5. ISBN 978-0-8330-2680-4.[page needed]
- ^ «The Avalon Project – Laws of War: Laws and Customs of War on Land (Hague II); July 29, 1899». Avalon.law.yale.edu. Retrieved 1 September 2010.
- ^ Gupta R (2009). Handbook of Toxicology of Chemical Warfare Agents. Boston: Academic Press. ISBN 978-0-12-374484-5.[page needed]
- ^ Romano Jr JA, Salem M, Lukey BJ (2007). Chemical Warfare Agents: Chemistry, Pharmacology, Toxicology, and Therapeutics, Second Edition. CRC Press. p. 437. ISBN 978-1-4200-4662-5.
- ^ «Ricin – Biological Weapons». www.globalsecurity.org.
- ^ Edwards, Richard (19 June 2008). «Poison-tip umbrella assassination of Georgi Markov reinvestigated». The Telegraph. Archived from the original on 12 January 2022.
- ^ «Cornell University Department of Animal Science». Ansci.cornell.edu. Retrieved 7 May 2012.
- ^ Kortepeter MG, Parker GW (1999). «Potential biological weapons threats». Emerging Infect. Dis. 5 (4): 523–527. doi:10.3201/eid0504.990411. PMC 2627749. PMID 10458957.
- ^ van Aken J (2001). «Biological Weapons: Research Projects of the German Army». Backgrounder Series No. 7. The Sunshine Project. Archived from the original on 8 January 2013.
- ^ «RiVax™ Ricin Toxin Vaccine». Soligenix, Inc. Retrieved 28 June 2017.
- ^ Hackett DW (11 February 2019). «Ricin Vaccine Candidate Rivax Awarded Patent Protection». Precision Vaccinations. Houston TX: Precision Vax Llc. Retrieved 27 February 2019.
- ^ Stillmark, Hermann (1888). Über Ricin, ein giftiges Ferment aus den Samen von Ricinus comm. L. und einigen anderen Euphorbiaceen [About ricin, a poisonous ferment [i.e., enzyme] from the seeds of Ricinus communis L. and some other Euphorbiaceae] (M.D. thesis) (in German). Dorpat, Estonia: University of Dorpat.
- ^ Stillmark H (1889). «Ueber ricin» [About ricin]. Arbeiten des Pharmakologischen Institutes zu Dorpat (in German). 3: 59–151.
- ^ The Russian physician N.A. Bubnow and the Australian physician Thomas Storie Dixson (1854–1932) probably isolated ricin in 1887 at the University of Strassburg (Strasbourg), Germany; however, Dixson mistakenly believed that ricin was a glycoside, whereas it is actually a protein.
- Dixson, Thomas (March 1887). «Ricinus communis». Australasian Medical Gazette. 6: 137–138, 155–158.
- Vogl A (1892). Pharmakognosie (in German). Vienna, Austria: Carl Gerold’s Sohn. p. 204. From p. 204: «Bubnow und Dixson (1887) erhielten aus den entfetteten Samen … vielleicht eine sogenannte Phytalalbumose darstellt.» (Bubnow and Dixson (1887) obtained, from the defatted seeds by extraction with dilute hydrochloric acid, a glycoside ([which they called] Ricinon) that belongs to the acid anhydrides [and that is] of very drastic effect. Mr. Stillmark (1889) finally precipitated, from the seeds and oilcake, a very poisonous substance, Ricin, (about 3% of the air-dried seeds) that’s insoluble in alcohol and that probably is a protein, an amorphous enzyme, perhaps a so-called phytalbumin.)
- Finnemore H (29 July 1905). «Castor oil – part 1». Pharmaceutical Journal. 75: 137–138. See p. 137.
- Cook B. Dixson, Thomas Storie (1854–1932). Australian Dictionary of Biography. National Centre of Biography, Australian National University.
- ^ «Ricin and the umbrella murder». CNN. 7 January 2003. Retrieved 15 March 2008.
- ^ Thomas DM (1998). Alexander Solzhenitsyn: A Century in His Life (First ed.). St. Martin’s Press. pp. 368–378. ISBN 978-0756760113.
- ^ «Internet dating couple jailed for plotting IS attack in Britain». Guernsey Press. 22 February 2018. One of many news items on plots to use ricin for terrorism.
- ^ «Letters to NYC Mayor Bloomberg contained ricin». MSN News. Associated Press. 30 May 2013. Archived from the original on 16 June 2013.
- ^ Harris P (8 June 2013). «Bit-part actor charged over plot to frame husband for ricin letters». The Guardian.
- ^ McLaughlin EC (16 July 2014). «Texas actress who sent Obama ricin sentenced to 18 years». CNN. Retrieved 16 July 2014.
- ^ «Ricin detected in mail sent to Pentagon». CNN. 10 October 2018.
- ^ Maravelias P (27 July 2019). «Suspicious substance which caused Pelican Bay building evacuation identified as ricin». KRCR-TV.
- ^ Roth A (27 April 2020). «Prague mayor under police protection amid reports of Russian plot». The Guardian. Retrieved 29 April 2020.
- ^ «Police protecting Prague mayor after ‘murder plot’«. BBC News. 29 April 2020. Retrieved 29 April 2020.
- ^ Mortkowitz S (6 May 2020). «Czech president lashes out at Prague mayor under police protection». Politico. Retrieved 7 May 2020.
- ^ «German prosecutors arrest man over alleged ricin attack plot». The Guardian. Associated Press. 14 June 2018.
- ^ Connolly, Kate (8 January 2023). «German police arrest Iranian man suspected of planning chemical attack». The Guardian.
- ^ «Things You Should Know About Ricin Before Watching the ‘Breaking Bad’ Finale». National Geographic. National Geographic Society. 27 September 2013. Archived from the original on 8 March 2021. Retrieved 2 May 2015.
- ^ «Woman tried to poison mother in plot inspired by Breaking Bad, court told». The Guardian. London. 22 September 2014. Retrieved 2 May 2015.
- ^ Noble A (15 September 2014). «Guilty plea in Georgetown University ricin case with tie to ‘Breaking Bad’«. The Washington Times. Retrieved 2 May 2015.
- ^ «Breaking Bad fan guilty of Dark Web ricin plot». BBC News. 29 July 2015. Retrieved 29 July 2015.
External links[edit]
Wikimedia Commons has media related to Ricin.
- Studies showing lack of toxicity of castor oil from the US Public Health Service
- Castor bean information at Purdue University
- Plants Poisonous to Livestock – Ricin information at Cornell University
- Ricin cancer therapy tested at BBC
- Ricin – Emergency Preparations at CDC
- Emergency Response Card – Ricin at CDC
- Overview of all the structural information available in the PDB for UniProt: P02879 (Ricin) at the PDBe-KB.
Рицин – это сильнейший естественный яд, который выделяют в процессе производственной обработки распространенного лекарственного растения под названием клещевина обыкновенная.
Помимо умышленного применения в качестве отравляющего вещества, рицином, который отличается доступностью и высокой токсичностью, еще со времен Первой мировой войны интересуются специалисты в области бактериологического оружия.
Известно, что рицин в 6 раз более ядовит, чем цианистый калий. Поскольку небольшой дозы рицина размером с булавочную головку достаточно, чтобы убить взрослого человека, способы применения рицина в качестве оружия массового поражения изучались военными ведомствами разных стран, однако из-за ряда недостатков это вещество так и не было принято на вооружение. Тем не менее, рицин нашёл применение у спецслужб.
Одним из наиболее известных инцидентов с применением рицина стало убийство болгарского диссидента Георгия Маркова, который был отравлен в 1978 году при помощи укола зонтиком особой конструкции. По другим данным оружие убийцы было пневматическим ружьем, стрелявшим микрокапсулой с рицином и замаскированным под зонтик. Доза введенная Маркову составила не более 450 мкг (или 0,45 миллиграмма).
Через несколько дней Марков умер, зато другой жертве – бывшему редактору болгарского государственного радио – В. Костову повезло больше. Капсула с рицином попала в его тело в результате выстрела, однако задержала отраву толстая шерстяная кофта.
Простота получения токсина сделала его потенциально доступным для террористических групп. Так, в 2001 году пресса сообщала об обнаружении инструкций по изготовлению рицина на разгромленной базе «Аль-Каида» в Кабуле. В 2003 году некоторое количество рицина было найдено у террористов в Лондоне, следы рицина обнаружились в ячейке хранения на Лионском вокзале в Париже.
В 2013 году ряд лиц из штата Миссисипи были арестованы за попытку послать Президенту США Бараку Обаме и другим высокопоставленным лицам США письма с рицином. Так в мае этого же года мэру города Нью-Йорк прислали письмо с угрозами, содержащее рицин, предположительно в ответ на деятельность общественной организации «Мэры против нелегального оружия». Позднее в Техасе предъявлены обвинения актрисе Шэннон Ричардсон, подозреваемой в рассылке писем со смертельным ядом американским политикам.
Письма с рицином 2003 года относятся к инциденту с двумя письмами, содержащими в себе рицин, найденных в двух отдельных случаях в период с октября по ноябрь 2003 года. Одно письмо было отправлено по почте в Белый дом, и его перехватили на объекте обработки; другое письмо (без адреса) было обнаружено в Южной Каролине.
Письма были отправлены от имени человека, называющего себя «Падшим ангелом» (англ. «Fallen Angel»). Отправитель, который утверждал, что является владельцем транспортной компании, выразил недовольство по поводу изменений в федеральные правила грузоперевозки. В 2004 году федеральными правоохранительными органами, расследующими дело, была предложена награда в $ 100000 тому, кто поможет разыскать это лицо, но на сегодняшний день эту награду никто не получил.
Письма с рицином 2013 года — это три письма, содержащие в себе высокотоксичное вещество рицин, которые были посланы трём разным адресатам.
16 апреля 2013 года, конверт, который предварительно прошёл тест и получил положительный результат на рицин, был перехвачен на пути в Капитолий в вашингтонском почтовом отделении. Согласно сообщениям, конверт был адресован в офис сенатора—республиканца от штата Миссисипи Роджера Уикера.
17 апреля 2013 года конверт, который был направлен на имя президента США Барака Обамы, предварительно был протестирован и дал положительный результат на рицин.
Оба письма, которые были отправлены из Мемфиса, штат Теннесси, включали в себя письма с фразами «No one wanted to listen to me before. There are still ‘Missing Pieces.’ Maybe I have your attention now even if that means someone must die. This must stop. To see a wrong and not expose it, is to become a silent partner to its continuance.» и «I am KC and I approve this message». («Никто раньше меня не хотел слушать. Есть еще «Пропущенные пьесы». Возможно, теперь я обращу ваше внимание, даже если это означает, что кто-то должен умереть. Это должно прекратиться. Чтобы увидеть неправду, а не раскрывать ее, нужно стать молчаливым партнером для ее продолжения. и «Я есть КС, и я одобряю это сообщение»).
Третье письмо было отправлено из Миссисипи судье округа Ли Сэди Холланду, который получил и открыл его 10 апреля. В письме содержался аналогичный текст; письмо было отправлено на тестирование, которое дало положительный результат на рицин.
Происхождение вещества
Растение-источник рицина под названием клещевина обыкновенная произрастает по всему земному шару. Клещевина несколько напоминает пальму, имеет большие, похожие на кленовые, листья, а семена созревают в коробочках, сплошь покрытых шипами. Растение отличается ярким цветом, как правило, имеет красно-зеленый или коричневатый окрас. Клещевина нетребовательна и приятна на вид, растение часто выбирают для посадки на приусадебных участках в декоративных целях.
Основное применение однолетнего кустарника – изготовление касторового масла. Отрава же получается из «отходов» производства – переработанных касторовых бобов. Бобы сами по себе, а также производные растения, которые изготавливаются в промышленных масштабах и попадают на полки аптек, откуда отпускаются без рецепта, совершенно безвредны для здоровья человека. Но поврежденные семена представляют серьезную угрозу жизни животного или человека, который их проглотит.
Кроме непосредственно рицина в бобах содержится небольшое количество схожего вещества.
Проникновение яда в организм человека
Что такое рицин и как он действует, попадая в организм?
Вдыхание токсичного вещества, которое в шесть раз сильнее цианистого калия, проявляется характерными симптомами через восемь часов после непосредственно происшествия, при проглатывании признаки появляются уже через шесть часов.
Смерть, как правило, наступает через трое-четверо суток. Осложняется ситуация тем, что специфического противоядия против рицина на данный момент времени не существует.
Основной путь попадания яда в организм – пищевой. Через кожу вещество не проникает, но длительное вдыхание отравленного воздуха или непосредственно нескольких кристаллов чистого вещества провоцирует серьезнейшее отравление с высокой вероятностью смертельного исхода.
Максимальное быстродействие достигается при введении вещества в кровь посредством инъекции.
Механизм действия и летальность
Проникая в организм, отравляющее вещество действует комплексно и оперативно. Молекула рицина состоит из двух основных частей, одна из которых используется непосредственно для нападения, атаки, другая – для маскировки. Крупная белковая молекула рицина способна эффективно блокировать механизмы действия клеток человеческого тела, вследствие чего те полностью перестают функционировать. При отсутствии своевременных лечебных мероприятий это приводит к отказу органов.
Естественная иммунная защита человеческого организма может препятствовать проникновению яда в клетки, однако тут начинает работу маскировочная часть рицина. Компонент молекулы ядовитого вещества поступает таким образом, что клетки в организме человека признают рицин дружественным элементом и пропускают отраву.
Вещество ядовито и для самого растения, в котором вырабатывается. Однако клещевина преодолевает токсичность, делая яд одной неделимой молекулой, без возможности «отключения» маскировочных функций, которые не дают одновременно вступить в действие и «нападающей» части. Связи разрушаются, когда рицин выделяется, становясь отдельной молекулой.
Доказано также довольно любопытное свойство рицина, которое имеет потенциал для дальнейших лабораторных исследований. Вещество может расщепляться и создавать новые, неизвестные науке и не встречающиеся в природе, токсичные соединения с другими молекулами.
Для человека смертельная доза составляет 0,003 миллиграмм чистого вещества на один килограмм массы тела. Это значит, что для серьезного отравления с возможным смертельным исходом достаточно и 1 мг вещества, которое имеет вид белого порошка, или употребления в пищу двадцати семян растения для взрослого человека и шести для ребенка.
Симптомы отравления
При проникновении яда в организм наблюдаются типичные симптомы интоксикации и отправления, однако, более интенсивные и продолжительные. Со стороны желудочно-кишечного тракта характерно нарушение стула, диарея с кровяными примесями, которая не купируется лекарственными препаратами, сильная тошнота и непрекращающаяся рвота. Пострадавший может ощущать жжение в пищеварительном тракте и колики, изнеможение и обезвоживание, которые являются уже не первичными признаками, а следствием непрекращающихся рвоты и диареи.
Симптомы отравления рицином включают в себя падение артериального давления, выраженные судороги, бледность кожи и синюшность носогубного треугольника. При отравлении путем вдыхания кристаллов чистого вещества возникает кашель, иногда с кровью и затрудненность дыхания. В преобладающем большинстве случаев, когда токсин попадает в организм с пищей, наблюдаются сильные боли в животе, колики, увеличение лимфатических узлов. Если вещество было введение инъекционно, то мышцы в месте укола парализуются.
Сильное отравление рицином характеризуется помутнением сознания, нарушением ориентации в пространстве, галлюцинациями, внутренними кровоизлияниями. Одним из типичных признаков, который можно выявить еще в то время, когда медицинская помощь способна предупредить дальнейшее распространение яда, является появление множественных мелких кровоизлияний на сетчатке глаза.
Обнаружение рицина в организме подтверждается различными диагностическими мероприятиями. Но в условиях, когда каждая минута на счету, специалисты первым делом проводят все необходимые лечебные мероприятия, а затем уже выясняют первопричину опасного состояния больного.
Лечение отравления рицином
Противоядие от рицина, которое могло бы использоваться как эффективный антидот для введения пострадавшим, на данный момент времени еще не изобретено. Крупнейшими медицинскими исследовательскими центрами ведется разработка, но пока их деятельность в данном направлении не увенчалась успехом.
Лечение отравления рицином предполагает устранение симптомов и блокирование дальнейшего воздействия яда. Летальность и возникновение серьезных последствий отравления зависят от своевременного оказания пострадавшему помощи.
В медицинских учреждениях лечебные мероприятия включают в себя:
переливание крови;
назначение комплекса препаратов, в который входят обволакивающие средства, слабительное, сильные обезболивающие;
кислородная терапия;
глубокое промывание кишечника;
ощелачивание мочи.
Первая помощь предусматривает оперативное предупреждение дальнейшего распространения яда и немедленную транспортировку пострадавшего в больницу.
В домашних условиях оказание первой помощи происходит следующим образом:
пострадавшему следует дать обильное питье и активированный уголь (одна таблетка на 10 кг веса);
далее применяется обволакивающий раствор: кисель, рисовый отвар, крахмал;
для поддержания почек пострадавшему необходимо выпить стакан воды с растворенными в нем несколькими граммами пищевой соды.
Последствия отравления рицином
Рицин быстро поражает внутренние органы: в первую очередь страдает пищеварительная система (желудочно-кишечный тракт и вспомогательные железы), кроме того, токсическое вещество оказывает негативное влияние на сердце и сосуды, а также нервную систему. При своевременном медицинском вмешательстве успешно удается устранить опасные для жизни последствия (возможный отказ органов), но терапия возникающих острого токсического гепатита и геморрагического воспаления, которые склонны переходить в хроническую форму, занимает длительное время.
Идентификация
На рынке имеется ряд систем идентификации рицина. В своем каталоге Environics представляет систему ENVI Assay, которая позволяет идентифицировать рицин на месте в порошках, поверхностях или жидкостях за 15 минут.
ENVI Assay System Gold предлагает одноразовые отдельные комплекты для анализа семь очень ядовитых отравляющих веществ: рицина, ботулин- токсина, сибирской язвы, оспы, стафилококк-энтеротоксина (SEB), возбудителя туляремии (Francisella tularensis) и возбудителя чумы (Yersinia pestis). Тест-наборы системы ENVI Assay включают в себя все принадлежности, необходимые для выполнения теста: тест-картриджи, тампоны отбора проб, буферные контейнеры хранения проб, диспенсеры и реагенты антител и инструкции по применению — никаких дополнительных комплектов для отбора проб не требуется.
ВЫВОД
Растение-источник рицина культивируется во всем мире без какого-либо контроля. Добыча рицина не очень сложна, но получение хорошей продукции непросто. Диагноз трудно сделать, поскольку симптомы неспецифичны. Нет никакого противоядия, нет лекарств. Идентификация поля возможна в таких системах, как ENVI Assay, что облегчает диагностику у пациента.
Это может показаться пугающим, но хорошо помнить, что, если угроза существует, вероятность ее реализации по-прежнему относительно высока.
ТОКСИКОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА РИЦИНА
- Авторы
- Файлы
Таинственный яд «рицин» завоевал умы мировых и отечественных средств масс-медиа. Он становится главным оружием террористов, приходя на смену сибирской язве. Всемирную славу яду принесло отравление болгарского диссидента Георгия Мартова в Лондоне, когда на мосту Ватерлоо писателя укололи зонтиком, наконечник которого был отравлен рицином. В связи с этим мы провели исследование степени разработанности проблемы в контексте токсикологических аспектов. Согласно данным специальной литературы рицин — лектин, выделяемый из семян клещевины обыкновенной. Отравление рицином по своей клинической и патоморфологической картине может маскироваться под септические состояния, поэтому дифференциальная диагностика должна проводиться, прежде всего, между отравлением рицином и инфекционными заболеваниями. Особенностью действия рицина является разрастание соединительной ткани в паренхиматозных органах, в том числе и в межальвеолярных перегородках легких на фоне макрофагально-гистиоцитарной инфильтрации. Рицин вызывает характерное истощение лимфоидных органов с образованием многочисленных апоптотических телец, что позволяет рассматривать его как иммунотропный яд. Данные нарушения свидетельствовали о состоянии глубокой иммуносупрессии и акцидентальной инволюции тимуса. Механизм инициируемой рицином иммуносупрессии окончательно не изучен . Известно, что лектины, выделенные из различных растительных источников, являются мощными активаторами клеток иммунной системы и индукторами синтеза эндогенных биорегуляторов, в частности провоспалительных цитокинов, таких как ИЛ-1, ФНО-а и ИНФ-у. Избыток этих биологически активных пептидов может вызывать нарушения внутренних органов, приводить к системной воспалительной реакции и полиорганной недостаточности, нарушать проницаемость сосудов. Кроме того, ФНО-а и ИНФ-у, могут вызывать программируемую гибель лимфоцитов. Рицин проникает в клетки благодаря избирательному взаимодействию с галактозой клеточной мембраны, связываясь с которым, молекула рицина вначале фиксируется на цитоплазматической мембране, а затем по механизму эндоцитоза проникает внутрь клетки. Вакцина против рицина (RiVax), разработанная исследователями университета штата Техас, успешно прошла тестирование в рамках пилотного испытания на 15 волонтерах. По мнению разработчиков, такая вакцина необходима как для вооруженных сил, так и для мирного населения.
Библиографическая ссылка
Омарова Ш.О., Доника А.Д. ТОКСИКОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА РИЦИНА // Успехи современного естествознания. – 2011. – № 8.
– С. 125-126;
URL: https://natural-sciences.ru/ru/article/view?id=27719 (дата обращения: 24.05.2023).
Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания»
(Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления)
Рицин — бинарный токсин, получаемый из жмыха семян касторовых бобов Ricinus communis (клещевина обыкновенная). С конца Первой мировой войны он привлекает внимание специалистов в области химического и биологического оружия из-за высокой токсичности и доступности. В медицине рицин широко применяется для разработки иммунобиологических противоопухолевых препаратов из группы иммунотоксинов. Цель настоящее работы — анализ подходов к распознанию поражений рицином, вызванных профессиональной деятельностью по созданию иммунобиологических лекарственных препаратов и актами биологического терроризма. Рассмотрены молекулярная структура и механизм токсического действия рицина, его токсические и поражающие свойства. На конкретных примерах показана клиника, патоморфология и диагностика поражений, возникающих при энтеральном, парентеральном и ингаляционном экспонировании к рицину.
Супотницкий М.В. Распознание поражений рицином // Прикладная токсикология. — 2013. — № 1 (9). — С. 44–49.
The ricin is binary toxin, received from seed meal of castor beans of Ricinus communis. Since World war I ricin attracts attention of specialists in the field of chemical and biological weapon due to high toxicity and availability. The ricin is widely used in medicine for development of immunological antitumor immunotoxin group remedies. The aim of our research was analysis of approaches to identification of ricin damage, caused by professional activity on creation of immunobiological drugs and by biological terrorist acts. The molecular structure and toxic mechanism of ricin action as well as it toxic and destructive effects are considered in the article. The clinical picture, pathomorphology and diagnostic of damages, arising after enteral, parenteral and exhalative exposure of ricin are also given in the article.
Supotnitskiy M. V. The recognition of damage by ricin // Applied toxicology— 2013. — № 1 (9). — P. 44–49.
Рицин (ricin toxin) — бинарный токсин, получаемый из жмыха семян касторовых бобов Ricinus communis (клещевина обыкновенная). В медицине широко применяется для разработки иммунобиологических противоопухолевых лекарственных препаратов из группы иммунотоксинов. Получение неочищенного рицина не представляет особых сложностей для террористических организаций. Цель настоящее работы — анализ подходов к распознанию поражений рицином, связанных с профессиональной деятельностью по созданию иммунобиологических лекарственных препаратов и вызванных актами биотеррора.
Препараты рицина. Основными производителями касторовых бобов являются Китай, Индия, Бангладеш и США, где они используются для получения касторового масла. В самом масле рицина нет — технологическая цепочка его получения предполагает инактивацию токсина нагреванием. В жмыхе семян касторовых бобов содержится 0,5–5% рицина, образующего комплекс с агглютинином. Агглютинин — лектин гликолипиной природы. Прямым цитотоксическим действием он не обладает, но способен агглютинировать и лизировать эритроциты. Клинически значимый гемолиз он вызывает только после внутривенного введения. Препараты рицина различаются агрегатным состоянием, степенью очистки и наличием изоформ токсина.
Очищенный рицин представляет собой белый порошок без запаха. Разработаны технологии его выделения и очистки в кристаллическом виде. Рицин хорошо растворим в воде и сохраняет токсические свойства в широком диапазоне pH. В водных растворах он инактивируется при температуре 80 0С в течение часа, в сухом виде более устойчив [1, 2, 3].
Кроме рицина в касторовых бобах содержатся небольшие количества токсического алкалоида рицинина. Он экстрагируется совместно с рицином. Случаев отравления людей очищенным рицинином не описано [4].
Молекулярная структура и механизм действия. Молекулярная масса рицина — 60–65 кДа. Рицин — типичный АВ-токсин. На рибосомах синтезируется в виде цельной полипептидной цепи. В вакуолях клеток растения эта цепь расщепляется в единственном сайте, образуя две субъединицы: А (ферментативная) и В (связывающая), остающиеся соединенными через дисульфидную связь. Субъединицы сами по себе не токсичны, токсическое действие проявляется только при условии кооперативного взаимодействия обеих субъединиц в составе молекулы рицина. B-цепь представляет собой лектин, связывающийся с галактозой или N-ацетилгалактозамином гликопротеинов и гликолипидов на поверхности клетки мишени, вызывая эндоцитоз и проникновение молекулы рицина из ранней эндосомы в транспортную сеть Гольджи (рис. 1).
 Рис. 1. Механизм токсического действия рицина. После взаимодействия В-субъединицы рицина с галактозой или N-ацетилгалактозамином на поверхности клетки, молекула токсина подвергается эндоцитозу (1, 2). Большинство молекул рицина выводится обратно на поверхность клетки благодаря механизму экзоцитоза (3). Если везикулы сливаются с лизосомами, то рицин разрушается благодаря механизму протеолиза (4). Часть рицин-содержащих везикул сливается с транспортной сетью Гольджи (trans-Golgi network, TGN) (5), оттуда они также могут быть выведены на поверхность клетки (6). Токсическое действие рицин оказывает тогда, когда его молекула распадается на субъединицы и А-субъединица пенетрирует мембрану TGN и проникает в цитозоль (7) где катализирует депуринизацию (depurination) рибосом, останавливая синтез белка. По [1]
Рис. 1. Механизм токсического действия рицина. После взаимодействия В-субъединицы рицина с галактозой или N-ацетилгалактозамином на поверхности клетки, молекула токсина подвергается эндоцитозу (1, 2). Большинство молекул рицина выводится обратно на поверхность клетки благодаря механизму экзоцитоза (3). Если везикулы сливаются с лизосомами, то рицин разрушается благодаря механизму протеолиза (4). Часть рицин-содержащих везикул сливается с транспортной сетью Гольджи (trans-Golgi network, TGN) (5), оттуда они также могут быть выведены на поверхность клетки (6). Токсическое действие рицин оказывает тогда, когда его молекула распадается на субъединицы и А-субъединица пенетрирует мембрану TGN и проникает в цитозоль (7) где катализирует депуринизацию (depurination) рибосом, останавливая синтез белка. По [1]
А-субъединица рицина — высокоэффективная N-гликозидаза. Она действует через удаление специфического аденинового основания (А4324) вблизи 3′-конца 28S рибосомальной РНК. Одна А-субъединица способна в минуту инактивировать около 1500 рибосом. Аминоацилтранспортная РНК не соединяется с усеченной 28S рибосомальной РНК. Синтез белка останавливается, и запускается механизм апоптоза клетки [2, 5]. Аминокислотная последовательность А-субъединицы рицина имеет обширную гомологию с энзиматической субъединицей шига-токсина. Механизмы действия обоих ферментов одинаковы [1].
Токсические свойства. Рицин обладает прямым цитотоксическим действием. Летальные дозы рицина зависят от способа ведения в организм животного, от вида животного, степени очистки рицина, условий его хранения и наличия изоформ в препарате.
Lct50 мелкодисперсного аэрозоля очищенного рицина (размер частиц аэрозоля 1–5 мкм) для крыс в пределах 4,54–12,7 мг.мин/м3 (LD50 3,7–9,8 мкг/кг) [3]. Летальные дозы рицина при ингаляционном поражении для обезьян резусов и африканских зеленых обезьян составили 15,0 и 5,8 мкг/кг, [6]. Минимальная ингаляционная летальная доза мелкодисперсного аэрозоля рицина для человека близка к 4,0 мкг/кг [7]. При энтеральном отравлении для человека ее оценивают в диапазоне от 1 до 20 мг/кг [2]. Снижение токсичности рицина при попадании в организм через ЖКТ, вызвано его разрушением панкреатическими ферментами. Симптомы отравления и причина смерти зависят от места аппликации токсина [1, 8].
Интоксикация экспериментального животного А-цепью рицина при различных путях его введения проявляется виде синдрома проницаемости сосудов (гипоальбунемия, отеки), вызванного повреждением клеток эндотелия. Мыши, кролики, приматы, ингаляционно экспонированные к высоким дозам рицина, всегда имели тяжелые поражения легочной ткани, сопровождающиеся отеком легких и затоплением альвеол (alveolar flooding), приводящие их к смерти вследствие гипоксемии. Появление первого клинического симптома ингаляционного отравления рицином — отдышки, C. Wilhelmseann и L. Pitt [9] связывают с начавшимся затоплением альвеол; отека легких — с проявлением синдрома проницаемости сосудов.
Патологические последствия сосудистых нарушений, индуцированные токсином, более серьезны, чем прямое действие токсина на клетки. Высокие дозы рицина, введенного экспериментальным животным внутривенно, уже через 4 ч повреждали Купферовы клетки, затем развивались повреждение клеток эндотелия и диссеминированная внутрисосудистая коагуляция. В сосудистой сети печени формировались тромбы, приводящие к гепатоцеллюлярному некрозу. Животные погибали от гепатоцеллюлярной и ренальной недостаточности. Повреждение сосудистого эндотелия, вызванного внутривенным введением рицина, может привести к периваскулярному отеку легких. Заглатывание рицина вызывает некроз эпителия желудочно-кишечного тракта, локальное кровотечение и некроз печени, селезенки и почек. Внутримышечное введение сопровождается локальным некрозом мышц и региональных лимфатических узлов с умеренным поражением висцеральных органов [8].
Клиника энтерального поражения. Из 751 обобщенных случаев отравления касторовыми бобами, смертельными оказались 19 (смертность 1,9%). При отсутствии эффективной терапии смертность достигает 6 %. Количество съеденных бобов, вызвавших летальный исход у отравленного (или отравившегося) человека, варьирует от 10 до 20 штук. Клиника отравления однообразна. В течение нескольких часов после приема в пищу касторовых бобов у отравленного появляется чувство тошноты, развиваются рвота и боли в брюшной полости; затем появляются диарея и кровотечение из ануса. К ним присоединяются анурия, судороги, расширение зрачков, повышается температура тела. Отравленного человека мучают чувство жажды, боли в груди, головные боли, развивается сосудистый коллапс и шок. Смерть наступает на третий день после приема касторовых бобов или позже. На аутопсии у погибших от отравления рицином обнаруживают мультифокальное изъязвление и геморрагии на слизистой желудка и тонкого кишечника, которые могут быть очень выраженными; лимфоидный некроз мезентеральных лимфоидных узлов, некроз Купферовых клеток, некротические очаги в печени, диффузный нефрит и спленит [8].
Клиника ингаляционного поражения. Ингаляционное поражение рицином людей и экспериментальных животных возможно в том случае, если размер частиц аэрозоля находится в пределах 1–5 мкм, более крупные частицы задерживаются в верхних дыхательных путях. Частицы рицина меньше микрона выходят из легких при выдохе [8].
Данных по ингаляционному поражению людей рицином в доступной литературе найти не удалось. Ингаляционное экспонирование крыс к рицину вызывает у них диффузную некротизирующую пневмонию с интерстициальным и альвеолярным воспалением и отеком, но не ранее 8 ч после ингаляции. Через 12 ч отмечаются первые признаки нарушения проницаемости воздушно-кровяного барьера и цитотоксического действия рицина: в жидкости бронхиального пространства обнаруживаются повышенное содержание общего белка и воспалительные клетки крови. Наличие воспалительного процесса показывает и общая формула крови.
Через 18 ч после ингаляции рицина уже заметен альвеолярный отек и увеличено количество экстраваскулярной жидкости в легких. Через 30 ч выраженная артериальная гипоксемия и ацидоз, гистопатологические доказательства альвеолярного отека. Иммунохимические исследования показали, что ингалированный рицин связывается с реснитчатыми клетками, альвеолярными макрофагами и альвеолярными обкладочными клетками дыхательных путей [8].
При сравнительном исследовании поражений легких крыс, вызванных ингаляцией рицина разной степени очистки (в сопоставимых дозах по очищенному рицину), установлено, что неочищенный рицин вызывает более обширные и разнообразные поражения, чем очищенный [3].
В исследованиях на нечеловекообразных приматах установлено, что ингаляционная токсичность рицина имеет дозозависимый преклинический период 8–24 ч. В клиническом периоде у животных наблюдается анорексия, прогрессирующее снижается двигательная активность, развивается отдышка. Через 36–48 ч после ингаляции рицина они погибали от легочной недостаточности. Скорость гибели животных также зависела от ингалированной дозы. У всех обезьян, погибших от ингаляционного отравления рицином, обнаружили гнойно-фибринозную пневмонию, разной выраженности диффузный некроз легочной ткани и острые воспалительные изменения нижних дыхательных путей [8].
Подробное описание патологии мелкодисперсного аэрозоля очищенного рицина у нечеловекообразных приматов (макак резусов) приведено в работе [9]. Пять животных весом 5.9–6.3 кг были экспонированы к частицам аэрозоля рицина (размер частиц аэрозоля 1–2 мкм) из расчета ингаляционной дозы 21,0–41,8 мкг/кг. Средний диаметр частиц рицина 1,2 мкм, их основная масса осела в участке соединения бронхиол с альвеолами. В период времени между 36 ч и 48 ч после ингаляции большая часть животных погибла. Оставшиеся в живых обезьяны были умерщвлены и затем подверглись патологоанатомическому исследованию.
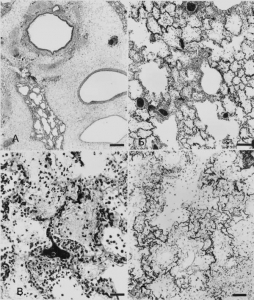
Наиболее тяжелые видимые и микроскопические поражения обнаружены в нижнем респиратором тракте животных. В грудной полости находились серозная или сероангинозная жидкость и нити фибрина. Висцеральная легочная плевра была покрыта пленкой фибрина. Легкие не колапсированы, но тяжелые, плотной упругой консистенции, покрытые жидкостью. Их окраска пестрая, с красной и пурпурной исчерченностью (рис. 2).
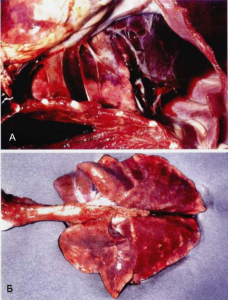
В трахее и бронхах обнаружена светлая пенистая жидкость, вытекающая из отверстия гортани. Медиастинум утолщен вследствие студенистого отека (gelatinous edema), медиастинальные лимфатические узлы расширены и отечны. Перикардиальная сумка заполнена серозной или серозноангинозной жидкостью и расширена. Легочные доли у всех обезьян имели не очень заметный мультифокальный сливающийся некроз и воспалительные изменения эпителия воздушных путей, перибронховаскулярный отек, альвеолярное затопление (alveolar flooding) и фибринозно-гнойные альвеолиты (fibrinopurulent alveolitis) как проявление интерстициальной пневмонии с участками некроза.
Нити перибронховаскулярной соединительной ткани разделены эозинофильным белковым материалом (отек). Перибронхиальные лимфатические узлы расширены фибриллярным эозинофильным материалом (отек и фибрин) с эритроцитами, нейтрофилами, лимфоцитами и макрофагами. Лимфоциты в ассоциированных с бронхами лимфоидных тканях истощенны (depleted). На отдельных бронхах эпителий остался интактным, другие частично утратили подкладочный эпителий (lining epithelium) (рис 3, А).
Рис. 3. Гистологические изменения в легочной ткани у обезьян, экспонированных к мелкодисперсному аэрозолю рицина.
А. Выраженный периваскулярный и перибронхиальный отек с лимфангиестазией (lymphangiectasia) и истощением бронхо-ассоциированной лимфоидной ткани. Полоса соответствует 333 мкм. Б. Бронхоальвеолярный некроз с альвеолярным затоплением (alveolar flooding) и гнойнофибринозным перибронхиолитом и альвеолитом. Полоса соответствует 133 мкм. В. Гнойнофибринозный альвеолит. Полоса соответствует 33 мкм. Г. Внутриальвеолярное отложение полимеризованного фибрина. Полоса соответствует 66 мкм. Окрашивание фосфовольфрамовым кислым гематоксилином. По [9]
Перибронхиальные инфильтраты включают нейтрофилы, лимфоциты, и макрофаги. Многие маленькие бронхиолы почти полностью утратили эпителий, сохранив только гладкие мышцы (см. рис. 3, Б). Терминальные бронхиолы некротизированы (респираторные бронхиолы, альвеолярные проходы и соседние альвеолы) и «раздуты» миграцией эозинофилов, эритроцитов, альвеолярных макрофагов, клеточного дебриса и отложением нитей фибрина. Большинство альвеол утратили подкладочный эпителий. Альвеолярное септальное интерстициальное пространство утолщено эозинофильным белковым материалом, капилляры переполнены и инфильтрированы нейтрофилами и макрофагами (см. рис. 3, В). Капилляры подкладочного эндотелия и большие кровеносные сосуды «раздуты». Имеет место внутриальвеолярное отложение полимеризованного фибрина (см. рис. 3, Г).
Верхний респираторный тракт воспален незначительно. Трахея у всех обезьян и гортань у трех обезьян имели небольшое количество мигрировавших нейтрофилов и редкие очаги некротических эпителиальных клеток. В просвете обнаружено незначительное количество воспалительного экссудата, включающего разрушенные нейтрофилы, макрофаги, эритроциты, слущившиеся эпителиальные клетки и муцин.
Другие торакальные поражения выявлены вдоль легочного лимфатического дренажного протока. У всех обезьян синусы трахеобронхиальных лимфатических узлов утолщены отложением фибрина, гиперсегментированными нейтрофилами, макрофагами, некротизированным клеточным дебрисом. В трахеобронхиальных лимфатических узлах отдельных обезьян обнаружено выраженное лимфатическое истощение кортекса и кариолизис фолликулярных клеток. Соединительная ткань вокруг лимфатических узлов и центростремительные лимфатические протоки заполнены нейтрофилами, макрофагами, лимфоцитами, эритроцитами и фибрином. У двух обезьян обнаружен адренокортикальный некроз.
Клиника парентерального поражения. Клиника низких доз изучена в экспериментах по лечению рака. Раствор рицина пациентам вводили внутривенно (18–20 мкг/м2). Первые симптомы отравления у них появились через 4–6 ч после инъекции. Преобладали гриппозные симптомы, больные также жаловались на тошноту, рвоту, боли в мышцах и слабость. Такое состояние длилось у отравленных до двух суток. Смертельных исходов не было [10].
Клиника парентерального отравления рицином человека задокументирована при расследовании убийства в Лондоне в 1978 г. болгарского диссидента Георгия Марков. Из неустановленного оружия в него была выпушена 1,7 мм пуля, содержащая примерно 500 мкг рицина. Пуля представляла собой пустотелый шарик, состоящий на 9/10 из платины и 1/10 иридия, и была покрыта воском, который расплавлялся при температуре тела, высвобождая рицин [11].
Марков почти сразу почувствовал локальную боль в бедре, в участке, в который попала пуля. Затем, примерно в течение 5 ч, ощущение боли прошло. Марков не понял, что в него стреляли. В период 15–24 ч у него резко повысилась температура, появилось ощущение тошноты, началась рвота. Только через 36 ч после выстрела Марков доставлен в госпиталь в тяжелом состоянии и с высокой температурой и тахикардией, с увеличенными и болезненными паховыми лимфоузлами. Артериальное давление оставалось нормальным. На бедре вокруг участка инъекции рицина наблюдалась плотная воспаленная зона диаметром 6 см. Спустя чуть более двух суток после инъекции рицина у Маркова внезапно упало артериальное давление (пульс 160/мин), развились сосудистый коллапс и шок. Белые клетки крови — 26300/мм3, анурия. Еще до завершения третьих суток после инъекции рицина у него началась рвота с кровью. ЭКГ обнаружила полный атриовентрикулярный блок. Марков умер. Белые клетки крови на момент смерти — 32200/мм3 [11].
Внутримышечное и подкожное введение высоких доз рицина людям, обычно приводило к локальному лимфоидному некрозу, желудочно-кишечному кровотечению, некрозу печени, диффузному нефриту и сплениту. Сходные результаты были получены и в опытах на животных [8].
При внутривенном введении больших доз рицина, отравление может клинически маскироваться под сепсис (лихорадка, головная боль, головокружение, тошнота, анорексия, гипотония, абдоминальные боли) [2].
Диагностика поражения рицином. Предположение об отравлении рицином позволяют сделать данные анамнеза отравленного в сочетании с определенными клиническими симптомами и результатами патологоанатомического исследования. Окончательное подтверждение диагноза остается за лабораторными исследованиями, предполагающими обнаружение следов рицина в тканях отравленного, и/или на орудиях совершения преступления. У выживших после экспонирования к рицину подтвердить диагноз можно через две недели по обнаружению специфических антител в сыворотке крови. Поэтому для измерения образования антител у пациентов необходимо брать парные пробы сыворотки в острый период и период выздоровления.
Без определенной настороженности клиницистов единичное энтеральное поражение рицином пройдет под видом «нераспознанного пищевого отравления». Для специалистов, работавших с рицином и случайно экспонированных к нему, установление природы отравления особых проблем не вызовет. Подозрение о криминальном характере отравления должно появиться в результате сопоставления анализа личности (социального статуса) отравленного (коммерсант, политический или военный деятель) и возможных мотивов к убийству у окружающих его лиц, наличия у них легального доступа к рицину, и событий, предшествовавших отравлению. Например, в 1995 г. онколог Дебора Грин из Канзас-Сити пыталась убить своего мужа добавляя в пищу рицин, используемый для лечения онкологических больных в клинике, где она работала. Важны показания и самого отравленного, например, связывание им своего болезненного состояния с приемом какой-то пищи. На причастность рицина к отравлению будет указывать сочетание симптомов, характерных для пищевой интоксикации (рвота и боли в брюшной полости, диарея) и внутрисосудистой коагуляции (геморрагии, кровотечения из ануса).
Парентеральное отравление рицином можно предполагать при наличии в анамнезе отравленного указаний на получение им каких-то царапин или уколов, вызвавших жгучую боль в участке повреждения кожи, особенно если они были нанесены (сделаны) в общественных местах или на улице неизвестными лицами, или их происхождение осталось отравленному неизвестным. На отравление рицином (кроме общих симптомов отравления — тошнота, рвота, коллаптоидное состояние, признаки поражения печени и почек, и др.) будут указывать плотная воспаленная зона в участке инъекции, воспаление лимфатических узлов, ближайших к участку инъекции, локальный лимфоидный некроз, и симптомы внутрисосудистой коагуляции (геморрагии, желудочно-кишечное кровотечение). Внутривенное введение рицина не сопровождается местными симптомами. Предположение об отравлении рицином можно сделать на основе клинических признаков диссеминированной внутрисосудистой коагуляции, сочетающихся признаками гепатоцеллюлярной и ренальной недостаточности.
Поражение аэрозолем рицина можно предполагать в случае: 1) появления в течение одних суток больных с геморрагическими явлениями в сетчатке глаз и прогрессирующей легочной патологией, проявляющейся отеком легких, отдышкой, кровохарканием, нарастающими очагами деструкции легочной ткани; 2) обнаружением на секции патологии мелкодисперстного аэрозоля; 3) установлением эпидемиологии точечного источника и локализованности очага поражения[1].
Если рицин не обнаружен непосредственно в использованном для совершения преступления орудии (например, в случае с Марковым диагностика отравления рицином была облегчена обнаружением пули с рицином), то диагностировать (подтвердить) лабораторными способами отравление человека рицином сложно. Даже в тех случаях, когда такое отравление можно предполагать исходя из анамнеза жертвы, клиники и патологической анатомии отравления, необходимо иметь в виду то, что рицин распределяется в организме неравномерно, и быстро метаболизируется. Внутривенное введение крысам рицина, меченного I125, позволило установить, что через 30 мин наибольшее его количество находится в печени — до 45 %, в других органах и тканях его содержание значительно меньше (в мышцах — 13%, в селезенке — 8 %). Через 24 ч в организме животного удается обнаружить не более 11 % от введенного количества меченного рицина. До 70 % рицина выводится с мочой в первые сутки после отравления в виде низкомолекулярных метаболитов. Подтвердить факт рициновой ингаляции, по крайней мере, через 24 ч после инцидента, можно иммунологическими методами (различные варианты иммуноферментного анализа), отобрав материал из носовых ходов жертвы [8]. Чувствительность ELISA по рицину вполне удовлетворительна — 1 нг/мл при определении токсина в буферном растворе, моче и сыворотке крови [12].
Для дифференциальной диагностики необходимо исключить другие биологические агенты, такие как стафилококковый энтеротоксин В (СЭВ), возбудителей лихорадки Ку, туляремии, чумы, гемолитико-уремического синдрома (E. coli O104:H4; O157:H7) и некоторые отравляющие вещества (фосген, дифосген). Индуцируемый рицином отек легких ожидается намного позднее (1–3 дня после экспонирования) по сравнению с таковым, индуцируемым СЭВ (около 12 ч после экспонирования) или фосгеном (около 6 ч после экспонирования). Вероятно, интоксикация, вызванная рицином, будет прогрессировать несмотря на лечение антибиотиками, в отличие от инфекционного процесса. При ингаляционном поражении рицином не должно быть медиастинита, как в случае ингаляционной сибирской язвы. У больных, отравленных рицином, не следует ожидать клинической стабилизации, как в случае интоксикации СЭВ. К дополнительным признакам, подтверждающим клиническую картину или диагноз, после аэрозольного экспонирования к рицину относятся следующие: двусторонние инфильтраты на рентгенограммах грудной клетки, артериальная гипоксемия, нейтрофильный лейкоцитоз и бронхиальный аспират, богатый плазменным белком, что характерно для отека легких [13].
В качестве маркера отравления рицином может использоваться алкалоид рицинин. Он содержится в следовых количествах практически во всех препаратах рицина, но менее чем рицин подвержен метаболизации. Его определение в моче возможно даже спустя двое суток после экспонирования экспериментального животного к рицину [2].. При помощи ПЦР в большинстве рициновых препаратов можно обнаружить ДНК клещевины обыкновенной [13].
При исследовании рицинсодержащих препаратов, использованных для совершения преступления, необходимо обращать внимание не только на количественное содержание в них рицина, но и на их агрегатную форму (жидкость или порошок) и состав компонентов. В сухих препаратах целесообразно определить средний размер частиц рицина и выявить наличие дезагрегирующего наполнителя, в жидких — стабилизирующие соединения.
Иммунопрофилактика. Рицин обладает выраженными иммуногенными свойствами. На стадии проведения доклинических исследований находится несколько вакцин и иммуноглобулинов, обладающих протективным действием в отношении рицина. Подробное изложение достигнутого уровня и истории создания рициновых вакцин и антитоксинов приведено в работе [3]. Практического значения эти вакцины пока не имеют.
Лечение. Специфического лечения отравления рицином не существует. В настоящее время лечение ограничивается интенсивной поддерживающей и симптоматической терапией. При лечении поражения, возникшего после проникновения токсина через дыхательные пути, значительных усилий от врачей требует купирование отека легких и поддержание нормальной легочной вентиляции. При энтеральных поражениях лучше всего проводить энергичное промывание желудка с последующим применением слабительных средств, таких как цитрат магнезии. Активированный уголь малоэффективен для больших молекул, таких как рицин. Важное значение имеет возмещение объема потерь желудочно-кишечной жидкости. При парэнтеральном введении рицина в распоряжении врача остаются только поддерживающие и реанимационные мероприятия [2, 13].
В экспериментах на мышах показана возможность химиотерапии при отравлениях рицином. С этой целью могут быть использованы D-галактоза и ее производные (конкурирует с рицином за участки связывания на поверхности клеток-мишеней), азидотимидин (AZT) и брефельдин А (блокируют транспорт рицина по сети Гольджи) [8].
Список литературы
1. Bigalke H., Rummel A. Medical aspects of toxin weapons // Toxicol. — 2005. — Vol. 214. — P. 210–220.
2. Audi J., Belson M., Patel M. et al. Ricin poisoning. A comprehensive review // JAMA. — 2005 — Vol 294, № 18. — P. 2343–3251.
3. Griffiths G. D., Phillips G. J., Holley J. Holley inhalation toxicology of ricin preparations: animal models, prophylactic and therapeutic approaches to protection // Inhal. Toxicol. — 2007. — Vol. 19. — P. 873–887.
4. Darby S.M., Miller M.L., Allen R.O. Forensic determination of ricin and the alkaloid marker ricinine from castor bean extracts // J. Forensic. Sci. — 2001. — Vol. 46. — P. 1033–1042.
5. Lord M. J., Jolliffe N. A., Marsden C. J. et al. Ricin. Mechanisms of cytotoxicity // Toxicol. Rev. — 2003. — Vol. 22. — P. 53–64.
6. Wannemacher R. W., Anderson J. B. Inhalation ricin: aerosol procedures, toxicology and therapy // Inhalation toxicology, 2nd ed., eds. H. Salem and S. Katz. — 2006. — P. 973–980.
7. Антонов Н. С. Химическое оружие на рубеже двух столетий. — М: А/О Издательская группа «Прогресс»; 1994.
8. Franz D., Jaax N. Ricin toxin // Medical aspects of Chemical and Biological Warfare / Ed. F. R. Sidell, E. T. Tafuqi, D. R. Franz. — Washington, 1997. — P. 631–642.
9. Wilhelmseann C., Pitt L. Lesions of acute inhaled lethal ricin intoxication in Rhesus monkeys // Vet. Pathol. — 1996. — Vol. 33. — P. 296–302.
10. Fodstad O., Kvalheim G., Godal A. et al. Phase I study of the plant protein ricin // Cancer Res. — 1984. — Vol. 44. — P. 862–865.
11. Crompton R., Gall D. Georgi Markov: death in a pellet // Med. Leg. J. — 1980. — Vol. 48. — P. 51–62.
12. Poli M. A., Rivera V. R., Hewetson J. F. et al. Detection of ricin by colorimetric and chemiluminescence ELISA // Toxicon. — 1994. — Vol. 32, № 11. — P. 1371–1377.
13. Kortepeter M., Christopher G., Cieslak T. et al. USAMRIID’s medical management of biological causalities. Handbook. 4-ed. — Fort Detrick, Frederick, Maryland, 2001.
Библиографическое описание:
Супотницкий М.В. Распознание поражений рицином // Прикладная токсикология. — 2013. — № 1 (9). — С. 44–49.
Supotnitskiy M. V. The recognition of damage by ricin // Applied toxicology— 2013. — № 1 (9). — P. 44–49.
ССЫЛКИ ПО ТЕМЕ
Супотницкий М.В. Биологическая война. Введение в эпидемиологию искусственных эпидемических процессов и биологических поражений. М., 2013.
Супотницкий М.В. Ещё не получали белый порошок? Тогда мы идём к вам! // Свободная пресса .— 2012 .— Интервью от 9 и 17 июля .
Супотницкий М.В. Нанообъекты как новая биологическая угроза // Нанотехнологии и охрана здоровья. — 2013. — № 4. — С. 22–41.
Супотницкий М. В. Развитие биологического оружия еще не начиналось. Беседа с журналистом Иваном Ленцевым (полная версия) // Солдаты России . — 2009. — № 7–9. — С. 76–86.
Супотницкий М.В. Распознание поражения палитоксином // Жизнь без опасностей. — 2013. — № 3. — С. 56–67.
Супотницкий М.В. Эпидемиология искусственных эпидемических процессов как третий раздел эпидемиологии // Новости медицины и фармации. — 2013. — № 5 (449).
НЕСОСТОЯВШАЯСЯ БИОЛОГИЧЕСКАЯ ВОЙНА
(цикл статей по истории биологического оружия)
I. Боги-«биотеррористы» и древние отравители // Офицеры. — 2011. — № 5. — С. 56-61.
II. Средневековые «сеятели чумы» // Офицеры. — 2011. — № 6. — С. 56-61.
III. Бактериологические диверсии Первой мировой // Офицеры. — 2012 — № 1. — С. 58–63.
IV. Между мировыми войнами. Ученые и военные блуждали в «бактериальном тумане» и витали в «микробных облаках» // Офицеры. — 2012 — № 2. — С. 62–67.
V. Крах «отряда 731» // Офицеры. — 2012 — № 3. — С. 62–67.
VI. Повелители эпидемий // Офицеры. — 2012 — № 5. — С. 56–61.
VII. Бактериологическая война в Корее // Офицеры — 2013. — № 1. — С. 58–63.
ПОКАЗАНИЯ ВОЕННОПЛЕННЫХ АМЕРИКАНСКИХ ЛЕТЧИКОВ, ПРИМЕНЯВШИХ БО В 1952 Г. ВО ВРЕМЯ ВОЙНЫ НА КОРЕЙСКОМ ПОЛУОСТРОВЕ
VIII. От расцвета до запрета // Офицеры — 2013. — № 3. — С. 58–61.
ЗАБЫТАЯ ХИМИЧЕСКАЯ ВОЙНА 1915-1918 гг.
(цикл статей о применении химического оружия в годы Первой мировой войны)
I. Отравляющие вещества и химическое оружие Первой мировой войны // Офицеры. — 2010. — № 3 (47). — С. 56–61.
II. Тактическое применение химического оружия в годы Первой мировой войны // Офицеры. — 2010. — № 4 (48). — С. 52–57.
III. Применение химического оружия в операциях Первой мировой войны // Офицеры. — 2010. — № 5 (49). — С. 54–59.
IV. Химическая война в России // Офицеры. — 2010. — № 6 (50). — С. 52–57.
V. От «шлема Гипо» — к защите Зелинского. Как совершенствовались противогазы в годы Первой мировой войны // Офицеры. — 2011. — № 1 (51). — С. 50–55.
VI. Адское пламя. Огнеметы Первой мировой войны // Офицеры. — 2011. — № 2 (52). — С. 56–61.
VII. Отложенный апокалипсис. Почему Вторая мировая война не стала химической // Офицеры. — 2011. — № 3 (53). — С. 56–61.
[1] Сжатая эпидемическая кривая с пиком заболеваемости, «укладывающимся» в средние значения инкубационного периода болезни. Будет наблюдаться в большинстве случаев экспонирования к точечному источнику поражающего агента.
1. Козлов Ю.В., Сударкина О.Ю., Курманова А.Г. Рибосом-инактивирующие лектины растений Молекулярная биология. 2006; 40(4): 711-23.
2. Bolognesi A, Bortolotti M, Maiello S, Battelli MG, Polito L. Ribosome-Inactivating Proteins from Plants: A Historical Overview. Molecules. 2016; 21(12). pii: E1627.
3. Bozza W.P., Tolleson W.H., Rivera Rosado L.A., Zhang B. Ricin detection: tracking active toxin. Biotechnol Adv. 2015; 33(1):117-123.
4. Синегубова Е.О., Дубровина И.А., Мясников В.А. Комплексный подход к оценке цитотоксичности рибосом-инактивирующих белков на клеточной модели in vitro. Медицина экстремальных ситуаций 2019; 21(S1): 53-62.
5. Endo Y, Tsurugi K. RNA N-glycosidase activity of ricin A-chain. Mechanism of action of the toxic lectin ricin on eukaryotic ribosomes. J Biol Chem 1987; 262:8128–30.
6. Дубровский Я.А., Подольская Е.П. Определение токсинов пептидной природы методом MALDI-MS. Научное приборостроение. 2010; 20(4): 21-35.
7. Браун А.В., Таранченко В.Ф., Тихомиров Л.А., Гречухин А.П., Рыбальченко И.В. Обнаружение рицина в растительных экстрактах и почве с использованием жидкостной хромато-масс-спектрометрии высокого разрешения. Журнал аналитической химии. 2018; 73(8): 622-631.
8. Бабаков В.Н., Роговская Н.Ю., Курдюков И.Д., Бельтюков П.П., Дулов С.А., Радилов А.С. Влияние агонистов арилгидрокарбонового рецептора и липополисахарида на маркеры генотоксического действия бенз(а) пирена Токсикологический вестник 2019; (3):19-25.
9. Дубровский Я.А., Горбунов А.Ю., Роговская Н.Ю., Мурашко Е.А., Бельтюков П.П., Бабаков В.Н. Протеомный подход по определению биотоксинов в объектах окружающей среды. В сб.: Медико-биологические аспекты химической безопасности. Под общей редакцией А.С. Радилова, В.Р. Рембовского. 2018. С. 25-26.
10. Griffiths G.D., Leek M.D., Gee D.J. The toxic plant proteins ricin and abrin induce apoptotic changes in mammalian lymphoid tissues and intestine. J Pathol. 1987;151(3):221-9.
11. Saxena N., Yadav P., Kumar O. The Fas/ Fas ligand apoptotic pathway is involved in abrin-induced apoptosis. Toxicol Sci. 2013;135(1):103-18.
12. Fodstad O., Olsnes S., Pihl A. Toxicity, distribution and elimination of the cancer ostatic lectins abrin and ricin after parenteral injection into mice. Br J Cancer. 1976;34(4):418-25.
13. Ramsden C.S., Drayson M.T., Bell E.B. The toxicity, distribution and excretion of ricin holotoxin in rats. Toxicology. 1989;55(1-2):161-71.
14. Authier F., Djavaheri-Mergny M., Lorin S., Frénoy J.P., Desbuquois B. Fate and action of ricin in rat liver in vivo: translocation of endocytosed ricin into cytosol and induction of intrinsic apoptosis by ricin B-chain. Cell Microbiol. 2016;18(12):1800-1814








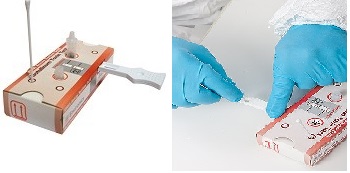
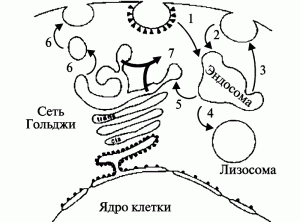 Рис. 1. Механизм токсического действия рицина. После взаимодействия В-субъединицы рицина с галактозой или N-ацетилгалактозамином на поверхности клетки, молекула токсина подвергается эндоцитозу (1, 2). Большинство молекул рицина выводится обратно на поверхность клетки благодаря механизму экзоцитоза (3). Если везикулы сливаются с лизосомами, то рицин разрушается благодаря механизму протеолиза (4). Часть рицин-содержащих везикул сливается с транспортной сетью Гольджи (trans-Golgi network, TGN) (5), оттуда они также могут быть выведены на поверхность клетки (6). Токсическое действие рицин оказывает тогда, когда его молекула распадается на субъединицы и А-субъединица пенетрирует мембрану TGN и проникает в цитозоль (7) где катализирует депуринизацию (depurination) рибосом, останавливая синтез белка. По [1]
Рис. 1. Механизм токсического действия рицина. После взаимодействия В-субъединицы рицина с галактозой или N-ацетилгалактозамином на поверхности клетки, молекула токсина подвергается эндоцитозу (1, 2). Большинство молекул рицина выводится обратно на поверхность клетки благодаря механизму экзоцитоза (3). Если везикулы сливаются с лизосомами, то рицин разрушается благодаря механизму протеолиза (4). Часть рицин-содержащих везикул сливается с транспортной сетью Гольджи (trans-Golgi network, TGN) (5), оттуда они также могут быть выведены на поверхность клетки (6). Токсическое действие рицин оказывает тогда, когда его молекула распадается на субъединицы и А-субъединица пенетрирует мембрану TGN и проникает в цитозоль (7) где катализирует депуринизацию (depurination) рибосом, останавливая синтез белка. По [1]