Арены (ароматические углеводороды) – это непредельные (ненасыщенные) циклические углеводороды, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей.
Общая формула: CnH2n–6 при n ≥ 6.
Строение, номенклатура и изомерия ароматических углеводородов
Способы получения ароматических углеводородов
Химические свойства ароматических углеводородов
Строение аренов
Рассмотрим подробно строение молекулы бензола. В ней присутствуют три двойные связи С=С, три одинарные связи С–C и шесть одинарных связей С–Н.
Структурная формула бензола:
Сокращенная структурная формула бензола:
Каждый из шести атомов углерода в молекуле бензола находится в состоянии sp2-гибридизации.
Каждый атом углерода в молекуле бензола связан с двумя соседними атомами углерода и атомом водорода тремя σ-связями. Валентные углы равны 1200:
Атомы углерода и водорода в молекуле бензола, соединенные σ-связями, образуют правильный шестиугольник, в котором все атомы углерода и все σ-связи С–С и С–Н лежат в одной плоскости.
Негибридные р-орбитали атомов углерода образуют единую циклическую (ароматическую) π-систему – единое электронное облако над и под плоскостью кольца.
Соответственно, на самом деле все связи между атомами углерода в молекуле бензола одинаковой длины (0,140 нм), что соответствует промежуточному значению между одинарной и двойной (полуторная связь).
Соответственно, в молекуле бензола между углеродными атомами нет обычных одинарных и двойных связей, а все они выравнены (делокализованы).
Поэтому структурную формулу бензола изображают в виде правильного шестиугольника и кружка внутри него, который обозначает делокализованные π-связи:
Гомологический ряд аренов
Простейший представитель гомологического ряда аренов — бензол:
Ближайший гомолог бензола – толуол (метилбензол):
Еще один представитель гомологического ряда бензола – этилбензол:
Изопропилбензол (кумол):
Номенклатура аренов
Первый представитель гомологического ряда аренов — бензол:
Ближайший гомолог бензола – толуол (метилбензол):
При составлении названия ароматического соединения за главную цепь принимают молекулу бензола. Если в ароматическом кольце несколько заместителей, то атомы углерода бензольного кольца нумеруются: в направлении, где больше заместителей, от самого главного заместителя (чем больше атомов углерода в радикале, тем он старше).
Например, 1,2-диметилбензол
Если в молекуле бензола присутствуют два заместителя, то также используют систему специальных приставок:
- орто— (о-) если заместители расположены у соседних атомов углерода в бензольном кольце (1,2-положения);
- мета— (м-) заместители расположены через один атом углерода (1,3-положения);
- пара— (п-) заместители расположены на противоположных сторонах кольца (1,4-положения).
Для названия многих производных бензола используют тривиальные названия:
| Структурная формула | Системное название | Тривиальное название |
 |
Метилбензол | Толуол |
 |
1,2-Диметилбензол | орто-Ксилол |
 |
Изопропилбензол | Кумол |
Названия радикалов, содержащих ароматическое кольцо:
Изомерия аренов
Структурная изомерия
Для гомологов бензола характерна структурная изомерия .
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
- Изомерия углеродного скелета в боковой цепи характерна для ароматических углеводородов, которые содержат три и более атомов углерода в боковой цепи.
Формуле С9Н12 соответствуют изомеру изопропилбензол и пропилбензол
- Изомерия положения заместителей характерна для аренов, которые содержат два и более заместителей в бензольном кольце.
Арены — ароматические углеводороды, содержащие одно или несколько бензольных колец.
Бензольное кольцо составляют 6 атомов углерода, между которыми чередуются двойные и одинарные связи.
Важно заметить, что двойные связи в молекуле бензола не фиксированы, а постоянно перемещаются по кругу.
Арены также называют ароматическими углеводородами. Первый член гомологического ряда — бензол — C6H6.
Общая формула их гомологического ряда — CnH2n-6.
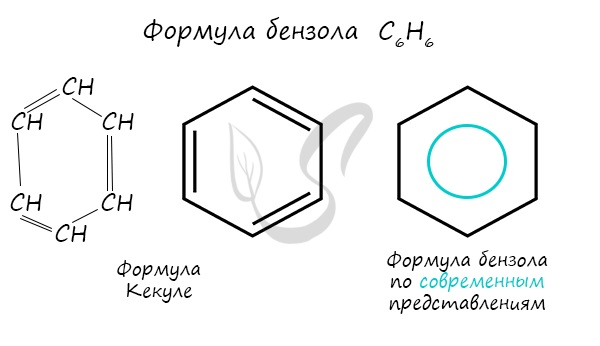
Долгое время структурная формула бензола оставалась тайной. Предложенная Кекуле формула с тремя двойными связями не могла
объяснить то, что бензол не вступает в реакции присоединения. Как уже было сказано выше, по современным представлениям
двойные связи в молекуле бензола постоянно перемещаются, поэтому более верно рисовать их в виде кольца.
За счет чередования двойных связей в молекуле бензола формируется сопряжение. Все атомы углерода находятся в состоянии sp2
гибридизации. Валентный угол — 120°.
Номенклатура и изомерия аренов
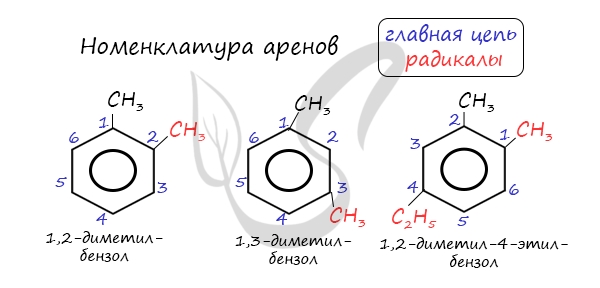
Названия аренов формируются путем добавления названий заместителей к главной цепи — бензольному кольцу: бензол, метилбензол (толуол),
этилбензол, пропилбензол и т.д. Заместители, как обычно, перечисляются в алфавитном порядке. Если в бензольном кольце несколько заместителей,
то выбирают кратчайший путь между ними.
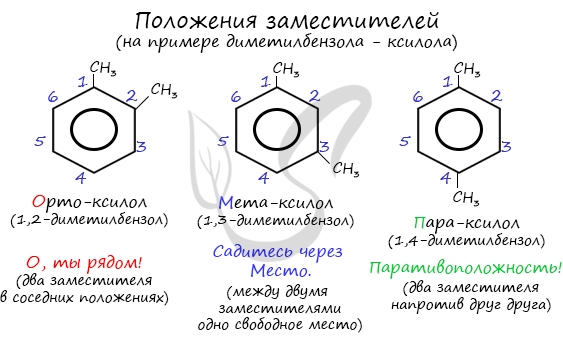
Для аренов характерна структурная изомерия, связанная с положением заместителей. Например, два заместителя в бензольном
кольце могут располагаться в разных положениях.
Название положения заместителей в бензольном кольце формируется на основе их расположения относительно друг друга. Оно обозначается
приставками орто-, мета- и пара. Ниже вы найдете мнемонические подсказки для их успешного запоминания 
Получение аренов
Арены получают несколькими способами:
- Реакция Зелинского (тримеризация ацетилена)
- Дегидроциклизация алканов
- Дегидрирование циклоалканов
- Синтез Дюма
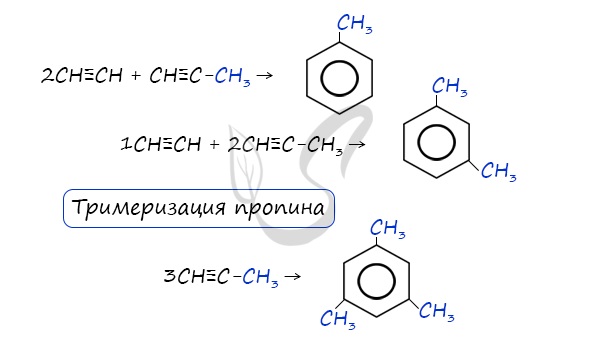
Данная реакция протекает при пропускании ацетилена над активированным углем при t = 400°C. В результате образуется ароматический
углеводород — бензол.

В случае, если к ацетилену добавить пропин, то становится возможным получение толуола. Увеличивая долю пропина, в конечном итоге
можно добиться образования 1,3,5-триметилбензола.
В ходе таких реакций, протекающих при повышенной температуре и в присутствии катализатора — Cr2O3, линейная
структура алкана замыкается в цикл, отщепляется водород.
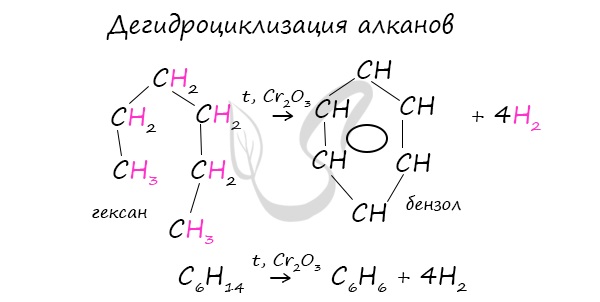
При дегидроциклизации гептана получается толуол.
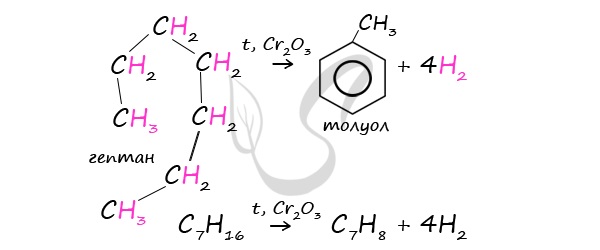
В результате дегидрирования уже «готовых» циклов — циклоалканов, отщепляются 3 моль водорода, и образуется соответствующий арен,
с теми же заместителями, которые были у циклоалкана.

Синтез Дюма заключается в сплавлении солей карбоновых кислот с щелочами. В результате такой реакции возможно образование различных органических веществ, в том числе аренов.
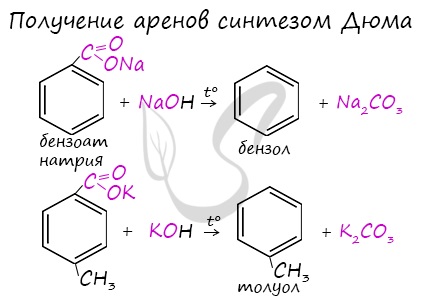
Химические свойства аренов
Арены — ароматические углеводороды, которые содержат бензольное кольцо с сопряженными двойными связями. Эта особенность
делает реакции присоединения тяжело протекающими (и тем не менее возможными!)
Запомните, что, в отличие от других непредельных соединений, бензол и его гомологи не обесцвечивают бромную воду и
раствор перманганата калия.
- Гидрирование
- Галогенирование
- Нитрование
- Алкилирование
- Окисление
- Полимеризация
При повышенной температуре и наличии катализатора, водород способен разорвать двойные связи в бензольном кольце
и превратить арен в циклоалкан.

Реакция бензола с хлором на свету приводит к образованию гексахлорциклогексана, если же использовать только катализатор,
то образуется хлорбензол.
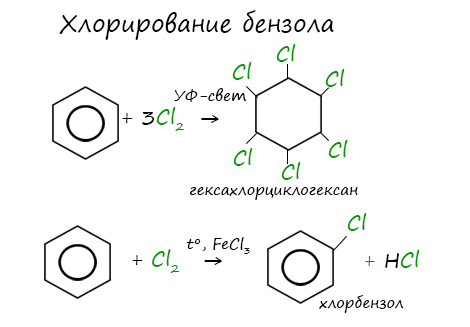
Реакции с толуолом протекают иначе: при УФ-свете хлор направляется в радикал метил и замещает атом водорода в нем, при действии катализатора хлор замещает один атом водорода в бензольном кольце (в орто- или пара-положении).
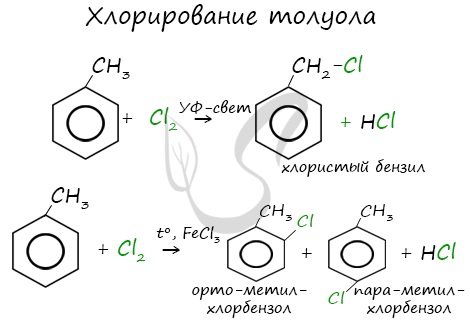
Почему хлор направляется именно в орто- и пара-положения относительно метильной группы? Здесь самое время
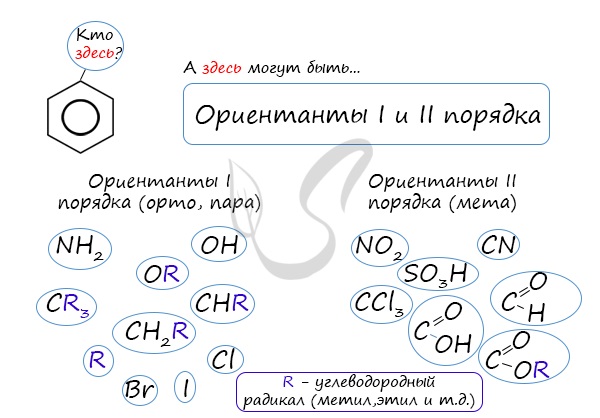
коснуться темы ориентантов I (орто-, пара-ориентантов) и II порядков (мета-ориентанты).
К ориентантам первого порядка относятся группы: NH2, OH, OR, CR3, CHR2,
CH2R, галогены. К ориентантам второго: NO2, CN, SO3H, CCl3,
CHO, COOH, COOR.
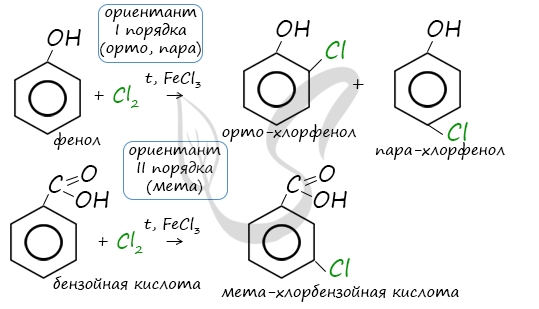
Например, ориентант I порядка, гидроксогруппа OH, обеспечивает протекание хлорирования в орто- и пара-положениях.
А карбоксильная группа COOH, ориентант II порядка, обуславливает хлорирование в мета-положениях.
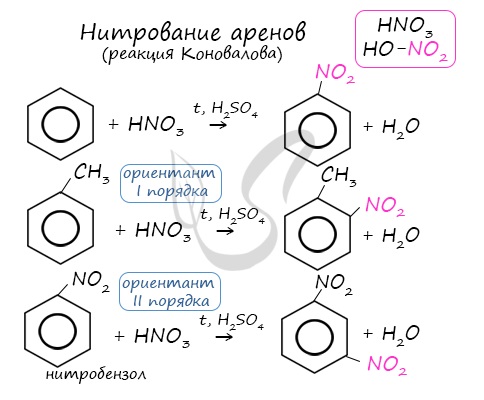
Арены вступают в реакции нитрования, протекающие при повышенной температуре и в присутствии серной кислоты,
обладающей водоотнимающими свойствами.
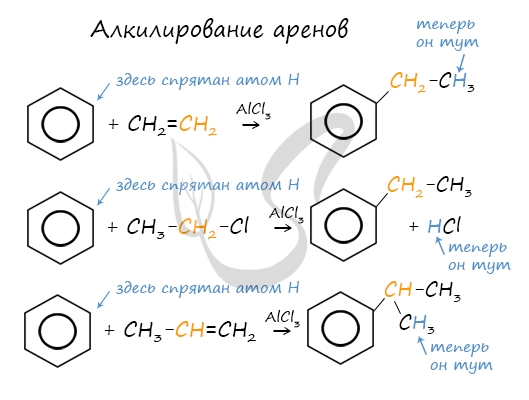
Алкилирование аренов осуществляется путем введения алкильного радикала в молекулу бензола. Алкильным радикалом чаще
всего выступает алкен или галогеналкан. В подобных реакциях используют катализатор AlCl3.
В случае если для алкилирования используется алкен, то с молекулой бензола соединяется наименее гидрированный атом
углерода алкена, прилежащий к двойной связи. Один атом водорода переходит из бензольного кольца к радикалу.
Арены, как и все органические вещества, сгорают с образованием углекислого газа и воды.
2C6H6 + 15O2 → 12CO2 + 6H2O
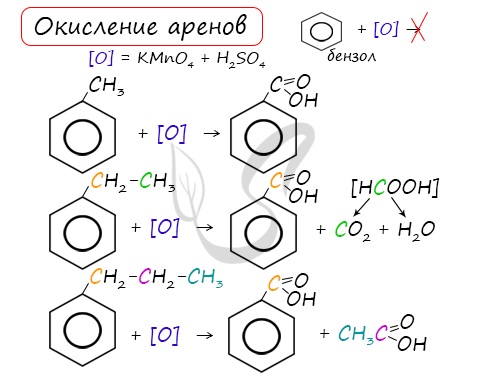
При неполном окислении гомологи бензола способны окисляться до бензойной кислоты (при подкислении раствора серной
кислотой). Сам бензол не вступает в реакцию окисления с KMnO4, не обесцвечивает его раствор.
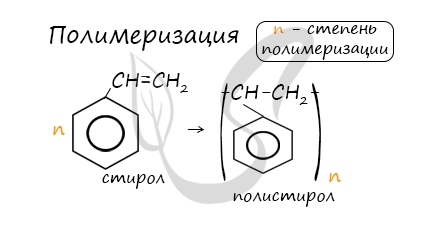
В реакцию полимеризации способен вступать стирол (винилбензол), в радикале которого содержится двойная связь.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Ароматические углеводороды рассматриваются как производные бензола, в молекуле которого атомы водорода замещены на радикалы. Если таких радикалов несколько, то атомы углерода бензольного кольца нумеруются так, чтобы сумма цифр в названии была наименьшей. Начинают нумерацию от старшего заместителя к младшему.
Используются также рациональные названия: толуол (метилбензол), ортоксилол ((1),(2)-диметилбензол), метаксилол ((1),(3)-диметилбензол), параксилол ((1),(4)-диметилбензол), кумол (изопропилбензол) и др.
В таблице показаны примеры нумерации атомов углерода в бензольном кольце и приведены названия веществ.
|
Структурная формула арена |
Название |
|
|
(1),(3)-диметилбензол (метаксилол) |
|
|
(1)-метил-(2)-этилбензол |
Гомологам бензола характерна структурная изомерия, которая может быть обусловлена:
- разным расположением углеводородных радикалов в бензольном кольце;
- разным строением боковых углеводородных радикалов.
Структурная изомерия в гомологическом ряду бензола возможна при числе атомов углерода не меньше (8). Бензол и метилбензол изомеров не имеют.
В таблице приведены формулы и названия некоторых изомеров, имеющих состав
C9H12
.
|
Структурная формула изомера |
Название |
|
|
пропилбензол |
|
|
изопропилбензол (кумол) |
|
|
(1)-метил-(2)-этилбензол |
|
|
(1)-метил-(3)-этилбензол |
|
|
(1),(2),(3)-триметилбензол |
|
|
(1),(2),(4)-триметилбензол |
План урока:
Определение и формула аренов
Строение молекулы бензола
Изомерия и номенклатура аренов
Методы получения аренов
Физические свойства ароматических соединений
Химические реакции ароматических углеводородов
Области применения аренов
Определение и формула аренов
Арены (ароматические углеводороды) – соединения, включающие устойчивый цикл из шести атомов углерода (бензольное кольцо). Важнейший представитель – бензол.
Общая формула ароматических углеводородов: CnH2n-6
Молекула бензола.
Строение молекулы бензола
Бензол – первый представитель гомологического ряда ароматических углеводородов, открытый в 1825 году Майклом Фарадеем. Т.к. его молекулярная формула – С6Н6, значит, в основе лежат двойные связи. Поэтому было предположено, что бензолу свойственна ненасыщенность. В 1865 году Фридрих Кекуле предположил структурную формулу бензола.
Но в экспериментах было доказано, что бензол входит в реакции присоединения только в жестких условиях и устойчив к реакциям окисления. Для него наиболее свойственно замещение, что доказывает принадлежность к предельным соединениям.
Парадоксальное электронное строение было доказано с помощью получения бензола из ацетилена. Его особенность заключается в том, что все атомы в кольце равноценны и имеют характер одинарных и кратных связей. Это можно отразить формулой с равномерным распределением электронной плотности.
Углеродные атомы в кольце имеют по четыре валентных электрона и им свойственна sp2-гибридизация. Атомы располагаются в единой плоскости. Особенности строения бензола состоят в том, что электроны составляют единую π-систему и все связи равноценны. Т.е. формула Кекуле неточна, т.к. отражает наличие двойных связей. Бензольное кольцо – это циклическая сопряженная система, связи которой перекрываются между собой.
Пространственное строение бензола Источник
Изомерия и номенклатура аренов
Для бензола и его гомологов характерна только структурная изомерия, которая включает:
- изомерию углеродного скелета боковой цепи,
- изомерию положения заместителей в кольце.
Источник
Главной цепью в названии аренов принимается ароматическое кольцо, от которого отходят заместители. В следующем представителе гомологического ряда ксилоле (диметилбензоле) имеет значение положение заместителей в кольце. Для его обозначения используются различные приставки:
- орто- (о-) – заместители находятся у соседних углеродных атомов в кольце,
- мета- (м-) – заместители находятся через один атом,
- пара- (п-) – заместители находятся через два атома.
Методы получения аренов
В промышленности бензол и его гомологи можно получить несколькими способами.
- Из каменноугольной смолы.
- Дегидрирование и циклизация алканов при катализаторе и под действием высоких температур.
- Дегидрирование циклоалканов при катализаторе и под действием высоких температур
В лаборатории моноциклические соединения также получают несколькими путями.
- Циклотримеризация ацетилена и его гомологов при катализаторе и под действием высоких температур (реакция получения бензола)
- Реакция Вюрца-Фиттига – взаимодействие галогеналканов и арилгалогенидов с металлическим натрием
- Алкилирование галогеналканами, алкенами и спиртами в присутствии кислот Льюиса
Физические свойства ароматических соединений
Бензол и его ближайшие гомологи – бесцветные жидкости с характерным запахом. Нерастворимы в воде, но растворимы в органических растворителях. Их плотность меньше плотности воды. Они огнеопасны и токсичны для животных и человека.
Химические реакции ароматических углеводородов
Несмотря на то, что бензол включает систему из сопряженных кратных связей, аренам не характерны реакции обесцвечивания бромной воды и перманганата калия.
Реакции присоединения
Бензолу характерны реакции присоединения, образуя циклогексан или его производные.
Реакции замещения
Аренам характерны реакции замещения.
Окисление аренов
При неполной химической реакции окисления гомологи бензола образуется бензойная кислота. Самому бензолу реакции окисления перманганатом калия не характерны.
Полимеризация аренов
В реакции полимеризации способен вступать стирол, образуя полистирол.
Области применения аренов
Без бензола и его гомологов невозможно представить современное промышленное производство. Основные области применения бензола – производство этилбензола, кумола и циклогексана и анилина.

– самая высокая по энергии, она имеет три узло— вые плоскости.
Поскольку все атомы углерода в молекуле бензола находятся в sp2—гибридном состоянии, уг— лы между связями в бензоле 120о. Длина полутор—
ной ароматической π-связи С 
ным подтверждением sp2—гибридного состояния атомов углерода в бензоле.
Примерами ароматических π-систем с 10 и 14 π-электронами являются пред— ставители многоядерных ароматических соединений:
|
нафталин |
и антрацен |
, которые относятся к аро— |
||||||
матическим углеводородам с конденсированными кольцами. Кроме того, суще— ствуют би— и полициклические арены с неконденсированными кольцами, про—
стейшим представителем которых является дифенил
1.Структурная изомерия гомологов бензола обусловлена взаимным рас—
положением заместителей в бензольном кольце. Положение двух заместителей указывают с помощью приставок: орто— (о-), если они находятся у соседних углеродных атомов (положение 1, 2-), мета— (м-) для разделенных одним ато— мом углерода (1, 3-) и пара— (п-) для находящихся напротив друг друга (1, 4-). Например, для диметилбензола (ксилола) можно записать три изомера:
|
орто—ксилол |
мета—ксилол |
пара—ксилол |
|
(1,2-диметилбензол) |
(1,3-диметилбензол) |
(1,4-диметилбензол) |
36

2.Межклассовая изомерия предполагает существование нескольких го— мологических рядов с общей брутто—формулой СnH2n-6. Это нециклические уг— леводороды с четырьмя двойными связями (тетраены), бициклоалкены, цик— лотриены и другие.
3.Гомологи бензола не проявляют способность к цис-транс- изомерии, оптическая изомерия обусловлена наличием заместителей с хиральными цен— трами.
Для построения названия углеводорода ряда бензола используют сле— дующие правила номенклатуры. Если в бензольном кольце находится один за— меститель несложного строения, то называют его, прибавляя к его названию слово «бензол».
Если заместителей два, используют приставки орто-, мета-, пара-, как было показано выше. Если в бензольном кольце несколько заместителей, то пе—
речисляют их названия с указанием номеров углеродных атомов в молекуле бензола, а в конце добавляют корень «бензол». При этом сумма цифр, указыва—
СН3
метилбензол (тривиальное название – толуол)

CH3
2,3-дифенилбутан
|
ющая положение замес— |
|||||||||||||
|
тителей, |
должна |
быть |
|||||||||||
|
наименьшей из всех воз— |
|||||||||||||
|
можных |
вариантов |
ну— |
|||||||||||
|
1,3-диметил-4-этилбензол |
мерации положений бен— |
||||||||||||
|
C |
C |
CH2 |
CH3 |
зольного кольца. |
При |
||||||||
|
наличии в бензольном |
|||||||||||||
|
кольце |
сложного |
за— |
|||||||||||
|
СН3 |
|||||||||||||
|
1-(м—толил)-1-бутин |
местителя, его называ— |
||||||||||||
ют по правилам номенклатуры ИЮПАК, считая ароматические остатки замес— тителями, которые имеют соответствующие названия. Названия арильных за— местителей образуют с помощью суффикса –ил:
37

|
м—толил |
п—толил |
2-этилфенил |
Двухвалентные остатки называют добавлением суффикса –илен, например, о—фенилен, м— фенилен и п—фенилен.
Пояснения по выполнению контрольной работы
1.В ответе на 1 вопрос рассматривается только соединение, отмеченное в задании *. Записывают его полную структурную формулу, относят соединение
ккакому—либо гомологическому ряду, определяют форму углеродного скелета, отмечают типы атомов углерода (только для атомов углерода в sp3—гибридном состоянии!).
2.Указать гомологический ряд, брутто—формулу, общую брутто— формулу, первый член гомологического ряда, к которому относится соедине— ние, отмеченное в задании *. Указать другие гомологические ряды (с такой же брутто—формулой, как у соединения, отмеченного в задании *).
3.Выделить, записать и назвать заместители – фрагменты молекулы со— единения, отмеченного в задании * (см. стр. 15).
4.Записать изомеры соединения, отмеченного в задании *. 3 изомера из того же гомологического ряда, по 3 – из других гомологических рядов, назван— ных в задании 2. Все записанные соединения необходимо назвать по номенкла— туре ИЮПАК.
5.Записать полную структурную формулу, отметить на ней гибридное со— стояние всех атомов углерода, величины углов между связями в молекуле. Изо—
бразить схему перекрывания атомных орбиталей при образовании σ-связей, на— пример, для молекул бензола и этана можно представить следующие рисунки:
38

6. Изобразить аналогичную схему перекрывания атомных орбиталей при образовании π-связей, например для молекул бензола и 1,3-бутадиена:
Выделить систему сопряжения, ароматическую π-систему.
7.Запишите для соединения, отмеченного в задании *, цис— и транс— изо— меры и оптические изомеры (если это возможно). Если это соединение не мо— жет проявлять цис—транс— и оптическую изомерию, выберите один из его структурных изомеров, записанных вами в пункте 4 и проделайте это задание с ним.
8.Запишите молекулу алкана, которая имеет тот же углеродный скелет,
что и молекула отмеченного в задании * соединения. Выделите одну из σ- связей, вокруг которой возможно вращение атомных групп относительно друг друга. Изобразите проекционные формулы Ньюмена заслоненной, заторможен— ной и скошенной конформации этого алкана. Расположите конформации в ряд по уменьшению их потенциальной энергии.
9. На основе углеродного скелета соединения, отмеченного в задании *, запишите структурную формулу алкилциклогексана, содержащего такое же число углеродных атомов, как и исходный углеводород. Например, на основе
CH3
структурной формулы соединения H3C CH CH2 (CH2)2 CH2 CH CH3 можно запи—
CH3
H3СH3С
сать H3С
«ванна» с указанием положения аксиальных и экваториальных атомов водорода.
39
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #





































