Radioactive decay is the release of alpha, beta, and gamma particles from unbalanced atoms known as radionuclides. Some substances, like uranium, have no stable forms and are therefore always radioactive. Radioactive substances are referred to as radionuclides. Rate of Decay is calculated to tell the exact amount of radioactive material that is being radiated. In this article, we will learn about the rate of decay formula and its examples in detail.
Half-Life of Radioactive Substances
A radionuclide decays into a different atom known as a decay product. Until the atoms achieve a stable state and stop being radioactive, they continue to change into new decay products. Most radionuclides only undergo one decay before stabilizing. Series radionuclides are those that decay in more than one step. The decay chain is the collection of decay products produced to achieve this equilibrium.
Each radionuclide has a unique decay rate that is measured by its “half-life.” The amount of time it takes for half of the radioactive atoms present to decay is known as the radioactive half-life. Others have half-lives of hundreds, millions, or billions of years. Some radionuclides have half-lives of just a few seconds.
The time it takes for the activity of a specific quantity of a radioactive substance to decay to half of its initial value is known as the half-life (t1/2).
t1/2 = ln(2) / λ = τ ln(2)
where,
t1/2 is the half-life of a radioactive substance.
λ is the mean lifetime of a radioactive substance.
τ is the average lifetime of a radioactive substance before decay.
Rate of Decay Formula
The breakdown of radioactive particles into new types of particles from the parent radionuclide is known as radioactive decay. There are three types of radioactive decay, alpha, beta, and gamma decay, and the half-lives of each type of decay have different values depending on the type of ionization. Due to the emission of many particle kinds, the decay rate differs for each type of decay.
It’s been observed that radioactive disintegration only happens when the nucleus is unstable. Alpha, beta, and gamma radiations are released by the unstable nucleus along with other ionizing particles and radiations as it loses energy. A radioactive element is one that has a nucleus that is unstable. Usually, the radioactive substance splits into two parts.
The term “Parent nuclide” denotes to one component of a radioactive element. The other component disintegrates into a “Daughter nuclide,” a modified atom that differs from the parent radionuclide as a result of the bombardment. The decay product is another name for the daughter nuclide. This is due to the fact that the parent nuclide’s atoms continue to decay and transform into new decay products. The decay product stops decaying when it reaches a stable state where its radioactivity disappears.
A first-order decay process determines the rate of radioactive particle decay. This indicates that it exhibits an exponential decline pattern, which is simple to calculate.
Nt = N0 e-λt
where,
Nt is the amount of radioactive particles at time (t)
N0 is the amount of radioactive particles at time (0)
λ is the rate of decay constant
t is time
Since this decay rate is exponential, taking the natural log on both sides of the equation will result in:
ln (Nt /N0) = -λt
Read, More
- Radioactivity
- Types of Radioactivity
- Radioactive Isotopes
Solved Examples on Rate of Decay Formula
Example 1: If U-238 has a half-life of 4.468 × 109 years, determine its rate of decay constant.
Solution:
The problem refers to half life of U-238, Half of the original sample has already decayed. Hence the ratio N0/Nt = 0.5.
ln (Nt /N0) = -λt
ln 0.5 = -λ × 4.468 × 109
λ = 1.55 x 10-10 years-1
Rate of decay constant (λ) is 8.38 x 10-11 years-1
Example 2: If U-238 has a 35% life of 5.142 × 109 years, determine its rate of decay constant.
Solution:
35% half life of U-238 has already decayed, Hence the ratio N0/Nt = 0.65 as 65 percent of original sample remains.
ln (Nt /N0) = -λt
ln 0.65 = -λ × 5.142 × 109
λ = 0.838 x 10-10 years-1
Rate of decay constant (λ) is 8.38 x 10-11 years-1
Example 3: Determine the amount of time it will take for 25% of a sample of U-238 to radioactively decay with a decay constant of 1.55 x 10-10 years-1.
Solution:
Since 75% of the original sample is still present, the ratio Nt/N0 = 0.75. Where 25% of the sample has undergone radioactive decay.
Rate of decay constant (λ) = 1.55 × 10-10 years-1
ln (Nt /N0) = -λt
ln 0.75 = -1.55 × 10-10 years-1 × t
t = 1.86 x 109 years
The amount of time for 25% radioactive U-238 decay is 1.86 x 109 years
Example 4: Determine the amount of time it will take for 45% of a sample of U-238 to radioactively decay with a decay constant of 1.55 x 10-10 years-1.
Solution:
Since 55% of the original sample is still present, the ratio Nt/N0 = 0.75. Where 45% of the sample has undergone radioactive decay.
Rate of decay constant (λ) = 1.55 × 10-10 years-1
ln (Nt /N0) = -λt
ln 0.55 = -1.55 × 10-10 years-1 × t
t = 3.86 x 109 years
The amount of time for 45% radioactive U-238 decay is 3.86 x 109 years
Example 5: The half-life of PD-100 is 3.6 days. How many atoms will remain after 20.0 days, if one has 6.02 x 1023 at the beginning?
Solution:
Time = 20 days
Half-life = 3.6 days
Initial atoms = 6.02 ×1023 atoms
Formula used to determine number of atoms after 20 days.
N = N0 × 1/2 × t/t1/2
N = 6.02 ×1023 × 1/2 × 20/3.6
= 1.28 × 1022
The number of atoms present is 1.28 × 1022
FAQs on Rate of Decay
Question 1: What is radioactive decay?
Answer:
The radioactive atom (radionuclide) changes into another nuclide as the nucleus releases radiation or breaks down. It is known as radioactive decay.
Question 2: What are the different types of radioactive decay?
Answer:
Alpha, beta, and gamma decay are the three main types of radioactive decay. The number of protons in an atom’s nucleus can change by alpha and beta decay, which transforms the atom into a different element. The atom does not convert into a different element due to gamma decay because it does not alter the proton number.
Question 3: What are examples of radioactive decay?
Answer:
Alpha decay, proton emission, double proton emission, beta decay, gamma decay, electron capture, and neutron emission are common examples of radioactive decay.
Question 4: What is the importance of radioactive decay?
Answer:
Radioactive decay is useful for many aspects of human life, including health, the creation of electricity, and astronomy, etc.
Question 5: What are the effects of radioactive decay on humans?
Answer:
The energy released into the environment as radioactive material decays or breaks down can injure a body in two different ways. It has the potential to directly destroy cells or to alter DNA. The cell may develop cancer if certain mutations are not fixed.
Question 6: What is the importance of radioactive half-life?
Answer:
Because long-lived radionuclides persist longer after release than shorter-lived species, the radiological half-life is essential for radiation control. Radionuclides with longer half-lives will remain in the environment longer than those with shorter half-lives.
Last Updated :
17 Apr, 2023
Like Article
Save Article
Кроме колебаний в природе часто встречается еще одна зависимость величины от времени — экспоненциальное уменьшение:
Здесь n(t) — это изменяющаяся со временем величина, n0 — ее начальное значение, а τ — это время жизни, параметр, характеризующий то, как быстро происходит уменьшение. Вторая формула выражает то же самое, что и первая, просто она записана иным способом, через степени двойки. Параметр T1/2 называется периодом полураспада и связан с временем жизни формулой T1/2 = τ·ln2 ≈ 0,7τ.
Экспоненциальная зависимость от времени встречается в самых разных ситуациях. Стандартный пример — это радиоактивность; собственно, эта формула обычно и называется законом радиоактивного распада. Эта формула относится к количеству радиоактивных ядер или нестабильных элементарных частиц и описывает их постепенное уменьшение с течением времени за счет распада.
Этот закон описывает также самые разные процессы затухания. Выведенная из равновесия система, как правило, самопроизвольно возвращается к первоначальному состоянию, и протекает этот процесс примерно по этому экспоненциальному закону. Величина n(t) в этом случае показывает величину отклонения от равновесия, а параметр τ называется временем затухания. Например, если горячий предмет положить на холодную поверхность, тепло начнет перетекать, стремясь выровнять температуру тел. Сначала этот поток тепла большой, но потом замедляется: чем ближе система к тепловому равновесию, тем меньше остаточный поток тепла. Если в какой-то точке тела у нас установлен тепловой датчик, то его показания будут постепенно приближаться к установившейся температуре по экспоненциальному закону.
Появление «ручных» сцинтилляционных счетчиков и, главным образом, счётчиков Гейгера–Мюллера, которые помогли автоматизировать подсчёты частиц (см. § 15-е), привело физиков к важному выводу. Любой радиоактивный изотоп характеризуется самопроизвольным ослабеванием радиоактивности, выражающимся в уменьшении количества распадающихся ядер в единицу времени.
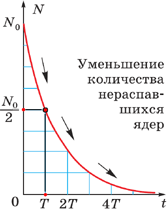
Построение графиков активности различных радиоактивных изотопов приводило учёных к одной и той же зависимости, выражающейся показательной функцией (см. график). По горизонтальной оси отложено время наблюдения, а по вертикальной – количество нераспавшихся ядер. Кривизна линий могла быть различной, однако сама функция, которой выражались описываемые графиками зависимости, оставалась одной и той же:
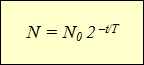 |
N – количество нераспавшихся ядер N0 – начальное количество ядер t – время наблюдения, с T – период полураспада, с |
Эта формула выражает закон радиоактивного распада: количество нераспавшихся с течением времени ядер определяется как произведение начального количества ядер на 2 в степени, равной отношению времени наблюдения к периоду полураспада, взятой с отрицательным знаком.
Как выяснилось в ходе опытов, различные радиоактивные вещества можно охарактеризовать различным периодом полураспада – временем, за которое количество ещё нераспавшихся ядер уменьшается вдвое (см. таблицу).
| Йод-129 | 15 млн лет | Углерод-14 | 5,7 тыс лет | |
| Йод-131 | 8 дней | Уран-235 | 0,7 млрд лет | |
| Йод-135 | 7 часов | Уран-238 | 4,5 млрд лет |
Период полураспада – общепринятая физическая величина, характеризующая скорость радиоактивного распада. Многочисленные опыты показывают, что даже при очень длительном наблюдении за радиоактивным веществом его период полураспада постоянен, то есть не зависит от числа уже распавшихся атомов. Поэтому закон радиоактивного распада нашёл применение в методе определения возраста археологических и геологических находок.
Метод радиоуглеродного анализа. Углерод – очень распространённый на Земле химический элемент, в состав которого входят стабильные изотопы углерод-12, углерод-13 и радиоактивный изотоп углерод-14, период полураспада которого составляет 5,7 тысяч лет (см. таблицу). Живые организмы, потребляя пищу, накапливают в своих тканях все три изотопа. После прекращения жизни организма поступление углерода прекращается, и с течением времени его содержание убывает естественным путём, за счёт радиоактивного распада. Поскольку распадается только углерод-14, с течением веков и тысячелетий изменяется соотношение изотопов углерода в ископаемых останках живых организмов. Измерив эту «углеродную пропорцию», можно судить о возрасте археологической находки.
Метод радиоуглеродного анализа применим и для геологических пород, а также для ископаемых предметов быта человека, но при условии, что соотношение изотопов в образце не было нарушено за время его существования, например, пожаром или действием сильного источника радиации. Неучёт подобных причин сразу после открытия этого метода приводил к ошибкам на несколько веков и тысячелетий. Сегодня применяются «вековые калибровочные шкалы» для изотопа углерода-14, исходя из его распределения в долгоживущих деревьях (например, в американской тысячелетней секвойе). Их возраст можно подсчитать весьма точно – по годовым кольцам древесины.
Предел применения метода радиоуглеродного анализа в начале XXI века составлял 60 000 лет. Для измерения возраста более древних образцов, например горных пород или метеоритов, используют аналогичный метод, но вместо углерода наблюдают за изотопами урана или других элементов в зависимости от происхождения исследуемого образца.
|
При всем разнообразии реакций самопроизвольного (спонтанного) распада ядер в этом процессе наблюдается общая закономерность, которую можно описать математически. Интересно, что зависимость количества распавшихся ядер от времени задается одной и той же функцией для различных ядер, участвующих в распаде. Перейдем к количественному описанию процессов радиоактивного распада. |
Большинство изотопов любого химического элемента превращается в более устойчивые изотопы путем радиоактивного распада. Каждый радиоактивный элемент распадается со своей, присущей только ему «скоростью». При этом для каждого радиоактивного ядра существует характерное время, называемое периодом полураспада , спустя которое в исходном состоянии остается половина имевшихся ядер. Таким образом, периодом полураспада
называется промежуток времени, за который распадается половина начального количества
радиоактивных ядер. Другая половина ядер превращается в более устойчивые изотопы посредством распада.
Отметим, что период полураспада не зависит от того, в каком состоянии находится вещество: твердом, жидком или газообразном. Кроме того, период полураспада радиоактивного вещества не зависит от его количества, от времени, места и условий, в которых оно находится. Поэтому количество радиоактивных ядер «тогда» и «сейчас»
непосредственно определяет промежуток времени
, прошедший с момента уменьшения числа ядер от
до
.
Невозможно точно предсказать, когда произойдет распад данного ядра. Однако можно оценить среднее число ядер, которые распадутся за данный промежуток времени. Таким образом, закон радиоактивного распада является статистическим и он справедлив только при достаточно большом количестве радиоактивных ядер.
Для записи закона радиоактивного распада будем считать, что в начальный момент времени () число радиоактивных ядер
. Через промежуток времени, равный периоду полураспада, это число будет
, еще через такой же промежуток времени —
(рис. 218). Спустя промежуток времени, равный n периодам полураспада
, радиоактивных ядер останется:
|
|
(1) |
Это соотношение выражает закон радиоактивного распада, который можно сформулировать следующим образом:
число нераспавшихся радиоактивных ядер убывает с течением времени по закону, представленному соотношением (1).
Закон радиоактивного распада позволяет найти число нераспавшихся ядер в любой момент времени. Полученное выражение хорошо описывает распад радиоактивных ядер, если их количество достаточно велико.
Приведем экспериментальные результаты, которые показывают, что при малом количестве радиоактивных ядер это выражение неприменимо. На рисунке 219 изображен график распада 47 ядер изотопа фермия , период полураспада которого
. Из рисунка 219 видно, что пока ядер было достаточно много — от 47 до 12, то показательная функция хорошо описывала закон распада. Однако при меньшем числе ядер истинная зависимость существенно отличается от показательной функции.
Периоды полураспада некоторых радиоактивных изотопов веществ приведены в таблице 11.
| Таблица 11. Периоды полураспада радиоактивных изотопов веществ | |
| Вещество | Период полураспада |
| 30,17 лет | |
| 5,3 года | |
| 8,04 суток | |
| 24 390 лет | |
| 1600 лет | |
| 3,8 суток | |
| 700 млн лет | |
| 4,5 млрд лет |
|
Впервые процесс радиоактивного распада для измерения промежутков времени был использован в 1904 г. Резерфордом. По отношению концентрации урана и его дочернего продукта распада (гелия) он определил возраст урановой породы. Эта работа положила начало ядерной геохронологии — определению возраста различных минералов Земли по радиоактивным долгоживущим веществам. В дальнейшем исследование процессов ядерного синтеза позволило перейти к ядерной космохронологии, т.е. к определению продолжительных промежутков времени, прошедших с момента образования элементов в масштабах Галактики и Вселенной. В основу ядерной космохронологии положена неизменность «скорости» радиоактивного распада. В 1927 г. американский ученый Г. Блюмгарт, используя изотоп В 1934 г. венгерский ученый Дьердь фон Хевеши, используя дейтерий, впервые установил, что в организме человека вода полностью обновляется в течение 14 суток. В 1943 г. Дьердь фон Хевеши была присуждена Нобелевская премия по химии «за работу по использованию изотопов в качестве меченых атомов при изучении химических процессов». |
 |
Закон радиоактивного распада. Период полураспада
- Подробности
- Обновлено 20.07.2018 21:25
- Просмотров: 1196
«Физика — 11 класс»
Радиоактивный распад подчиняется статистическому закону.
Резерфорд, исследуя превращения радиоактивных веществ, установил опытным путем, что их активность убывает с течением времени.
Об этом говорилось в предыдущем параграфе.
Так, активность радона убывает в 2 раза уже через 1 мин.
Активность таких элементов, как уран, торий и радий, тоже убывает со временем, но гораздо медленнее.
Для каждого радиоактивного вещества существует определенный интервал времени, на протяжении которого активность убывает в 2 раза.
Этот интервал носит название период полураспада.
Период полураспада (Т) — это время, в течение которого распадается половина начального числа радиоактивных атомов.
Спад активности, т. е. числа распадов в секунду, в зависимости от времени для одного из радиоактивных препаратов изображен на рисунке.
Период полураспада этого вещества равен 5 сут.
Пусть число радиоактивных атомов в начальный момент времени (t = 0) равно N0.
Тогда по истечении периода полураспада это число будет равно
Спустя еще один такой же интервал времени это число станет равным:
По истечении времени t = nТ, т. е. спустя n периодов полураспада Т, радиоактивных атомов останется:
Поскольку
то
Это и есть основной закон радиоактивного распада.
По формуле можно найти число нераспавшихся ядер в любой момент времени.
Период полураспада — основная величина, определяющая скорость радиоактивного распада.
Чем меньше период полураспада, тем меньше времени «живут» ядра, тем быстрее происходит распад.
Для разных веществ период полураспада имеет сильно различающиеся значения.
Так, период полураспада урана 
Именно поэтому активность урана на протяжении нескольких лет заметно не меняется.
Период полураспада радия значительно меньше — он равен 1600 лет.
Поэтому активность радия значительно больше активности урана.
Есть радиоактивные элементы с периодом полураспада в миллионные доли секунды.
Чтобы определить период полураспада, надо знать число атомов N0 в начальный момент времени и число нераспавшихся атомов N спустя определенный интервал времени t.
Сам закон радиоактивного распада довольно прост.
Но физический смысл этого закона уяснить себе нелегко.
Действительно, согласно этому закону за любой интервал времени распадается одна и та же доля имеющихся атомов (за период полураспада половина атомов).
Значит, с течением времени скорость распада нисколько не меняется?
Радиоактивные ядра «не стареют»..
Так, ядра радона, возникающие при распаде радия, претерпевают радиоактивный распад как сразу же после своего образования, так и спустя 10 мин после этого.
Распад любого атомного ядра — это, так сказать, не «смерть от старости», а «несчастный случай» в его жизни.
Для радиоактивных ядер не существует понятия возраста.
Можно определить лишь их среднее время жизни τ.
Время существования отдельных ядер может варьироваться от долей секунды до миллиардов лет.
Атом урана, например, может спокойно пролежать в земле миллиарды лет и внезапно взорваться, тогда как его соседи благополучно продолжают оставаться в прежнем состоянии. Среднее время жизни τ — это просто среднее арифметическое времени жизни достаточно большого количества атомов данного вида.
Оно прямо пропорционально периоду полураспада.
Предсказать, когда произойдет распад ядра данного атома, невозможно.
Смысл имеют только утверждения о поведении в среднем большой совокупности атомов.
Закон радиоактивного распада определяет среднее число ядер атомов, распадающихся за определенный интервал времени.
Но всегда имеются неизбежные отклонения от среднего значения, и, чем меньше количество радиоактивных ядер в препарате, тем больше эти отклонения.
Закон радиоактивного распада является статистическим законом.
Говорить об определенном законе радиоактивного распада для малого числа ядер атомов не имеет смысла.
Этот закон справедлив в основном для большого количества частиц.
Источник: «Физика — 11 класс», учебник Мякишев, Буховцев, Чаругин
Физика атомного ядра. Физика, учебник для 11 класса — Класс!ная физика
Методы наблюдения и регистрации элементарных частиц —
Открытие радиоактивности. Альфа-, бета- и гамма-излучения —
Радиоактивные превращения —
Закон радиоактивного распада. Период полураспада —
Открытие нейтрона —
Строение атомного ядра. Ядерные силы. Изотопы —
Энергия связи атомных ядер —
Ядерные реакции —
Деление ядер урана —
Цепные ядерные реакции —
Ядерный реактор —
Термоядерные реакции. Применение ядерной энергии —
Получение радиоактивных изотопов и их применение —
Биологическое действие радиоактивных излучений —
Краткие итоги главы —
Три этапа в развитии физики элементарных частиц —
Открытие позитрона. Античастицы