Как вам известно, вещества могут находиться в твёрдом, жидком и газообразном состоянии. Молекулы жидкости и твёрдого вещества располагаются близко друг к другу. Это возможно благодаря тому, что молекулы притягиваются друг к другу. То есть существуют силы, которые удерживают молекулы жидкости или твёрдого вещества вместе. Из курса химии 8-го класса вы знаете, что эти силы называются силами межмолекулярного взаимодействия. Молекулы газов находятся на значительно большем расстоянии друг от друга, чем в случае жидкостей и твёрдых веществ. На таком расстоянии молекулы практически не взаимодействуют друг с другом. Поэтому, чтобы превратить жидкость или твёрдое вещество в газ, необходимо преодолеть силы межмолекулярного взаимодействия, отдалив молекулы друг от друга.
Переход в газообразное состояние осуществляется в результате нагревания веществ, находящихся в твёрдом или жидком состоянии (кипение жидкостей, возгонка твёрдых веществ).
Так как расстояние между молекулами газов значительно больше размеров самих молекул, то объём, который занимает газ, — это, по существу, объём свободного пространства между хаотически движущимися молекулами газа. Величина этого пространства определяется условиями, при которых находится газ, т. е. температурой и давлением. Эта величина примерно одинакова для всех газов. При этом объёмом, занимаемым самими молекулами, можно пренебречь. Отсюда следует закон Авогадро — в равных объёмах различных газов при одинаковых условиях содержится одинаковое число молекул.

Авогадро (1776—1856)
Интересно знать
Из курса химии 8-го класса вы уже знакомы с постоянной Авогадро, равной 6,02 ∙ 1023 моль–1, которая показывает, сколько частиц содержится в одном моле вещества. Эта величина названа в честь выдающегося итальянского учёного Амедео Авогадро, внёсшего значительный вклад в развитие молекулярной физики, электрохимии и других областей естествознания. На основании исследования соотношения объёмов реагирующих и образующихся газов, таких как водород и хлор, кислород и азот, Авогадро впервые предположил, что молекулы азота, кислорода, водорода и хлора состоят из двух атомов. Это предположение, сначала долго не находившее понимания у учёных того времени, впоследствии блестяще подтвердилось.
Из закона Авогадро вытекают два основных следствия.
Первое следствие. Один моль любого газа при одинаковых условиях занимает одинаковый объём. Этот объём называется молярным объёмом газа (Vm), и измеряется в дм3/моль. Молярный объём газа равен отношению объёма газа к его количеству:
.
Величина Vm зависит от температуры и давления. Например, при нагревании газы расширяются. Значит, при нагревании увеличивается молярный объём газа. В связи с этим сравнение характеристик различных газовых смесей необходимо осуществлять при одинаковых условиях — температуре и давлении. В качестве эталона таких условий приняты нормальные условия (н. у.): температура таяния льда (0 °С или 273,15 K) и атмосферное давление (101,3 кПа). При нормальных условиях Vm = 22,4 дм3/моль.
Таким образом, из закона Авогадро следует, что 22,4 дм3 любого газа при нормальных условиях содержат 6,02 ∙ 1023 молекул.
Второе следствие. Плотности газов относятся между собой как молярные массы газов.
Это видно из следующих соображений. Пусть имеется две порции различных газов. Рассчитаем их плотности:
газ 1: 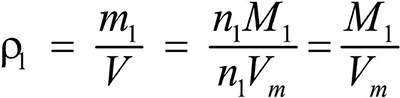
газ 2: 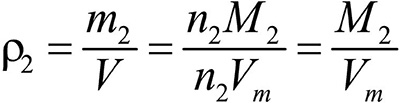
Разделив плотность первого газа на плотность второго, получим: 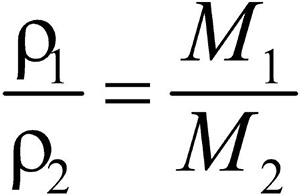
Отношение плотностей газов, равное отношению молярных масс, называется относительной плотностью одного газа по другому (D). D — величина безразмерная.
Зная D и молярную массу одного газа, легко найти молярную массу другого газа:
Пример 1. Относительная плотность газа по водороду равна 8. Определите молярную массу газа.
М(Х) = М(Н2) ∙ D = 2 ∙ 8 = 16 г/моль.
Газ с такой молярной массой — метан СH4.
Пример 2. Относительная плотность некоторого газообразного углеводорода по воздуху равна 2. Определите молярную массу углеводорода.
Средняя молярная масса воздуха равна 29 г/моль;
М(Х) = М(возд.) ∙ D = 29 ∙ 2 = 58 г/моль.
Углеводород с такой молярной массой — бутан С4Н10.
Следует отметить, что газы с молярной массой меньше 29 легче воздуха, больше 29 — тяжелее.
В расчётных задачах могут быть даны относительные плотности неизвестного газа по азоту, кислороду и другим газам. В этом случае для нахождения молярной массы неизвестного газа необходимо умножить относительную плотность на молярную массу соответственно азота (28 г/моль), кислорода (32 г/моль) и т. д.
Закон Авогадро широко применяется в химических расчётах. Поскольку для газов объёмы пропорциональны количествам (моль) веществ, то коэффициенты в уравнении реакции между газообразными веществами, отражающие количественное соотношение реагирующих веществ, пропорциональны объёмам взаимодействующих газов. Очевидно, что объёмы должны быть измерены при одинаковых условиях.
Пример 3. Какой объём кислорода потребуется для сжигания 2 дм3 пропана? Объёмы измерены при н. у.
Уравнение реакции горения пропана:
С3Н8 + 5О2 3СО2 + 4Н2О
Из закона Авогадро следует, что равные объёмы различных газов содержат одинаковое количество (моль) веществ. Пусть объём пропана равен 1 дм3. Тогда, согласно приведённому уравнению, для сжигания 1 дм3 пропана потребуется 5 дм3 кислорода. Следовательно, для сжигания 2 дм3 пропана потребуется:
1 дм3 С3Н8 — 5 дм3 O2,
2 дм3 С3Н8 — 10 дм3 О2
Ответ: V(О2) = 10 дм3.
Смеси газов
Рассмотрим две колбы объёмом 0,5 дм3. Одна колба заполнена азотом, а другая метаном. Давление и температура в колбах одинаковые. Если смешать содержимое этих колб, то полученная смесь займёт при таких же условиях объём 1 дм3.
Состав смеси газов часто выражают в объёмных долях. Объёмная доля газа обозначается греческой буквой φ (фи) и равна отношению объёма данного газа к объёму смеси. Рассчитаем объёмную долю азота в полученной выше смеси газов:
φ = = 0,5, или 50 %.
Пример 4. В результате пропускания 150 дм3 (н. у.) воздуха через избыток известковой воды выпало 0,201 г осадка. Найдите объёмную долю (%) углекислого газа в данном образце воздуха.
Уравнение реакции взаимодействия углекислого газа с известковой водой:
СО2 + Са(ОН)2 = СаСО3 + Н2О
Найдём количество (моль) карбоната кальция, выпавшего в осадок (M(CaCO3) = 100 г/моль):
n(СаСО3) = 0,201/100 = 0,00201 моль.
По уравнению реакции:
n(СаСО3) = n(СО2).
Рассчитаем объёмную долю углекислого газа в воздухе:
V(CO2) = 0,00201 ∙ 22,4 = 0,045 дм3;
φ(СО2) = 0,045/150 = 0,0003, или 0,03 %.
Ответ: φ(СО2) = 0,03 %.
Пример 5. Объём смеси водорода с хлором составляет 50 см3. После взаимодействия газов осталось 10 см3 хлора. Найдите состав исходной смеси в объёмных долях. Все объёмы измерены при н. у.
Уравнение реакции взаимодействия водорода с хлором:
H2 + Cl2 2HCl
Поскольку после взаимодействия осталось 10 см3 хлора, то 40 см3 исходной смеси прореагировало. Хлор и водород реагируют между собой в равных объёмных отношениях. Исходя из этих соображений, в реакцию вступили по 20 см3 хлора и водорода. Поскольку осталось 10 см3 хлора, то в первоначальной смеси было 20 см3 водорода и 30 см3 хлора.
Рассчитаем объёмные доли газов в исходной смеси:
φ(H2) = 20/50 = 0,4, или 40 %;
φ(Cl2) = 30/50 = 0,6, или 60 %.
Ответ: φ(H2) = 40 %; φ(Cl2) = 60 %.
Согласно закону Авогадро, в равных объёмах различных газов при одинаковых условиях содержится одинаковое количество молекул.
Один моль любого газа при нормальных условиях (температура таяния льда, атмосферное давление) занимает объём
22,4 дм3. Эта величина называется молярным объёмом газа (Vm).
Плотности газов, измеренные при одинаковых условиях, относятся между собой как их молярные массы. Это отношение называется относительной плотностью одного газа по другому газу.
Газы, имеющие молярную массу более 29 г/моль, тяжелее воздуха, а менее 29 г/моль — легче воздуха.
Объёмная доля газа в смеси равна отношению объёма данного газа к общему объёму смеси.
Вопросы: Состав и физико-химические
свойства природных газов, их классификация.
Газовые смеси, плотность газов, состав
газовой смеси. Парциальные давление и
объём в смеси идеальных газов. Аналитические
методы расчета физических свойств
природных газов. Вязкость газа
Состав и физико-химические свойства природных газов. Классификация природных газов
Природные газы, добываемые из чисто
газовых, нефтяных и газоконденсатных
месторождений, состоят из углеводородов
гомологического ряда метана (СnН2n+2), а также неуглеводородных
компонентов: азота (N2),
углекислого газа (СО2), сероводорода
(H2S),
редкоземельных (инертных) газов (гелия,
аргона, криптона, ксенона), ртути. Число
углеродных атомов n в молекуле углеводородов
может достигать 17 и более.
Метан
(СН4),
этан (С2Н6)
и этилен (С2Н4)
при нормальных условиях (Р = 0,1 МПа и T =
273 К) являются реальными газами. Пропан
(С3Н8),
пропилен (С3Н6),
изобутан (i-C4H10),
нормальный бутан (n-С4Н10),
бутилены C4Н8)
при атмосферных условиях находятся в
парообразном (газообразном) состоянии,
при повышенных давлениях — в жидком. Они
входят в состав жидких (сжижаемых,
сжиженных) углеводородных газов.
Углеводороды, начиная с изопентана
(i-C5H12)
и более тяжелые (17 > n > 5) при атмосферных
условиях находятся в жидком состоянии.
Они входят в состав бензиновой фракции.
Углеводороды, молекула которых состоит
из 18 и более атомов углерода (отC18H38),
расположенных в одну цепочку, при
атмосферных условиях находятся в твердом
состоянии.
Природные газы подразделяются на три
группы:
1. Сухой газ, свободный от тяжелых
углеводородов, добываемый из чисто
газовых месторождений.
2. Смесь сухого газа, пропанобутановой
фракции (сжиженного газа) и газового
бензина, добываемые вместе с нефтью.
3. Сухой газ и жидкий углеводородный
конденсат, добываемые из газоконденсатных
месторождений.
Углеводородный конденсат состоит из
большого числа тяжелых углеводородов,
из которых можно выделить бензиновые,
лигроиновые, керосиновые, а иногда и
более тяжелые маслянистые фракции.
Следует отметить, что в промышленности
используются искусственные газы,
полученные из твердых топлив (горючие
сланцы, бурый уголь и пр.).
Газовые смеси. Плотность газов
Под плотностью, или объёмной массой,
тела понимают отношение массы тела в
состоянии покоя к его объёму.
Плотность газа
в нормальных физических условиях (при
0,1013 МПа и 273 К) можно определить по формуле
(1)
где М —молекулярная масса.
Если плотность газа задана при давлении
0,1013 МПа, то пересчёт её на другое давление
(при той же температуре) для идеального
газа проводится по формуле
(2)
где Р – давление, МПа.
Часто для характеристики газа применяют
относительную плотность его по воздуху
при нормальных условиях (0,1013 МПа и 273 К)
(3)
Коммерческие расчёты в газовой
промышленности проводят при стандартных
физических условиях — 0,1013 МПа и 293 К.
Состав газовой смеси
Газовые смеси (как и смеси жидкостей и
паров) характеризуются массовыми или
молярными концентрациями компонентов.
Объёмный состав газовой смеси примерно
совпадает с молярным, так как объёмы 1
кмоля идеальных газов при одинаковых
физических условиях по закону Авогадро
имеют одно и то же численное значение,
в частности при 273 К и 0,1013 МПа составляют
22,41 м3.
Для характеристики газовой смеси следует
знать её среднюю молекулярную массу,
среднюю плотность (в кг/м3) или
относительную плотность по воздуху.
Если известен молярный состав смеси в
процентах, то среднюю молекулярную
массу вычисляют по формуле
(4)
где у1, у2, …,уn—молярные
(объёмные) доли компонентов, %;
Ml,
М2, …, Mn— молекулярные массы
компонентов.
Если
задан массовый состав смеси, то её
среднюю молекулярную массу определяют
по формуле
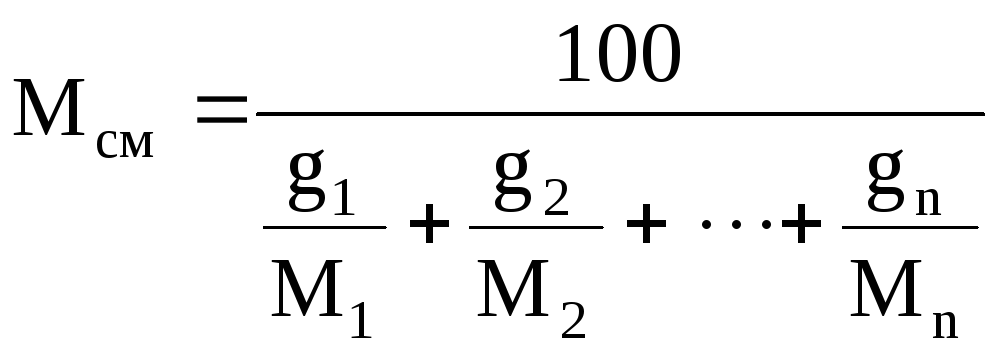
где g1,g2,
…,gn—массовые
доли компонентов, %.
Плотность смеси ρсм определяется
по вычисленному значению средней
молекулярной массы Мсмпо формуле,
аналогичной (1)
(6)
Относительную
плотность смеси вычисляют по формуле
(7)
где ρcми ρв— плотности соответственно смеси и
воздуха при 273 К и 0,1013 МПа.
Парциальные
давление и объём компонента в смеси
идеальных газов
Смеси
идеальных газов характеризуются
аддитивностью
парциальных давлений и парциальных
объёмов. Это означает, что каждый газ в
смеси идеальных ведет себя так, как если
бы в данном объёме он был бы один.
Парциальное давление газа — давление
газа, входящего в состав газовой смеси,
которое он оказывал бы, занимая один
весь объём смеси и находясь при неизменных
первоначальных объёме и температуре.
Парциальный объём — объём, который
занимал бы газ, входящий в состав газовой
смеси, если бы он находился при тех же
давлении и температуре, что и вся смесь.
Аддитивность
парциальных давлений выражается законом
Дальтона, согласно которому
(8)
где р — общее давление смеси
газов;
pi —парциальное давление
i-го компонента в смеси;
(9)
или
(10)
где ni
— число молей i-го компонента в смеси;
N — общее число молей смеси;
уi —
ni/N—молярная доля i-го компонента в
смеси.
Таким образом, парциальное давление
компонента рiв смеси
идеальных газов равно произведению его
молярной доли в смесиyiна общее давление смеси газовр.
Аддитивность парциальных объёмов
компонентов газовой смеси выражается
законом Амага, согласно которому
(11)
где V— общий объём смеси;
Vi, — парциальный объём
i-го компонента в смеси.
(12)
или
(13)
Таким образом, парциальный объём
компонента в смеси идеальных газов; Vi
—равен произведению его
молярной долиуi в
смеси на общий объёмVсмеси газов.
Аналитические
методы расчета физических свойств
природных газов
Для определения многих физических
свойств природных газов используют
уравнение состояния — аналитическую
зависимость между параметрами,
описывающими изменение
простого или сложного вещества (давление,
объём и температура).
Клапейрон и Менделеев предложили
следующее уравнение состояния идеальных
газов:
(14)
где р — абсолютное давление. Па;
V —объём, м3;
G— масса вещества, кг;
Т— абсолютная температура, К;
R — удельная
газовая постоянная, Дж/(кг К).
Идеальным называется газ, собственный
объём молекул, которого пренебрежимо
мал по сравнению с объёмом, занимаемым
газом, и когда отсутствует взаимодействие
между молекулами.
С термодинамической точки зрения
идеальным называется газ, для которого
справедливо равенство
(15)
где Е — внутренняя энергия парообразования,
Дж/моль или
(16)
где z — коэффициент
отклонения реального газа от закона
идеального.
Экспериментальная проверка уравнения
(14), проведенная многими исследователями,
показала, что изменение свойств реальных
газов при высоких давлениях нельзя
описать зависимостью (16).
Голландский физик Ван-дер-Ваальс в 1879
г. предложил учесть собственный объём
молекул газа и силы их взаимного
притяжения посредством введения
дополнительных членов в уравнение
Клапейрона — Менделеева:
(17)
где v — V/G— удельный объем газа, м3/кг;
а/v2— константа сцепления
молекул. Па;
b— поправка на собственный объём
молекул, м3.
В уравнении (17) слагаемое а/v2,выражает внутреннее давление, которое
является как бы равнодействующей сил
притяжения всех молекул в объёмеV.Оно прибавляется к внешнему давлению.
Это уравнение приближенное.
В соотношениях для критического состояния
вещества

коэффициенты aиbвыражаются
через критическое давлениеркри критическую температуруТкр
следующим образом:
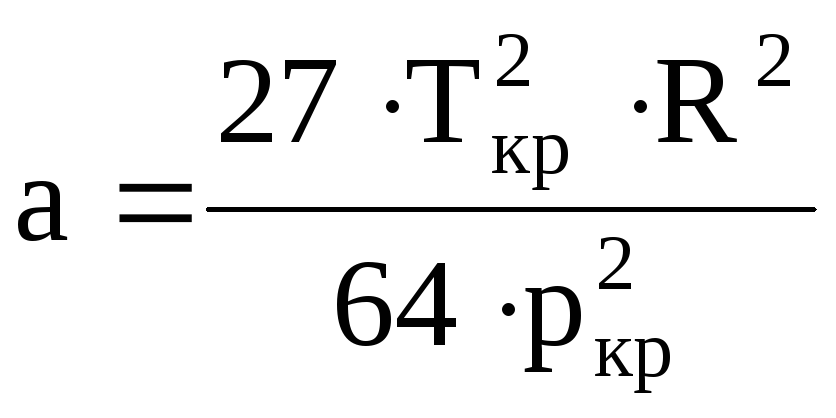
(19)
Ван-дер-Ваальс нашел, что поправка bна собственный объём молекул, имеющих
шарообразную форму, равна учетверённому
объёму молекул.
Уравнение (17) приближенное. Коэффициенты
аиbв действительности
являются сложными функциями объёма,
температуры, формы молекул газа.
Критическая температура чистого вещества
— это максимальная температура, при
которой жидкая и паровая фазы могут
сосуществовать в равновесии, или та
температура, при которой средняя
молекулярная кинетическая энергия
становится равной потенциальной энергии
притяжения молекул. При более высокой
температуре существование жидкой фазы
невозможно.
Давление
паров вещества при критической температуре
называется критическим давлением, а
объём вещества, отнесенный к одному
молю или другой единице массы вещества,
называется критическим удельным объёмом.
Критической принято называть такую
температуру, выше которой газ под
действием давления любого значения не
может быть обращен в жидкость.
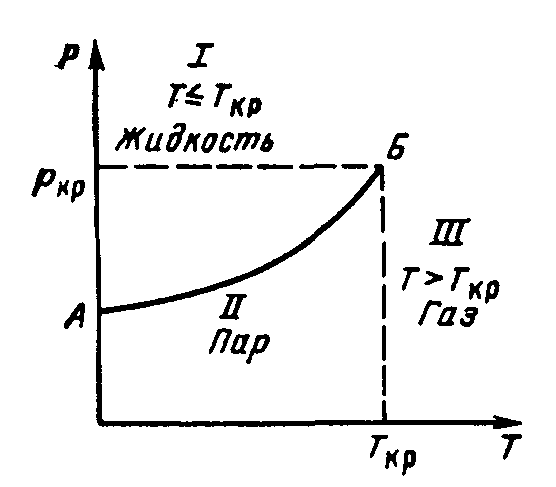
На рис. 1. приведена зависимость давления
(упругости насыщенных паров) чистых
веществ от температуры. Эта зависимость
более точно описывает изменение свойств
реальных газов при давлениях до 10 МПа
и температурах от 283 до 293 К, но она не
может численно описывать изменение,
свойств многокомпонентных смесей
месторождений природных газов.
Рисунок
1. Зависимость давления (упругости
насыщенных паров) чистых веществ от
температуры
Давление, необходимое для сжижения газа
при критической температуре, называется
критическим. Кроме критического давления
и критической температуры вводится
понятие критического объёма, равного
объёму одного моля газа при критических
давлении и температуре. Для природных
газов, представляющих собой смесь
отдельных компонентов, значения Ркр
и Ткр определяются
как среднекритические (псевдокритические).
Средние критические давление и температуру
смеси можно определить по формулам:
(20)
где х1, х2…хn— объёмные доли компонентов, входящих
в состав газа;
—критические давления компонентов;
— критические температуры компонентов.
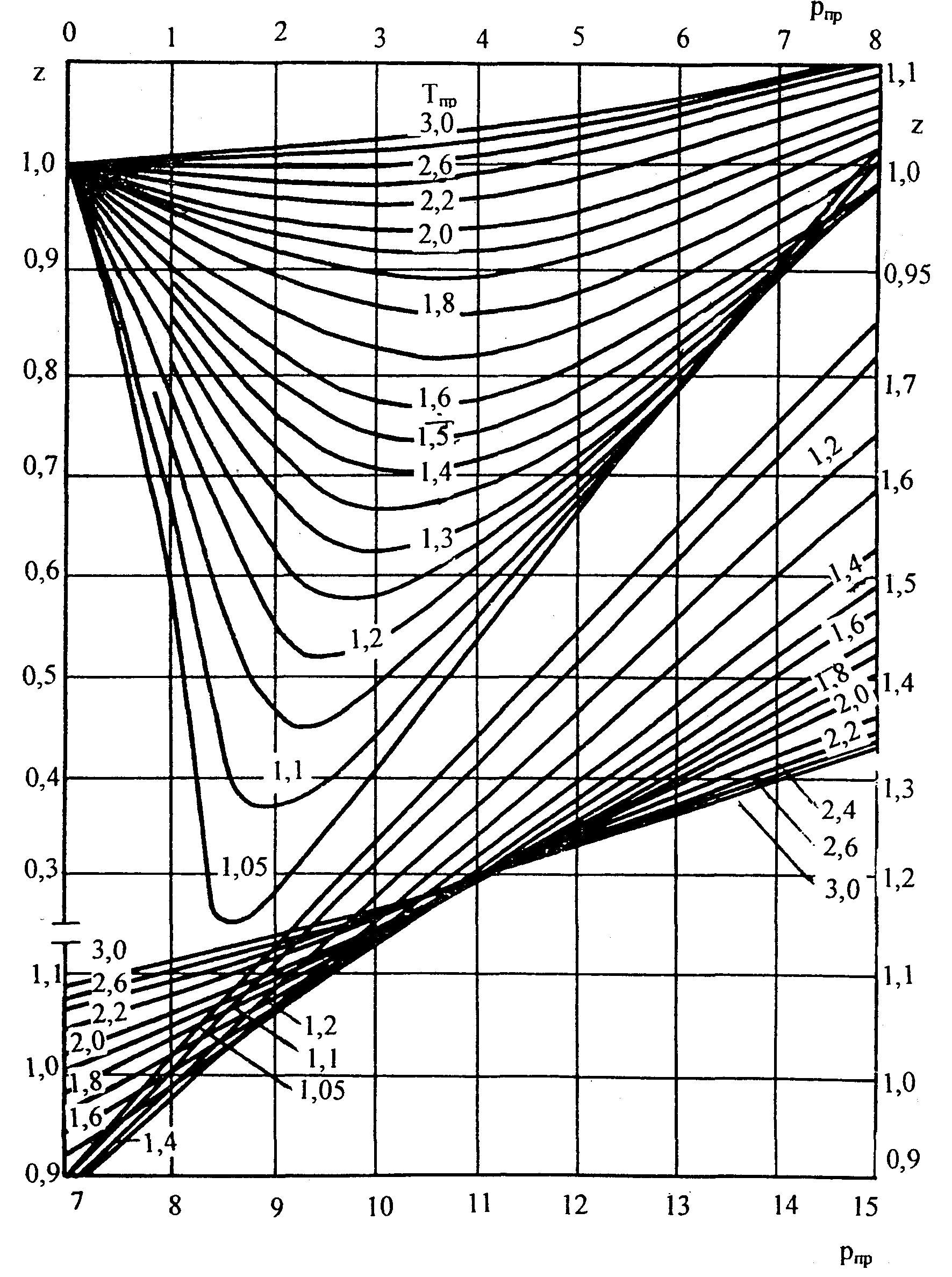
Следует отметить, что коэффициент
сверхсжимаемости природной углеводородной
смеси Zсмможно определить по
графической зависимости представленной
на рисунке 1.2.
Если известна относительная плотность
газа
,
то средние критические давление и
температуру природного газа можно
определить по графикам.При содержании в природном газеN2,
СО2илиH2Sв значенияРкр иТкрвводятся соответствующие поправки.
Когда содержаниеN2,CO2или Н2Sпревышает 15% об., вместо графиков для
определенияРкриТкрследует пользоваться формулой (1.20).
Рис. 1.2. Значение коэффициента
сверхсжимаемости z
по данным Стэндинга и Катца
Для приближенных расчётов при изменении
,
от 0,5 до 0,9 значенияРкриТкрможно определить
по формулам:
,
МПа (21)
,
К
Часто в расчётах, например, при определении
вязкости и коэффициента сверхсжимаемости
газа, пользуются так называемыми
приведенными давлениями и температурами.
Приведенными параметрами индивидуальных
компонентов называют безразмерные
величины, показывающие, во сколько раз
действительные параметры состояния
газа (давление, абсолютная температура,
объём, плотность, коэффициент отклонения)
больше или меньше критических:
Приведенным давлением Рпрназывается отношение давления газаРк его критическому давлениюРкр
(22)
Приведенной температурой газа Тпрназывается отношение абсолютной
температуры газаТк его критическому
значению:
,
(23)
Дальнейший прогресс науки и техники
потребовал разработки более точного
уравнения состояния природных газов,
способного правильно описывать изменение
их свойств при давлениях до 100 МПа и
температурах до 573 К в процессах добычи
газа и при давлениях до 20 МПа и низких
температурах до 223 — 93 К (от минус 50 до
минус180°С) в процессах переработки
природных газов.
В решении этой проблемы выявились два
направления:
1) введение поправочного коэффициента
zв уравнение состояния
идеального газа (1.17), учитывающего
отклонение реального газа от идеального,
т. е.pV==zRT
2) дополнение уравнения состояния
идеального газа большим числом констант.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Объёмные отношения газов при химических реакциях. Относительная плотность газов
I. Закон объемных отношений
«Объемы газов, вступающих в химические реакции, и объемы газов, образующихся в результате реакции, относятся между собой как небольшие целые числа».
Следствие. Стехиометрические коэффициенты в уравнениях химических реакций для молекул газообразных веществ показывают, в каких объемных отношениях реагируют или получаются газообразные вещества.
V1:V2:V3 = ν1:ν2:ν3.
Примеры:
2CO + O2 → 2CO2
При окислении двух объемов оксида углерода (II) одним объемом кислорода образуется 2 объема углекислого газа, т.е. объем исходной реакционной смеси уменьшается на 1 объем.
V(CO):V(О2):V(CO2) = ν(CO):ν(О2):ν(CO2) = 2 : 1 : 2
При синтезе аммиака из элементов:
N2 + 3H2 → 2NH3
Один объем азота реагирует с тремя объемами водорода; образуется при этом 2 объема аммиака — объем исходной газообразной реакционной массы уменьшится в 2 раза.
V(N2):V(H2):V(NH3) = ν(N2):ν(H2):ν(NH3) = 1 : 3 : 2
II. Решите задачу по образцу
Вычислите объём кислорода, который потребуется для сжигания 5 м3 метана СН4н.у.?
Образец:
Какой объём кислорода (н.у.) потребуется для полного сгорания 10 м3 пропана С3Н8 (н.у.)?
|
Дано: V(С3Н8) = 10 м3 |
Решение: 1. Запишем УХР С3Н8 +5О2 → 3СО2+ 4Н2О 1моль 5моль 2. Согласно закону объёмных отношений для газов: V(С3Н8):V(О2) = ν(С3Н8):ν(О2) = 1 : 5 10 м3 :V(О2) = 1 : 5 V(О2) = (10 · 5) /1= 50 м3 Ответ: для сжигания 10 м3 пропана потребуется 50 м3 кислорода. |
|
Найти: V(О2) = ? |
III. Относительная плотность газов
Закон Авогадро: в равных объёмах различных газов при одинаковых условиях (температуре и давлении) содержится одинаковое число молекул. (1811 г, итальянский учёный Амедео Авогадро)
Cледствия из закона Авогадро:
2 следствие:
Отношение масс одинаковых объёмов различных газов при одинаковых условиях равно отношению их молярных масс (поскольку в равных объёмах газов при одинаковых условиях содержится одинаковое число молекул и, следовательно, одинаковое число молей):
Это отношение называется относительной плотностью D ( или d) одного газа по другому.
D – показывает во сколько раз один газ тяжелее или легче другого и является безразмерной величиной.
Например,
DO2 (газа)= Mr(газа)/Mr(O2)=Mr(газа)/32;
DH2 (газа)= Mr(газа)/Mr(H2)=Mr(газа)/2;
Dвоздуха (газа)= Mr(газа)/Mr(воздуха)=Mr(газа)/29.
Задача
Образец: Найдите относительную плотность газа N2 по воздуху?
|
Дано: N2 М(воздуха) = 29 |
Решение: Dвоздуха (N2)= Mr(N2)/Mr(воздуха)=Mr(N2)/29. Mr(N2) = 2·Ar(N) = 2· 14 = 28 г/моль Dвоздуха (N2)= Mr(N2)/Mr(воздуха)=Mr(N2)/29=28/29= 0,97 |
|
Найти: Dвоздух — ? |
Ответ: газ азот легче воздуха в 0,97 раз Dвоздуха (N2)= 0,97 |
Задачи для самостоятельного решения
- Найдите относительную плотность газа О2 по водороду?
- Найдите относительную плотность газа СО2 по воздуху?
Решите задачуи для закрепления:
- Относительная плотность газа этана по водороду равна 15. Найдите молярную массу этана.
- Найдите относительную плотность газов по воздуху следующих газов: О2, Аr.
- Параграф 39
- Стр. 130 упр. 2,3 (письменно); тест