3аряд
внутренней сферы комплексного соединения
представляет собой алгебраическую
сумму зарядов образующих ее частиц.
Например,
величина и знак заряда комплекса [Fe
(C
2О4)2]
определяется следующим образом. Заряд
иона железа равен +3, суммарный заряд
двух оксалат ионов – (–4). Следовательно,
заряд комплекса =(+3)+(–4)=–1 и формула
комплекса [Fe(С2О4)2]
—.
Заряд комплексного иона численно равен
суммарному заряду внешней сферы и
противоположен ему по знаку. Например,
заряд внешней сферы К3[Fe(CN)
6]
равен +3. Следовательно, заряд комплексного
иона равен -3.
3аряд
комплексообразователя равен по
величине и противоположен по знаку
алгебраической сумме зарядов всех
остальных частиц комплексного соединения.
Отсюда,
в К3
[Fe(CN)
6]
заряд иона железа равен +3, т.к. суммарный
заряд всех остальных частиц комплексного
соединения равен (+3) + (–6) = –3.
Наиболее
устойчивые и разнообразные комплексы
по составу и выполняемым ими функциям
образуют d–элементы. Особенно большое
значение имеют комплексные соединения
переходных элементов: железа, марганца,
кобальта, меди, цинка и молибдена, которые
выступают в качестве комплексообразователя.
Биогенные s–элементы (Na, К, Mg, Са) образуют
комплексные соединения только с лигандами
определенной циклической структуры,
выступая также в качестве
комплексообразователя. Основная часть
р–элементов (N, Р, S, О) является активной
действующей частью комплексообразующих
частиц (лигандов) в том числе и биолигандов.
В этом состоит их биологическая
значимость.
Следовательно,
способность
к комплексообразованию —
это общее свойство химических элементов
периодической системы Д. И. Менделеева,
эта способность уменьшается в следующем
порядке: f>d>p>>s.
2. Химическая связь в комплексных соединениях и особенности их строения
В
образовании комплексных соединений
важную роль играют донорно — акцепторные
взаимодействия лиганда и центрального
атома. Донором электронной пары, как
правило, является лиганд. Акцептором –
центральный атом, который имеет свободные
орбитали. Связь эта прочна и не разрывается
при растворении комплекса (неионогенна)
и ее называют координационной.
Наряду
с s-связями образуются p-связи по
донорно-акцепторному механизму. При
этом донором служит ион металла отдающий
свои спаренные d-электроны
лиганду, имеющему энергетически выгодные
вакантные орбитами. Такие связи называют
дативными. Они образуются: а) за счет
перекрывания вакантных р-орбиталей
металла с d-орбиталью
металла на которой находятся электроны
не вступившие в s-связь (dp-pp
взаимодействие); б) при перекрывании
вакантных d-орбиталей
лиганда с заполненными d-орбиталями
металла (dp-dp
взаимодействие).
Ионы
d–элементов образуют с биосубстратами
(белками) прочные комплексы. А мягкие
кислоты Cd, Pb, Hg сильно токсичны. Они
образуют прочные комплексы с белками
содержащими R—SH группы,
2R—SH+Hg
2+
®R—S—Hg—S—R+2H+
Цианид–ион
токсичен. Мягкий лиганд активно
взаимодействует с d–металлами в
комплексах с биосубстратами, активируя
последние.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Просмотров 8.5к. Опубликовано 04.09.2022
Простые вещества, такие как Cl2и О2 в этом случае не происходит сдвига электронов и степень окисления равна нулю.
Качественная характеристика окислительно-восстановительных реакций
Окислительно-восстановительные реакции являются наиболее распространенными химическими реакциями в природе. К ним относятся, например, фотосинтез, метаболизм и биологические процессы, а также сжигание топлива, производство металлов и многие другие реакции.
Реакции восстановления давно и успешно используются человечеством для самых разных целей, но сама теория электронов в окислительно-восстановительных процессах возникла совсем недавно, т.е. в начале 20 века.
Для того чтобы перейти к современной теории окислительно-восстановительных процессов, необходимо ввести различные понятия, такие как сила, степень окисления и структура электронной оболочки атома. Мы уже сталкивались с этими понятиями при изучении таких модулей, как периодический закон Менделеева, основные принципы атомной структуры элементов, химическая связь и молекулярная структура. Давайте теперь рассмотрим их более подробно.
Валентность
Живучесть — это сложное понятие, которое возникает с понятием химической связи и определяется как свойство атома соединяться с определенным количеством атомов другого элемента или вытеснять их, т.е. способность атома образовывать химические связи в соединении.
Изначально валентность определялась по водороду (считался как 1) или кислороду (валентность 2).
Впоследствии были выделены положительные и отрицательные значения. Количественно, положительная валентность — это число электронов, поставляемых атомом, а отрицательная валентность — это число электронов, которые должны быть присоединены к атому для выполнения правила октавы (т.е. для завершения внешнего энергетического уровня).
Совсем недавно в понятие жизненной силы стали включать природу химических связей, образующихся при объединении людей.
Как правило, наибольшая интенсивность данных соответствует номеру группы в периодической таблице.
Однако, как и во всех правилах, есть исключения.
Например, медь и золото находятся в первой группе периодической таблицы, и их интенсивность должна быть равна номеру группы, т.е. 1, тогда как на практике медь имеет максимальную интенсивность 2, а золото — 3.
Степень окисления
Степень окисления, иногда называемая окислительным числом, электрохимической валентностью или состоянием окисления, является относительным понятием.
Например, при расчете степеней окисления большинство соединений вообще не являются ионными, а молекулами считаются только ионы.
Количественно, степень окисления атомов элемента в соединении определяется числом электронов, присоединенных к атомам или смещенных с них.
Таким образом, если смещения электронов не происходит, степень окисления будет равна нулю, отрицательной — если электроны смещены в сторону конкретного атома, и положительной — если они смещены в сторону от конкретного атома.
Нахождение степени окисления химического вещества — простое занятие, требующее лишь внимания и знания основных правил и исключений. Для того чтобы разобраться в исключениях и использовать специальные таблицы, не требуется много времени.
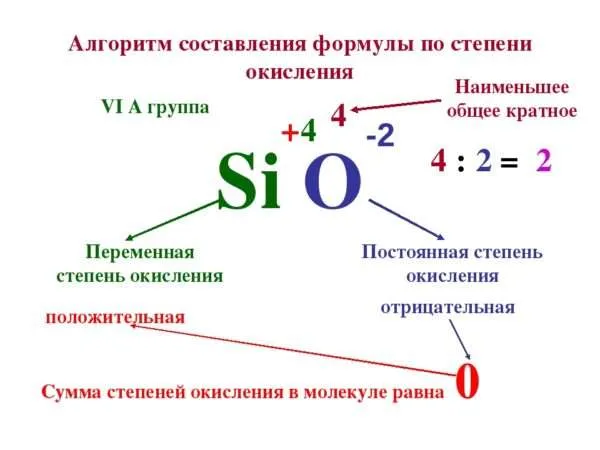
Как расставлять и как определить степень окисления элементов
Атомы и молекулы играют важную роль в химических процессах, а их свойства определяют последствия химических реакций. Одним из важных свойств атомов является их число окисления. Это упрощает метод расчета переноса электронов на частицы. Как определить степень окисления или типичный заряд частицы и какие правила для этого нужно знать?
Все химические реакции происходят в результате взаимодействия атомов различных веществ. Свойства мелких частиц определяют процесс реакции и ее последствия.
Термин окисление в химии относится к реакции, в которой группа атомов или один из них теряет или приобретает электрон. В случае усиления реакция называется «восстановлением».
Состояние окисления — это количественная мера перераспределения электронов в реакции. Другими словами, в процессе окисления электроны внутри атома уменьшаются или увеличиваются и перераспределяются между другими взаимодействующими частицами, а степень окисления показывает, как именно они реорганизуются. Это понятие тесно связано с электроотрицательностью частиц, т.е. их способностью притягивать и отталкивать свободные ионы.
Это интересно! Что такое алканы: структура и химические свойства
Определение степени окисления зависит от свойств и характеристик каждого вещества, поэтому процесс расчета нельзя однозначно охарактеризовать как простой или сложный, но результаты помогают документировать процесс обычных окислительно-восстановительных реакций. Важно понимать, что результаты расчета являются следствием переноса электронов, не имеют физического смысла и не представляют фактический заряд ядра.
Важно знать! Обратите внимание, что в неорганической химии термин валентность часто используется вместо состояния окисления элемента, что не является ошибкой, но второй термин более распространен.
Понятия и правила расчета движения электронов лежат в основе классификации химических веществ (номенклатуры), описания их свойств и синтеза типов связей. Однако часто этот термин используется для описания и проведения окислительно-восстановительных реакций.
Правила определения степени окисления
Как узнать состояние окисления? Имея дело с окислительно-восстановительными реакциями, важно знать, что типичный заряд частицы всегда равен численно выраженному значению электрона. Эта специфика обусловлена предположением, что электронная пара, образующая связь, всегда полностью смещается к наиболее отрицательной частице. Если мы говорим об ионной связи, то следует понимать, что в случае реакций ковалентной связи электроны поровну распределяются между одними и теми же частицами.
Число окисления может иметь как положительное, так и отрицательное значение. Важно отметить, что во время реакции атомы должны стать нейтральными. Для этого необходимо добавить электрон, если ион положительный, или удалить его, если он отрицательный. Чтобы указать на это значение при записи типа, принято писать арабскую цифру с соответствующим символом над названием предмета. Например, или и т.д.
Следует отметить, что заряд металла всегда положительный и в большинстве случаев его можно определить с помощью таблицы Менделеева. Существует несколько характеристик, которые необходимо учитывать для правильного определения цены
Как определить степень окисления
- У простых элементов всегда равна нулю: или .
- У фтора всегда будет равна -1.
- Как и у металлов, у элементов из групп IA, IIA и IIIA групп всегда одинаковая – это номер группы, в которой они расположены.
- У кислорода в любой связи равна -2, кроме связей с пероксидами (Н2О2), когда значение равно -1 и оксидом фтора (O+2F2-1, O2+1F2-1), когда она равна +2.
- У водорода всегда +1, кроме его взаимодействия с гидридами (Na+H- и связями по типу C+4H4-1).
- У простого вещества без связей с другими элементами всегда равна нулю.
- У простого иона с одним атомом равна числу его электрона (Na+, Ca+2).
- Если рассматривается связь двух веществ различной природы (металл и неметалл), то отрицательное окислительное число будет наблюдаться у вещества, которое обладает большей электроотрицательностью (H+F-, Cu+Br-), а положительное, соответственно, у элемента с электроотрицательностью больше нуля.
- У щелочных металлов, таких как литий, натрий, калий и прочих, всегда +1.
- У металлов из главной подгруппы II (магний, барий, кальций и стронций) равна +2.
- У алюминия всегда одинаковое значение +3.
Запомнив эти свойства, очень легко определить номер окисления элемента, независимо от его атомной сложности или количества уровней.
Полезное видео: определение степени окисления
Регулярные таблицы Менделеева содержат практически всю информацию, необходимую для работы с химическими веществами. Например, студенты используют их только для описания химических реакций. Например, чтобы определить максимальные положительные и отрицательные числа окисления, им нужно проверить названия химических веществ в таблице.
- Максимально положительное – это номер группы, в которой находится элемент.
- Максимально отрицательная степень окисления – это разница между максимально положительной границей и числом 8.
Поэтому очень легко найти стандартные пределы погрузки для того или иного товара. Такие действия можно выполнить с помощью расчетов, основанных на таблице Менделеева.
Это важно знать! Элемент может одновременно иметь множество различных значений окисления.
Существует два основных способа определения уровня окисления. Примеры приведены ниже. Первый метод требует знания и умения применять химические законы. Как с помощью этого метода можно определить степень окисления?
Правила определения состояния окисления.
- Определить, является ли данное вещество элементарным и находится ли оно вне связи. Если да, то его окислительное число будет равно 0, независимо от состава вещества (отдельные атомы или многоуровневые атомные соединения).
- Определить, состоит ли рассматриваемое вещество из ионов. Если да, то степень оксидации будет равна их заряду.
- Если рассматриваемое вещество металл, то посмотреть на показатели других веществ в формуле и вычислить показания металла путем арифметических действий.
- Если все соединение имеет один заряд (по сути это сумма всех частиц представленных элементов), то достаточно определить показатели простых веществ, затем вычесть их от общей суммы и получить данные металла.
- Если связь нейтральная, то общая сумма должна быть равна нулю.
Это интересно! Курс химии: что такое галоген?
В качестве примера рассмотрим соединение ионов алюминия с общим зарядом, равным нулю. Правила химии подтверждают тот факт, что число окисления иона Cl равно -1, и в этом случае в соединении их три. Поэтому, чтобы нейтрализовать все соединение, ион al должен иметь значение +3.
Этот метод очень хорош тем, что, суммируя все уровни окисления вместе, всегда можно контролировать точность раствора.
Второй метод можно применять без знания химических законов.
- Найти данные частиц, по отношению к которым нет строгих правил и точное количество их электронов неизвестно (можно путем исключения).
- Выяснить показатели всех прочих частиц и после из общей суммы путем вычитания найти нужную частицу.
Рассмотрим второй метод на примере вещества Na2SO4, где отдельные S не определены.
Это интересно! Курс химии: катионы и анионы — что это такое?
Для того чтобы все степени окисления были одинаковыми, необходимо
- Найти известные элементы, помня о традиционных правилах и исключениях.
- Ион Na = +1, а каждый кислород = -2.
- Умножить количество частиц каждого вещества на их электроны и получить степени оксидации всех атомов, кроме одного.
- В Na2SO4 состоят 2 натрия и 4 кислорода, при умножении получается: 2 X +1 = 2 – это окислительное число всех частиц натрия и 4 X -2 = -8 – кислородов.
- Сложить полученные результаты 2+(-8) =-6 – это общий заряд соединения без частицы серы.
- Представить химическую запись в виде уравнения: сумма известных данных + неизвестное число = общий заряд.
- Na2SO4 представлено следующим образом: -6 + S = 0, S = 0 + 6, S = 6.
С ионом NH4 + ион, вид азотной нагрузки — x + (+1) x 4 = 1. Ясно, что x = -3, т.е. степень окисления азота равна -3.
Таблица окисления химических элементов
Таблицы химического окисления используются для определения состояния загрузки индивида в реакции окисления. В зависимости от качества индивида элемент может иметь положительное или отрицательное состояние окисления.
Что такое степень окисления
Элементарная нагрузка элемента в композитном материале называется его состоянием окисления. Величина нагрузки индивидуума регистрируется в окислительно-восстановительной реакции, чтобы понять, какие элементы восстанавливаются и какие окислители восстанавливаются.
Степень окисления связана с электричеством и указывает на способность человека принимать или отдавать электроны. Чем выше значение электронов, тем больше способность человека потреблять электроны в реакции.
Рисунок 1. Ряд электрических свойств.
Для состояния окисления существует три значения.
- нулевое – атом находится в состоянии покоя (все простые вещества имеют степень окисления 0);
- положительное – атом отдаёт электроны и является восстановителем (все металлы, некоторые неметаллы);
- отрицательное – атом принимает электроны и является окислителем (большинство неметаллов).
Например, степень окисления в реакции между натрием и хлором составляет
В реакциях с неметаллическими металлами металл всегда является восстановителем, а неметалл — окислителем.
Как определить
Существует таблица, показывающая все возможные состояния окисления элементов.
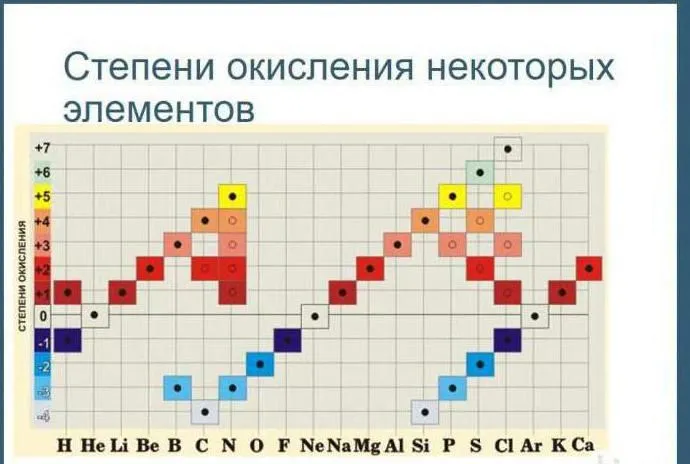
Состояние окисления
В качестве альтернативы используйте эту версию таблицы в уроке.
Рисунок 2.Таблица окисления.
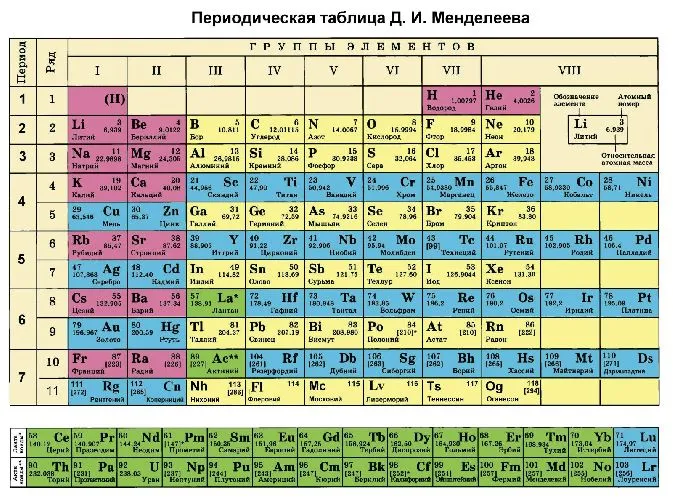
В качестве альтернативы, степень окисления химического элемента можно определить по периодической таблице Менделеева.
- высшая степень (максимально положительная) совпадает с номером группы;
- для определения минимального значения степени окисления из номера группы вычитается восемь.
Рисунок 3. Таблица Менделеева.
Большинство неметаллов имеют положительную и отрицательную степень окисления. Например, кремний относится к группе IV и имеет максимальную степень окисления +4 и минимальную -4. К неметаллическим соединениям (так3co2, sic) окислительные среды — это неметаллы с отрицательной степенью окисления или высшей электризуемостью. Например, в Союзе PCL3Фосфор имеет степень окисления +3, а хлор -1. Электроны фосфора составляют 2,19, а хлора — 3,16.
Второе правило не применяется к щелочным и щелочноземельным металлам, которые всегда имеют положительную степень окисления, равную номеру группы. Исключение составляют магний и бериллий (+1 и +2). Состояние окисления также является постоянным.
Другие металлы не имеют стабильного состояния окисления. В большинстве реакций они выступают в качестве восстановителей. В редких случаях это могут сделать окислители с отрицательной степенью окисления.
Фтор является сильнейшим окислителем. Его степень окисления всегда равна -1.
Для соединений определяется, состоят ли они из ионов. Для многоатомных ионов сумма всех степеней окисления равна их нагрузке. Найдите эту сумму из таблицы растворителей и приравняйте ее к известному числу окисления.
Как расставлять степень окисления в солях
Соль состоит из металла и одного или нескольких кислотных остатков. Метод определения такой же, как и для кислых кислот.
Металл, непосредственно образующий соль, находится в главной подгруппе, и его степень равна номеру группы. Это означает, что они всегда остаются стабильными.
В качестве примера рассмотрим расположение степеней окисления нитрата натрия. Соль образована элементами главной подгруппы в группе 1, поэтому ее степень окисления положительна и равна 1. В нитрате кислород имеет значение -2. Чтобы получить числовое значение, сначала строится уравнение с неизвестными, учитывающее все отрицательные и положительные значения, +1 +x-6 = 0. Решив уравнение, можно прийти к тому, что число положительное и равно + 5. Такова цена азота. Таблица является ключом к расчету степени окисления.
Как определить заряд комплексного иона
Существует целый класс сложных химических веществ — комплексных соединений. В их состав входят: центральный атом – комплексообразователь, внутренняя и внешняя сфера. Внутренняя сфера может состоять как из ионов, так и из молекул, а также из сочетания ионов и молекул. Внешней сферой может быть как положительно заряженный катион, так и отрицательно заряженный анион. Комплексообразователь вместе с внутренней сферой образуют так называемый комплексный ион.

Инструкция
Первым делом напишите точную формулу комплексного соединения. Вот, например, желтая кровяная соль – гексацианоферрат калия. Ее формула: К4[Fe(CN)6].
Определите состав комплексного иона. В данном случае это ион [Fe(CN)6], величину и знак заряда которого вам надо определить. А четыре иона калия составляют внешнюю сферу этого соединения.
Теперь вам поможет одно из основных правил химии, гласящее: любая молекула электрически нейтральна. То есть в данном конкретном случае суммарный заряд молекулы гексацианоферрата калия также равен нулю. А это может быть только тогда, когда заряд комплексного иона [Fe(CN)6] уравновешен суммарным зарядом четырех ионов калия, находящихся во внешней сфере. То есть заряд комплексного иона такой же по размерности, но с противоположным знаком.
Посмотрите в таблицу Менделеева. Калий – один из самых активных металлов, он уступает только своим собратьям по первой главной группе таблицы – рубидию, цезию и францию. Следовательно, по сравнению с другими элементами, входящими в состав этого соединения, – железом (Fe), углеродом (С) и азотом (N), калий, безусловно, самый электроположительный. То есть он будет не притягивать к себе общую электронную плотность молекулы, а отталкивать ее от себя. Это вполне объяснимо, ведь у калия на внешнем электронном уровне всего один электрон, и ему гораздо легче отдать его (чтобы предыдущий уровень, на котором восемь электронов, стал устойчивым), нежели притянуть еще целых семь.
Таким образом, каждый атом калия, образуя химическую связь в этой молекуле, отдал по одному электрону и превратится, соответственно, в ион с положительным зарядом +1. Таких ионов четыре, следовательно, суммарный заряд внешней сферы равен +4. А чтобы молекула была нейтральной, его должен уравновесить заряд -4. Вот и ответ на поставленный вопрос.
Войти на сайт
или
Забыли пароль?
Еще не зарегистрированы?
This site is protected by reCAPTCHA and the Google Privacy Policy and Terms of Service apply.
Как определить заряд иона | Сделай все сам
В силу определенных причин атомы и молекулы могут либо приобретать, либо терять свои электроны. В этом случае образуется ион. Таким образом, ион – это одноатомная либо многоатомная заряженная частица. Видимо, важнейшей колляцией иона будет его заряд .
Вам понадобится
- Таблица химических элементов Д.И. Менделеева
Инструкция
1. Атом всякого вещества состоит из электронной оболочки и ядра. Ядро состоит из 2-х типов частиц – нейтронов и протонов.
Нейтроны не имеют электрического заряд а, то есть электрический заряд нейтронов равен нулю.
Протоны являются позитивно заряженными частицами и имеют электрический заряд , равный +1. Число протонов характеризует ядерный номер данного атома.
2. Электронная оболочка атома состоит из электронных орбиталей, на которых расположено различное число электронов. Электрон – негативно заряженная элементарная частица. Ее электрический заряд равен -1.При помощи связей атомы могут также соединяться в молекулы.
3. В нейтральном атоме число протонов равно числу электронов. Следственно его заряд равен нулю.Дабы определить зарядиона , нужно знать его конструкцию, а именно число протонов в ядре и число электронов на электронных орбиталях.
4. Суммарный зарядиона получается в итоге алгебраического суммирования заряд ов входящих в него протонов и электронов. Число электронов в ионе может превышать число протонов, и тогда ион будет негативным. Если число электронов поменьше числа протонов, то ион будет правильным.
5. Зная химический элемент, по таблице Менделеева мы можем определить его ядерный номер, тот, что равен числу протонов в ядре атома этого элемента (скажем 11 у натрия). Если один из электронов оставил атом натрия, то у атома натрия будет теснее не 11, а 10 электронов.
Атом натрия станет одобрительно заряженным ионом с заряд ом Z = 11+(-10) = +1.Обозначаться такой ион будет символом Na с плюсом сверху, в случае заряд а +2 – двумя плюсами и.т.д. Соответственно для негативного иона применяется знак «минус».
Совет 2: Как определить заряд ядра
Атом химического элемента состоит из ядра и электронной оболочки. Ядро – это центральная часть атома, в котором сфокусирована примерно каждая его масса. В различие от электронной оболочки, ядро имеет позитивный заряд .
Вам понадобится
- Атомный номер химического элемента, закон Мозли
Совет 3: Как определять ионы
Впереди лабораторная работа, а необходимые навыки и знания по распознаванию химических веществ не наработаны. А может в химической лаборатории нечаянно отклеились этикетки с наименованиями соединений.
Знание верно определять химические вещества в силу своей специфичности может теснее не понадобиться позже окончания учебных заведений. Но но эти познания могут потребоваться собственному ребенку, тот, что придет за подмогой.
Что тогда ему ответить?
Вам понадобится
- Штатив с пробирками, реагенты для определения веществ, спиртовка, проволочка с петелькой, индикаторы
Совет 4: Как определить заряд у элемента
В обыкновенных условиях атом электрически нейтрален. При этом ядро атома, состоящее из протонов и нейтронов, заряжено одобрительно, а электроны несут негативный заряд. При избытке либо недостатке электронов атом превращается в ион.
Совет 5: Как определить электрический заряд
Электрический заряд – это величина, характеризующая способность физического тела быть источником электромагнитного поля и принимать участие во взаимодействии с другими сходственными источниками. Еще древние греки нашли, что если кусок янтаря потереть о шерсть, то он приобретет способность притягивать легкие предметы. Янтарь на древнегреческом языке именовался «электрон».
Урок 6. Простые ионы – HIMI4KA
Архив уроков › Основные законы химии
В уроке 6 «Простые ионы» из курса «Химия для чайников» познакомимся с простыми ионами и выясним, чему равен его заряд; также рассмотрим как образуется ионная химическая связь; научимся определять степень окисления и валентность элементов. Данный урок очень важный, и чтобы его лучше понять, обязательно просмотрите прошлые уроки, особое внимание уделяя уроку 1 «Схема строения атомов», а также уроку 3 «Схема образования молекул».
Ионная химическая связь
Мы уже кратко рассматривали ковалентную полярную химическую связь, в которой из-за незначительного различия в электроотрицательности атомов (0.4-2.0) электронная пара распределяется между ними не равномерно. Для тех, кто забыл, напоминаю, что электроотрицательность — это способность атомов притягивать к себе электроны.
Однако, если электроотрицательность атомов различается больше чем на 2 по таблице электроотрицательности, то электронная пара полностью переходит к более электроотрицательному атому, и в результате образуется ионная химическая связь. Ионная химическая связь образуется только между атомами типичных металлов (т.к. они легко теряют внешние электроны) и неметаллов (т.к. они обладают большой электроотрицательностью).
Положительные и отрицательные ионы
Наглядным примером ионной химической связи может служить обычная поваренная соль NaCl, которая присутствует на каждой кухне. Атомы натрия (и вообще всех металлов) слабо удерживают внешние электроны, тогда как атомы хлора напротив, обладают очень большой способностью притягивать к себе электроны, т.е обладают большой электроотрицательностью.
Поэтому при образовании молекулы NaCl каждый атом Na теряет один электрон (e—), образуя положительный ион натрия Na+, а каждый атом Cl, наоборот, приобретает этот потерянный электрон натрия, образуя отрицательный ион хлора Cl—. Это записывается в виде двух реакций:
- Na → Na+ + e— и ½Cl2 + e— → Cl—
Записать ½Cl2 пришлось потому, что газообразный хлор в природе состоит из двухатомных молекул, а не из свободных одиночных атомов хлора.
На рисунке выше, изображена кристаллическая решетка NaCl, где каждый хлорид-ион Cl— окружен со всех сторон соседними положительными ионами натрия Na+; ионы натрия Na+ точно также окружены ближайшими хлорид-ионами Cl—. Подобное расположение ионов обладает высокой устойчивостью.
Положительно заряженные ионы называются катионами. К ним в основном относятся металлы, так как они легко отдают от одного до трех электронов. Ниже приведены примеры катионов:
Анионами являются неметаллы, поскольку с радостью присоединяют к себе электроны, превращаясь в отрицательно заряженные ионы. Примеры анионов:
Степень окисления веществ
Заряд простого, одноатомного иона, например Mg2+ или F2-, называется его степенью окисления. Степень окисления — это такое число электронов, которое необходимо прибавить (восстановить) к иону или отнять (окислить) у него, чтобы он превратился обратно в нейтральный атом.
- Реакция восстановления: Mg2+ + 2e— → Mg
- Реакция окисления: F2- → F + 2e—
Процесс присоединения электронов к атому или просто их смещение в сторону данного атома называется реакцией восстановления, а оттягивание электронов от атома или их полное удаление называется реакцией окисления. Вот вам отличная шпаргалка со степенями окисления простых ионов:
Пример 12. Окисляется или восстанавливается хлор при образовании хлорид-иона? Какова степень окисления этого иона?
Решение: Хлор восстанавливается, поскольку к каждому атому хлора необходимо присоединить один электрон, чтобы образовался хлорид-ион. Хлорид-ион, Сl—, имеет степень окисления -1.
Пример 13. Окисляются или восстанавливаются металлы при образовании ими ионов? Какова степень окисления иона алюминия?
Решение: При образовании ионов металлов последние окисляются, поскольку при этом происходит удаление электронов от атомов металла. Ион алюминия, Аl3+, имеет степень окисления +3.
Валентность химических элементов
Валентностью называют число химических связей, которые данный атом образует с другими атомами в молекуле. Однако, если говорить простыми словами, то под валентностью понимается все та же степень окисления, но в отличии от нее валентность не имеет знака и не равна нулю.
| Молекулярная формула | Валентность | Степень окисления |
| H2O | H(I), O(II) | H+1, O-2 |
| CS2 | C(IV), S(II) | C+4, S-2 |
| CH4 | C(IV), H(I) | C-4, H+1 |
Название ионов
Ионы металлов, которые имеют различные (переменные) степени окисления, записываются следующим образом:
- Fe2+ железо(II) или ион двухвалентного железа
- Fe3+ железо(III) или ион трехвалентного железа
- Сu+ медь(I) или ион одновалентной меди
- Cu2+ медь (II) или ион двухвалентной меди
- Sn2+ олово(II) или двухвалентного олова
- Sn4+ олово(IV) или ион четырехвалентного олова
Пример 2: Окисление или восстановление происходит при превращении иона трехвалентного железа в ион двухвалентного? Запишите уравнение этого процесса.
Решение: Уравнение реакции имеет следующий вид: Fe3+ + e— → Fe2+. Она представляет собой процесс восстановления, поскольку к исходному иону присоединяется электрон.
Надеюсь урок 6 «Простые ионы» оказался для вас понятным и полезным. Если у вас возникли вопросы, пишите их в комментарии.
Источник: https://himi4ka.ru/arhiv-urokov/urok-6-prostye-iony.html
Содержание:
- Последовательное соединение конденсаторов
- Параллельное соединение конденсаторов
- Смешанное соединение конденсаторов
- Пример расчета
В данной статье приведены различные схемы соединения конденсаторов, а так же формулы их расчета с примером.
-
Последовательное соединение конденсаторов
Если условно разделить выводы каждого из конденсаторов на первый и второй выводы последовательное соединение конденсаторов будет выполняется следующим образом: второй вывод первого конденсатора соединяется с первым выводом второго конденсатора, второй вывод второго конденсатора, соединяется с первым выводом третьего и так далее. Таким образом мы получим группу (блок) последовательно соединенных конденсаторов с двумя свободными выводами — первым выводом первого конденсатора в блоке и вторым выводом последнего конденсатора, через которые данный конденсаторный блок и подключается в электрическую цепь.
Схема последовательного соединения конденсаторов будет иметь следующий вид:
Фактически последовательное соединение конденсаторов имеет следующий вид:
При данной схеме соединения заряды на конденсаторах будут одинаковы:
Qобщ=Q1=Q2=Q3,
где: Q1, Q2, Q3 — соответственно заряд на первом, втором, третьем и т.д. конденсаторах
Напряжение на каждом конденсаторе при такой схеме зависит от его емкости:
U1=Q/C1; U2=Q/C2; U3=Q/C3, где:
- U1, U2, U3 — соответственно напряжение на первом, втором, третьем конденсаторах
- C1, C2, C3 — соответственно емкости первого, второго, третьего конденсаторов
При этом общее напряжение составит:
Uобщ=U1+U2+U3+…+Un
Рассчитать общую емкость конденсаторов при последовательном соединении можно по следующим формулам:
- При последовательном соединении двух конденсаторов:
Собщ=(C1*C2)/(C1+C2)
- При последовательном соединении трех и более конденсаторов:
1/Собщ=1/C1+1/C2+1/C3+…+1/Cn
-
Параллельное соединение конденсаторов
Если условно разделить выводы каждого из конденсаторов на первый и второй выводы параллельное соединение конденсаторов будет выполняется следующим образом: первые выводы всех конденсаторов соединяются в одну общую точку (условно — точка №1) вторые выводы всех конденсаторов соединяются в другую общую точку (условно — точка №2). В результате получается группа (блок) параллельно соединенных конденсаторов подключение которой к электрической цепи производится через условные точки №1 и №2.
Схема параллельного соединения конденсаторов будет иметь следующий вид:
Таким образом параллельное соединение конденсаторов будет иметь следующий вид:
При данной схеме напряжение на всех конденсаторах будет одинаково:
U=U1=U2=U3
Заряд же на каждом из конденсаторов будет зависеть от его емкости:
Q1=U*C1; Q2=U*C2; Q3=U*C3
При этом общий заряд цепи будет равен сумме зарядов всех параллельно подключенных конденсаторов:
Qобщ=Q1+Q2+Q3…+…Qn.
Рассчитать общую емкость конденсаторов при параллельном соединении можно по следующей формуле:
Собщ=C1+C2+C3+…+Cn
-
Смешанное соединение конденсаторов
Схема в которой присутствует две и более группы (блока) конденсаторов с различными схемами соединения называется схемой смешанного соединения конденсаторов.
Приведем пример такой схемы:
Для расчетов такие схемы условно разделяются на группы одинаково соединенных конденсаторов, после чего расчеты ведутся для каждой группы по формулам приведенным выше.
Для наглядности приведем пример расчета общей емкости данной схемы.
-
Пример расчета
Условно разделив схему на группы получим следующее:
Как видно из схемы на первом этапе мы выделили 3 группы (блока) конденсаторов, при этом конденсаторы в первой и второй группе соединены последовательно, а конденсаторы в третьей группе — параллельно.
Произведем расчет каждой группы:
- Группа 1 — последовательное соединение трех конденсаторов:
1/C1,2,3 = 1/C1+1/C2+1/C3 = 1/5+1/15+1/10=0,2+0,067+0,1 = 0,367 → C1,2,3 = 1/0,367 = 2,72 мкФ
- Группа 2 — последовательное соединение двух конденсаторов:
С4,5 = (C4*C5)/(C4+C5)= (20*30)/(20+30) = 600/50 = 12 мкФ
- Группа 3 — параллельное соединение трех конденсаторов:
С6,7,8 = C6+C7+C8 = 5+25+30 = 60 мкФ
В результате расчета схема упрощается:
Как видно в упрощенной схеме осталась еще одна группа из двух параллельно соединенных конденсаторов, произведем расчет ее емкости:
- Группа 4 — параллельное соединение двух групп конденсаторов:
С1,2,3,4,5 = C1,2,3+C4,5 = 2,72+12 = 14,72 мкФ
В конечном итоге получаем простую схему из двух последовательно соединенных групп конденсаторов:
Теперь можно определить общую емкость схемы:
Собщ = (C1,2,3,4,5*C6,7,8)/(C1,2,3,4,5+C6,7,8) = 14,72*60/14,72+60 = 883,2/74,72 = 11,8 мкФ
Была ли Вам полезна данная статья? Или может быть у Вас остались вопросы? Пишите в комментариях!
Не нашли на сайте ответа на интересующий Вас вопрос? Задайте его на форуме! Наши специалисты обязательно Вам ответят.
↑ Наверх