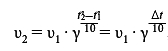При нагревании изменится плотность тела и его объем.
если пренебречь механическим воздействием нагревателя на тело таким как прилипание частичек сажи или отрывание частичек нагреваемого тела при нагреве, то можно сказать что масса тела при изменении его температуры не меняется, объем тела при нагревании увеличивается, плотность тела при нагревании уменьшается. это все верно если при изменении температуры на происходит фазовых переходов (плавление замерзание льда и тд)
Найдите правильный ответ на вопрос ✅ «Как найти массу (m) зная температуру (t) и количество теплоты (Q) ? …» по предмету 📘 Физика, а если вы сомневаетесь в правильности ответов или ответ отсутствует, то попробуйте воспользоваться умным поиском на сайте и найти ответы на похожие вопросы.
Смотреть другие ответы
Главная » Физика » Как найти массу (m) зная температуру (t) и количество теплоты (Q) ?
Плотность тела — зависимость массы и объема
Например, железный куб с ребром 10 см имеет массу 7,8 кг, алюминиевый куб тех же размеров имеет массу 2,7 кг, а масса такого же куба изо льда 0,9 кг. Величина, характеризующая массу, приходящуюся на единичный объём данного вещества, называется плотностью. Плотность равна частному от массы тела и его объёма, т.е.
ρ = m/V, где ρ (читается «ро») плотность тела, m — его масса, V объём.
В Международной системе единиц СИ плотность измеряется в килограммах на кубический метр (кг/м3); также часто используются внесистемные единицы, например, грамм на кубический сантиметр (г/см3). Очевидно, 1 кг/м3 = 0,001 г/см3. Заметим, что при нагревании веществ их плотность уменьшается или (реже) увеличивается, но это изменение так незначительно, что при расчётах им пренебрегают.
Сделаем оговорку, что плотность газов непостоянна; когда говорится о плотности какого-нибудь газа, обычно имеется ввиду его плотность при 0 градусов по Цельсию и нормальном атмосферном давлении (760 миллиметров ртутного столба).
Определение массы и плотности жидкостей
Определение массы жидкостей, кроме непосредственного взвешивании. — с известной погрешностью можно производить объемным методом — с помощью пипеток, бюреток, мерных цилиндров, колб, мензурок и т. п. по формуле:
m = Vp
где m — масса жидкости, г; V — ее объем, см3; р—плотность жидкости, г/см3.
Плотность жидкостей и растворов находят по справочным таблицам или определяют самостоятельно. В лабораторной практике наибольшее распространение получили два метода определения плотности: 1) определение степени погружения денсиметра з жидкость; 2) взвешивание жидкости в сосуде известного объема.
При определении плотности с помощью денсиметр а последний погружают в цилиндр с жидкостью, термостатированной при определенной температуре, обычно при 20 или 15 °С. (рис. 25).
Для измерения температуры жидкости используют термометр с ценой деления не менее 0,5°С: неточность в измерении температуры в 1°С дает ошибку в значении плотности до 0,1%. Шкала денсиметров проградупрозана непосредственно в единицах плотности. Значение плотности жидкости считывают по делению шкалы, находящемуся на одном уровне с мениском жидкости.
Рис. 21. Определение плотности жидкости с помощью денсиметра.
Цена деления таких денсиметров 0,001 г/см3, а весь набор охватывает интервал плотностей от 0,700 до 1,840 г/см3. Иногда удобнее пользоваться приборами, шкала которых проградуирована в единицах концентрации для растворов определенных веществ. Такие приборы принято называть ареометрами.
В тех случаях, когда количество жидкости, находящейся в распоряжении экспериментатора, слишком мало, ее плотность определяют посредством пикнометров— небольших (от 1 до 100 мл) мерных колб.
На каждый находящийся в работе пикнометр должен быть нанесен номер титановым карандашом и заведена индивидуальная карточка, в которую закосят его точную массу (взвешивают чистый сухой пикнометр вместе с пробкой на аналитических весах) и значение «водной константы». Водная константа — эта масса воды в объеме пикнометра, приведенная к массе воды при 4 °С (температура, при которой плотность воды равна 1 г/см3).
С целью определения водной константы нового пикнометра его тщательно моют и заполняют предварительно прокипяченной (для удаления растворенного воздуха) дистиллированной водой немного выше метки.
Наполненный пикнометр выдерживают в течение 20 мин в водяном термостате при 20°С, после чего с помощью капилляра или тонких полосок фильтровальной бумаги отбирают лишнюю воду, доводя ее уровень в шейке пикнометра до метки по нижнему краю мениска. Верхнюю часть шейки пикнометра и шлиф протирают досуха кусочком фильтровальной бумаги, закрывают пикнометр пробкой, тщательно вытирают его снаружи, обсушивают 20—25 мин, после чего взвешивают на аналитических весах. Вычитая из массы пикнометра с водой массу сухого пикнометра получают массу воды в объеме пикнометра при 20 °С. Частное от деления полученного значения на 0,99823 г (масса 1 мл воды при 20 °С) и есть водная константа пикнометра.
При определении плотности какой-либо жидкости проделывают тс же операции, что и при определении водной константы. Для вычисления относительной плотности вещества d массу жидкости в объеме данного пикнометра делят на величину его водной константы
К оглавлению
см. также
- Правила работы с весами
- Определение массы и плотности жидкостей
Расчет массы и объема тела
В повседневной жизни мы часто сталкиваемся с необходимостью рассчитывать массы и объёмы разных тел. Это удобно делать, применяя плотность.
Плотности разных веществ определяются по таблицам, например, плотность воды 1000 кг/м3, плотность этилового спирта 800 кг/м3.
Из определения плотности следует, что масса тела равна произведению его плотности и объёма. Объём же тела равен частному от массы и плотности. Этим пользуются при расчётах:
m = ρ * V; или V = m / p;
гдн m масса данного тела, ρ его плотность, V объём тела.
Как найти массу воды: узнай все
#1
Вода является источником жизни, одним из самых распространённых элементов в природе. Тем не менее, она остаётся самым важным соединением на планете, содержится в каждом живом организме. Кроме того, также она есть и во многих неорганических смесях и препаратах, используемых на производстве. Часто становится актуален вопрос как найти массу воды в определённой ёмкости или предмете, рассчитать её массовую долю.
#2
Массовая доля — отношение массы вещества ко всему весу тела. Например, организм человека на две трети состоит из воды, а огурец — на 90 %. Это значит, что в теле массой 75 килограммов, содержится 50 литров воды. Переходя к вопросу как перевести объём в массу, необходимо разобраться с таким понятием, как плотность вещества. Плотность является скалярной величиной и определяется как отношение веса к объёму.
#3
Также плотность определяется через количество вещества. Для этого необходимо, как рассчитать молярную массу, так и количество вещества. Рассмотрим пример: арбуз на 80% состоит из жидкости, объём арбуза 5 литров. Сколько килограммов воды в данном арбузе. Сначала вычислим объём воды в арбузе. 5 литров * 0,8 (это 80 %) = 4 литра. Теперь остаётся вычислить массу 4-х литров воды. Плотность воды составляет 1 кг/литр, следовательно 4 л * 1 кг/л = 4 кг. Ответ: 4 килограмма.
#4
Зная, как найти массу через плотность, можно вычислить не только массу воды, но и массу других веществ. Достаточно знать плотность необходимого элемента, для этого существуют специальные таблицы плотностей. Решим обратную задачу. Стальной брусок имеет массу 1 кг. Вычислить его объём. Для этого воспользуемся таблицей, установим плотность стали (7,8 кг/литр) . Далее разделим массу на объём, получим 1 (кг) / 7,8 (кг/литр) = 0,8 литра.
#5
Также может возникнуть задача, как найти массу, зная объем неоднородного вещества. Решим такую задачу. Трёхлитровую ёмкость полностью наполнили водой и ацетоном в соотношении 3 к 1. Вычислить массу полученной смеси, массой ёмкости пренебречь. Для начала, выясним какой объём воды и ацетона. Если соотношение было 3 к 1, то необходимо разделить всю ёмкость на 3+1 = 4 части. 3 литра / 4 = 0,5 литра приходится на одну часть.
#6
Следовательно, воды будет 3 * 0,5 = 2,5 литра, а ацетона 1*0,5 = 0,5 литра. Теперь можно приступить к вычислению масс. Плотность воды нам уже известна (1 кг/литр) , плотность ацетона, согласно таблице равна 0,8 кг/литр. Далее вычисляем массу воды: 2,5 литра * 1 кг/литр = 2,5 кг; и ацетона: 0.5 литра * 0,8 кг/литр = 0,6 кг. Сложим полученные результаты: 2,5 + 0,6 = 2.5 килограммов. Задаче решена.
Рассмотрим более сложный пример расчета
Слиток из двух металлов с плотностями ρ1 и ρ2 , имеет массу m и объём V. Определить объём этих металлов в слитке.
Решение. Пусть V1 объём первого металла, V2 объём второго металла. Тогда V1 + V2 = V; V1 = V V2; ρ1V1 + p2V2 = ρ1V1 + ρ2 (V V1) = m
Решив это уравнение относительно V1 , получаем:
V1= (m ρ2V)/(ρ1 ρ2)
Теперь найдём V2:
V2= V — (m ρ2V)/(ρ1 ρ2)
Ответ: объём первого тела равен (m ρ2V)/(ρ1 ρ2), второго V — (m ρ2V)/( ρ1 ρ2). Заметим, однако, что при ρ1 = ρ2 задача не имеет однозначного решения.
Формула зависимости массы от объема и плотности
Для того, чтобы найти плотность жидкости или твердого вещества, существует базовая формула: плотность равна массе, поделенной на объем.
Записывается это так:
И из нее можно вывести еще две формулы.
Формулу для объема тела:
А также формулу для расчета массы:
Как видите, запомнить последнюю очень легко: это единственная формула, где две единицы нужно умножить.
Для запоминания этой зависимости можно использовать рисунок в виде «пирамидки», разделенной на три секции, в вершине которой находится масса, а в нижних углах – плотность и объем.
Несколько иначе обстоят дела с газами.
Рассчитать их вес гораздо сложнее, так как у газов нет постоянной плотности: они рассеиваются и занимают весь доступный им объем.
Для этого пригодится понятие молярной массы, которую можно найти, сложив массу всех атомов в формуле вещества при помощи данных из периодической таблицы.
Вторая единица, которая нам понадобится – количество вещества в молях. Его можно вычислить по уравнению реакции. Подробнее об этом можно узнать в рамках курса химии.
Другой способ нахождения мольного количества – через объем газа, который нужно поделить на 22,4 литра. Последнее число – это объемная постоянная, которую стоит запомнить.
В итоге, зная две предыдущие величины, мы можем определить массу газа:
где M – это молярная масса, а n – количество вещества.
Результат получится в граммах, поэтому для решения физических задач важно не забыть перевести его в килограммы, поделив на 1000. Числа в этой формуле часто могут оказываться достаточно сложными, поэтому для вычислений может понадобиться калькулятор.
Еще один нестандартный случай, с которым можно столкнуться – необходимость найти плотность раствора
. Для этого существует формула средней плотности, построенная аналогично формулам других средних величин.
Для двух веществ посчитать ее можно так:
Также из этой формулы можно вывести несколько других в зависимости от того, какие из величин известны по условию задачи.
Формула зависимости массы от объема и плотности
Для того, чтобы найти плотность жидкости или твердого вещества, существует базовая формула: плотность равна массе, поделенной на объем.
Записывается это так:
И из нее можно вывести еще две формулы.
Формулу для объема тела:
А также формулу для расчета массы:
Как видите, запомнить последнюю очень легко: это единственная формула, где две единицы нужно умножить.
Для запоминания этой зависимости можно использовать рисунок в виде «пирамидки», разделенной на три секции, в вершине которой находится масса, а в нижних углах – плотность и объем.
Несколько иначе обстоят дела с газами.
Рассчитать их вес гораздо сложнее, так как у газов нет постоянной плотности: они рассеиваются и занимают весь доступный им объем.
Вес делить на плотность
Письмо с инструкцией по восстановлению пароля будет отправлено на вашу почту
В этом уроке мы изучим, как можно определить массу и объем тела, если известна плотность вещества.
Плотность – скалярная физическая величина, показывающая, чему равна масса вещества, взятого в объеме 1 м3, и равная отношению массы тела к его объему: p = m : v.
Из формулы плотности следует, что масса тела равна произведению плотности вещества на объем этого тела: m = ρ · V.
Чтобы вычислить объем тела, нужно массу тела разделить на его плотность: v = m : p.
Для правильного решения задач нужно уметь верно переводить единицы измерения величин в Международную систему единиц: 1 г = 0,001 кг, 1 л = 1 дм3 = 0,001 м3, 1 см3 = 0,000 001 м3, 1 г/см3 = 1000 кг/м3.
Какова масса подсолнечного масла в бутылке объемом 3 л, если плотность масла равна 930 кг/м3?
Запишем условие задачи. Нам известны объем бутылки (обозначается буквой V) 3 л, и плотность подсолнечного масла (обозначается буквой ρ) 930 кг/м3. Выразим объем бутылки в Международной системе единиц. 1 л = 0,001 м3, следовательно, 3 л составляют 0,003 м3.
Решение: Чтобы найти массу тела, нужно плотность умножить на объем: m = ρ · V. Подставим числовые значения величин: 930 кг/м3 · 0,003 м3 = 2,79 кг.
Сколько штук строительного кирпича размером 250 мм х 120 мм х 65 мм допускается перевозить на автомашине грузоподъемностью 4 т? Плотность кирпича 1800 кг/м3.
Запишем условие задачи и выразим данные в Международной системе единиц. Известны размеры кирпича: длина а = 250 мм = 0,25 м, ширина b= 120 мм = 0,12 м, высота с = 60 мм = 0,06 м, плотность кирпича ρ = 1800 кг/м3, грузоподъемность – наибольшая масса груза, которую может перевезти автомобиль – m = 4 т = 4000 кг. Найти количество кирпичей – обозначим латинской буквой N.
Как найти массу по термохимическому уравнению
Алгоритм 8
Расчеты по термохимическим уравнениям. Вычисление массы вещества по известному количеству теплоты
Пример. По термохимическому уравнению
С + О2 = СО2 + 412 кДж вычислите массу сгоревшего угля, если количество теплоты, выделившееся в результате реакции, составляет 82,4 кДж.
С помощью соответствующих обозначений запишем условие задачи, найдем молярную массу вещества, о котором идет речь в условии задачи
Запишем термохимическое уравнение реакции. Обозначим вопросительным знаком количество вещества, массу которого надо
найти, и надпишем количество теплоты, записанное в условии задачи. Под формулой вещества обозначим молярное соотношение, вытекающее из уравнения реакции. Вычислим количество вещества, массу которого требуется найти.
Решение:
Для этого составим пропорцию
х/1=82,4/412, откуда х= 0,2.
Следовательно, n(С)=0,2 моль
Перейдем от количества вещества к массе вещества. Для этого используем молярную массу вещества
химэко
Меню сайта
Категории каталога
| 8 класс [27] |
| 9 класс [16] |
| 10 класс [30] |
| 11 класс [5] |
| Экзамен [4] |
| Лаборатория [7] |
| Опорные конспекты [0] |
| Переменка [6] |
| НОТ школьника [9] |
| Решение задач [9] |
| Творческие работы учащихся [3] |
| Учебные пособия [5] |
Форма входа
Приветствую Вас Гость!
Поиск
Друзья сайта
Наш опрос
Статистика
Термохимические уравнения включают в себя кроме химических формул тепловой эффект реакции. Числовое значение в уравнении реакции строго соответствует количествам веществ, участников реакции, т.е. коэффициентам. Благодаря этому соответствию, можно установить пропорциональные отношения между количеством вещества или массой и количеством теплоты в этой реакции.
Например: Термохимическое уравнение разложения малахита
Мы видим, что на разложение 1 моля малахита необходимо израсходовать 47 кДж, при этом образуется 2 моля оксида меди, 1 моль воды и 1 моль углекислого газа. Если мы затратим энергии в 2 раза больше, мы сумеем разложить 2 моля малахита, при этом получим 4 моля оксида меди, 2 моля воды и 2 моля углекислого газа.
Аналогично можно установить пропорциональные отношения, используя коэффициенты и молярные массы участников реакции. 47 кДж энергии затратится на разложение 94 г малахита, при этом выделится 160 г оксида меди, 18 г воды и 44 г углекислого газа. Пропорция несложная, но, используя массовые числа, учащиеся часто допускают расчетные ошибки, поэтому я рекомендую решать задачи с пропорциями через количество вещества.
Задача 1. Определите количество теплоты, которое выделится при образовании 120 г MgO в результате реакции горения магния, с помощью термохимического уравнения.
2 Mq + O 2 = 2 MqO + 1204 кДж
1) Определяем количества оксида магния, используя формулу для нахождения количества вещества через массу.
n ( MqO ) = 120г/ 40 г/моль = 3 моль
2) Составляем пропорцию с учетом коэффициентов в уравнении реакции
Расчёты по термохимическим уравнениям
Теоретический материал представлен на страницах:
Любая химическая реакция сопровождается поглощением или выделением энергии. Термохимические уравнения показывают соотношение между кол-вом веществ, вступающих в реакцию, и кол-вом энергии, которую выделяют, либо поглощают эти вещества в процессе химической реакции.
Главное отличие термохимического уравнения от молекулярного заключается в том, что кроме формул и коэффициентов, в нем указывается еще и кол-во энергии (теплоты реакции), относящееся к числу молей реагирующих веществ, соответствующему коэффициентам в уравнении реакции.
Теплота реакции (тепловой эффект) обозначается буквой Q (измеряется в кДж), и записывается в конце уравнения. Знак «плюс» перед числом обозначает выделившееся кол-во энергии, знак «минус» — кол-во поглощенной энергии.
Реакции, протекающие с выделением энергии, называются экзотермическими; с поглощением энергии — эндотермическими.
Если известна масса одного из двух реагирующих веществ, на основе термохимического уравнения можно определить кол-во теплоты реакции.
Пример 1 . Определить теплоту реакции горения 320 г серы.
- Согласно уравнения реакции, при сгорании 1 моля серы выделяется 297 кДж энергии, нам надо узнать, сколько энергии выделится при сгорании 320 г серы.
- Для решения задачи необходимо составить и решить простую пропорцию:
- Переходим от молей к граммам:
- В пропорции заменяем моли на граммы:
Если известно кол-во выделенной (поглощенной) теплоты в ходе реакции, можно определить массы прореагировавших веществ.
Пример 2 . Определить кол-во сгоревшего угля, если в ходе горения было выделено 33520 кДж энергии.
- Согласно уравнения реакции, при сгорании 1 моль углерода (масса 1 моль С = 12 г) выделилсь 402,24 кДж энергии.
- Составляем и решаем пропорцию:
Пример 3 . При горении 1 л метана (н.у) выделяется 39 кДж энергии. Составить термохимическое уравнение реакции и вычислить тепловой эффект.
Пример 4 . При горении 2,4 г магния (н.у) выделяется 60,12 кДж энергии. Составить термохимическое уравнение реакции.
Пример 5 . Два моля аммиака образуются в результате взаимодействия 1 моля азота с тремя молями водорода. Необходимо составить уравнение термохимической реакции, в ходе которой выделяется 92 кДж тепла, а все вещества, участвующие в реакции, являются газами.
Это очень простая задача, решение которой указано в условии.
Второй вариант записи термохимического уравнения.
Пример 6 . Составить термохимическое уравнение эндотермической реакции образования двухвалентного оксида азота из азота и кислорода с поглощением 180 кДж энергии. Записать это уравнение для образования 1 моля NO.
Первая часть задания не вызывает трудностей:
В этом термохимическом уравнении 2 моля оксида азота образуется при взаимодействии 1 моля азота и 1 моля кислорода. Для того, чтобы переписать данное уравнение для 1 моля оксида азота, необходимо все коэффициенты и кол-во теплоты разделить на 2:
Пример 7 . При образовании 50 г карбоната кальция (CaCO3) выделилось 80 кДж энергии. Определить тепловой эффект реакции разложения одного моля карбоната кальция.
- Определяем кол-во энергии, выделяемое при образовании 1 моля CaCO3 (М(CaCO3)=100 г/моль):
- Термохимическое уравнение реакции образования 1 моль карбоната кальция имеет вид:
- Термохимическое уравнение реакции разложения 1 моль карбоната кальция имеет вид:
- Q=-160 кДж
Пример 8 . Рассчитать кол-во выделенной энергии при образовании 2 л аммиака при н.у.
- Согласно термохимического уравнения — 1 моль аммиака образовался из полумоля азота и полутора молей водорода. Составляем пропорцию:
Пример 9 . Рассчитать тепловой эффект реакции:
- На основании первого следствия из закона Гесса:
- Теплоты образования простых веществ равны нулю:
- Теплоты образования сложных веществ берем из таблицы:
- Подставляем числовые значения в уравнение:
- Термохимическое уравнение реакции будет иметь вид:
Пример 10 . Рассчитать тепловой эффект реакции:
- Тепловой эффект реакции будем рассчитывать по формуле, вытекающей из второго следствия закона Гесса:
- Тепловые эффекты сгорания C2H4 и C2H6 можно взять из приведенных выше термохимический уравнений.
- Тепловой эффект сгорания водорода можно вычислить из термохимического уравнения образования 1 моля воды (теплоту образования воды берем из таблицы):
- Подставляем численные значения в формулу:
- Термохимическое уравнение реакции будет иметь вид:
Пример 11 . Определить скорость изменения реакции синтеза аммиака при а) увеличении концентрации исходных веществ в 2 раза; б) уменьшении давления в реакционной смеси в 2 раза:
- Записываем кинетическое уравнение данной реакции:
- Если концентрации исходных веществ будут увеличены в 2 раза, кинетическое уравнение примет вид:
- Составляем отношение и решаем его:
- Увеличение концентрации исходных веществ в 2 раза приведет к ускорению скорости реакции в 16 раз.
- Исходя из того факта, что концентрации газов пропорциональны давлению (при уменьшении давления в 2 раза концентрации также уменьшатся в 2 раза), логично предположить, что при снижении в 2 раза давления скорость протекания реакции снизится в 16 раз. Убедимся в этом, составив соотношение кинетических уравнений.
- Исхдное кинетическое уравнение:
- Для удобства чтения формул сделаем подстановку:
- Кинетическое уравнение при снижении давления в 2 раза:
- Соотошение:
- При уменьшении давления в реакционной смеси в 2 раза скорость протекания реакции уменьшится в 16 раз.
Пример 12 . Определить скорость изменения реакции с температурным коэффициентом 4 (γ=4) при повышении температуры с 10°C до 30°C.
Для решения задачи воспользуемся правилом Вант-Гоффа, которое выражается следующей математической формулой:
Все, что нам нужно сделать — подставить численные значения в формулу и провести расчеты:
При повышении температуры с 10 до 30 градусов Цельсия скорость реакции увеличится в 16 раз.
Если вам понравился сайт, будем благодарны за его популяризацию 🙂 Расскажите о нас друзьям на форуме, в блоге, сообществе. Это наша кнопочка:
Код кнопки: 
Политика конфиденциальности Об авторе
источники:
http://himekoscho.ucoz.ru/load/termokhimicheskie_uravnenija/27-1-0-130
http://prosto-o-slognom.ru/chimia_primery/005-termochimicheskie_uravneniya.html
Wiki-учебник
Поиск по сайту
Реклама от партнёров:
Расчет массы и объема тела по его плотности
Масса любого тела зависит не только от его размеров, но и от вещества, из которого тело состоит. Так, тела одного объёма, сделанные из разных веществ, имеют разные массы, и обратно: тела, имеющие одинаковые массы, сделанные из разных веществ, имеют разные объёмы.
Плотность тела — зависимость массы и объема
Например, железный куб с ребром 10 см имеет массу 7,8 кг, алюминиевый куб тех же размеров имеет массу 2,7 кг, а масса такого же куба изо льда 0,9 кг. Величина, характеризующая массу, приходящуюся на единичный объём данного вещества, называется плотностью. Плотность равна частному от массы тела и его объёма, т.е.
ρ = m/V, где ρ (читается «ро») плотность тела, m — его масса, V объём.
В Международной системе единиц СИ плотность измеряется в килограммах на кубический метр (кг/м3); также часто используются внесистемные единицы, например, грамм на кубический сантиметр (г/см3). Очевидно, 1 кг/м3 = 0,001 г/см3. Заметим, что при нагревании веществ их плотность уменьшается или (реже) увеличивается, но это изменение так незначительно, что при расчётах им пренебрегают.
Сделаем оговорку, что плотность газов непостоянна; когда говорится о плотности какого-нибудь газа, обычно имеется ввиду его плотность при 0 градусов по Цельсию и нормальном атмосферном давлении (760 миллиметров ртутного столба).
Расчет массы и объема тела
В повседневной жизни мы часто сталкиваемся с необходимостью рассчитывать массы и объёмы разных тел. Это удобно делать, применяя плотность.
Плотности разных веществ определяются по таблицам, например, плотность воды 1000 кг/м3, плотность этилового спирта 800 кг/м3.
Из определения плотности следует, что масса тела равна произведению его плотности и объёма. Объём же тела равен частному от массы и плотности. Этим пользуются при расчётах:
m = ρ * V; или V = m / p;
гдн m масса данного тела, ρ его плотность, V объём тела.
Рассмотрим пример такого расчета
Пустой стакан имеет массу m1=200 г. Если налить в него воды, его масса будет m2= 400 г. Какую массу будет иметь этот стакан, если налить столько же (по объёму) ртути?
Решение. Найдём массу налитой воды. Она будет равна разности массы стакана с водой и массы пустого стакана:
mводы = m2- m1 = 400 г 200 г = 200 г.
Найдём объём этой воды:
V = m / ρв = 200 г / 1 г/см3 = 200 см3 (рв плотность воды).
Найдём массу ртути в этом объёме:
mрт = ρртV = 13,6 г/см3 * * 200 см3 = 2720 г.
Найдём искомую массу:
m = mрт + m1 = 2720 г + 200 г = 2920 г.
Ответ: масса стакана с ртутью равна 2920 граммам.
Рассмотрим более сложный пример расчета
Слиток из двух металлов с плотностями ρ1 и ρ2 , имеет массу m и объём V. Определить объём этих металлов в слитке.
Решение. Пусть V1 объём первого металла, V2 объём второго металла. Тогда V1 + V2 = V; V1 = V V2; ρ1V1 + p2V2 = ρ1V1 + ρ2 (V V1) = m
Решив это уравнение относительно V1 , получаем:
V1= (m ρ2V)/(ρ1 ρ2)
Теперь найдём V2:
V2= V — (m ρ2V)/(ρ1 ρ2)
Ответ: объём первого тела равен (m ρ2V)/(ρ1 ρ2), второго V — (m ρ2V)/( ρ1 ρ2). Заметим, однако, что при ρ1 = ρ2 задача не имеет однозначного решения.
Нужна помощь в учебе?
Предыдущая тема: Плотность вещества: формула, расчет
Следующая тема: Сила: явление тяготения и сила тяжести
| Нравится | Нравится |