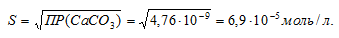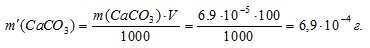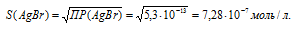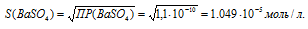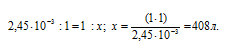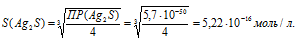- Формула: CCaO3 или CaCO3
- Относительная молекулярная масса CCaO3: 100.0869
- Молярная масса CCaO3: 100.0869 г/моль (0.10009 кг/моль)
| Элемент | Всего атомов | Атомная масса, а.е.м. | Общая масса атомов, а.е.м. |
|---|---|---|---|
| C (углерод) | 1 | 12.0107 | 12.0107 |
| Ca (кальций) | 1 | 40.078 | 40.078 |
| O (кислород) | 3 | 15.9994 | 47.9982 |
| 100.0869 |
Расчёт молярной и относительной молекулярной массы CCaO3
- Mr[CCaO3] = Ar[C] + Ar[Ca] + Ar[O] * 3 = 12.0107 + 40.078 + 15.9994 * 3 = 100.0869
- Молярная масса (в кг/моль) = Mr[CCaO3] : 1000 = 100.0869 : 1000 = 0.10009 кг/моль
Расчёт массовых долей элементов в CCaO3
- Массовая доля углерода (C) = 12.0107 : 100.0869 * 100 = 12 %
- Массовая доля кальция (Ca) = 40.078 : 100.0869 * 100 = 40.043 %
- Массовая доля кислорода (O) = 47.9982 : 100.0869 * 100 = 47.957 %
Калькулятор массы
Не уверен в ответе?
Найди верный ответ на вопрос ✅ «Вычислить молярную массу вещества CaCo3 …» по предмету 📙 Химия, а если ответа нет или никто не дал верного ответа, то воспользуйся поиском и попробуй найти ответ среди похожих вопросов.
Искать другие ответы
Вычисление молярной массы
To calculate molar mass of a chemical compound enter its formula and click ‘Compute’. В химической формуле, вы можете использовать:
- Любой химический элемент. Capitalize the first letter in chemical symbol and use lower case for the remaining letters: Ca, Fe, Mg, Mn, S, O, H, C, N, Na, K, Cl, Al.
- Функциональные группы:D, Ph, Me, Et, Bu, AcAc, For, Ts, Tos, Bz, TMS, tBu, Bzl, Bn, Dmg
- круглые () и квадратные [] скобки.
- Общие составные имена.
Примеры расчета молярной массы:
NaCl,
Ca(OH)2,
K4[Fe(CN)6],
CuSO4*5H2O,
water,
nitric acid,
potassium permanganate,
ethanol,
fructose.
Molar mass calculator also displays common compound name, Hill formula, elemental composition, mass percent composition, atomic percent compositions and allows to convert from weight to number of moles and vice versa.
Вычисление молекулярной массы (молекулярная масса)
Для того, чтобы рассчитать молекулярную массу химического соединения, введите её формулу, указав его количество массы изотопа после каждого элемента в квадратных скобках.
Примеры молекулярные вычисления веса:
C[14]O[16]2,
S[34]O[16]2.
Определение молекулярной массы, молекулярный вес, молекулярная масса и молярная масса
- Молекулярная масса ( молекулярной массой ) это масса одной молекулы вещества, выражающаяся в атомных единицах массы (и). (1 и равна 1/12 массы одного атома углерода-12)
- Молярная масса ( молекулярной массой ) является масса одного моля вещества и выражается в г / моль.
Массы атомов и изотопов с NIST статью .
См. также: молекулярные массы аминокислот
Решение задач по хими на вычисления с использованием значения произведения растворимости соли
Задача 563.
Исходя из произведения растворимости карбоната кальция, найти массу СаСО3, содержащуюся в 100 мл его насыщенного раствора.
Решение:
ПР(СаСО3) = 4,76 . 10-9.
Обозначим искомую растворимость соли СаСО3 через S моль/л. Тогда в насыщенном растворе соли содержится по S моль/л ионов Ca2+ и CO32-.
Выражение произведения растворимости карбоната кальция можно записать как:
ПР(СаСО3) = [Ca2+] . [CO32-] = S . S = S2.
Отсюда
Теперь рассчитаем массу СаСО3 в 1 л насыщенного раствора его:
m(СаСО3) = S . M(СаСО3) = (6,9 . 10-5) . 100 = 6,9 . 10-2.
Находим массу СаСО3 в 100 мл насыщенного раствора его:
Ответ: 6,9 . 10-4 г.
Задача 564.
Найти массу серебра, находящегося в виде ионов в 1 л насыщенного раствора АgВг.
Решение:
ПР(АgВг) = 5,3 . 10-13.
Обозначим искомую растворимость соли АgВг. через S моль/л. Тогда в насыщенном растворе соли содержится по S моль/л ионов Ag+ и Br—.
Выражение произведения растворимости бромида серебра можно записать как:
ПР(AgBr = = [Ag+] . [Br—] = S . S = S2.
Отсюда
Рассчитаем массу АgВг в 1л раствора, учитывая, что M(Ag+) = 107,688 г/моль, получим:
m(Ag+) = S . M(Ag+) = (7,28 . 10-7) . 107,688 = 7,85 . 10-5 г.
Ответ: 7,85 . 10-5 г.
Задача 565.
Вычислить объем воды, необходимый для растворения при 25°С 1 г ВаSO4.
Решение:
ПР(ВаSO4) = 1 . 10-10.
Уравнение диссоциации ВаSO4 имеет вид:
ВаSO4 ⇔ Ba2+ + SO42-.
Обозначим искомую растворимость соли ВаSO4 через S моль/л. Тогда в насыщенном растворе соли содержится по S моль/л ионов Ba2+ и SO42-.
Выражение произведения растворимости сульфата бария можно записать как:
ПР(AgBr) = [Ba2+] . [SO42-] = S . S = S2.
Отсюда
Рассчитаем массу ВаSO4 в 1л раствора, учитывая, что M(ВаSO4) = 233,39 г/моль, получим:
m(ВаSO4) = S . M(ВаSO4) = (1,049 . 10-5) . 233,39 = 2,45 . 10-3 г.
Находим объём воды, в котором растворится 1 г ВаSO4 для получения насыщенного раствора его из пропорции:
Ответ: 408 л.
Задача 566.
В каком объеме насыщенного раствора Ag2S содержится 1 мг растворенной соли?
Решение:
M(Ag2S) = 247,796 г/моль.
Обозначим искомую растворимость соли Ag2S через S моль/л. Тогда в насыщенном растворе соли содержится 2S моль ионов Ag+ и 1 моль ионов S2-.
Выражение произведения растворимости сульфида серебра можно записать как
ПР(Ag2S) = [Ag+]2 . [S2-] = 2S2 . S = 4S3.
Отсюда
Рассчитаем массу Ag2S в 1л раствора, учитывая, что M(Ag2S) = 247,796 г/моль, получим:
m(Ag2S) = S . M(Ag2S) = (5,22 . 10-16) . 247,796 = 1,3 . 1013 г или 1,3 . 1010 мг.
Находим объём воды, в котором можно растворить 1 мг сульфида серебра из пропорции:
Ответ: 7,69 . 10-11 л.
Ответ оставил Гость
Дано:
m(СаСО3) = 10кг
W(пр.)= 15%
Найти: m(СаСО3)
Решение
находим массу чистого СаСО3
примем всю массу СаСО3 за 100%
тогда чистого СаСО3 будет 100% — 15% =85%
составим пропорцию:
10кг(СаСО3) ——- 100%
Хкг———— 85%
Х= 8,5кг(СаСО3)
второй способ:
по формуле W(пр.) =m(пр.)*100%/m(СаСО3) отсюда находим
m(пр.) = W(пр.)*m(СаСО3) /100% = 1,5кг
находим массу чистого СаСО3 = 10кг- 1,5кг = 8,5кг
Ответ: масса чистой соли СаСО3 равна 8,5кг
Оцени ответ