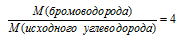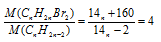Алкины – это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна тройная связь между атомами углерода С≡С.
Остановимся на свойствах, способах получения и особенностях строения алкинов.
Строение, изомерия и гомологический ряд алкинов
Химические свойства алкинов
Получение алкинов
Гомологический ряд алкинов
Все алкины имеют общие или похожие физические и химические свойства. Схожие по строению алкины, которые отличаются на одну или несколько групп –СН2–, называют гомологами. Такие алкины образуют гомологический ряд.
Первый представитель гомологического ряда алкенов – этин (ацетилен) C2H2, или СH≡СH.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь.
| Название алкина | Формула алкина |
| Этин (ацетилен) | C2H2 |
| Пропин | C3H4 |
| Бутин | C4H6 |
| Пентин | C5H8 |
| Гексин | C6H10 |
| Гептин | C7H12 |
Общая формула гомологического ряда алкинов CnH2n-2.
Первые три члена гомологического ряда алкинов – газы, начиная с C5Н8 по С16Н30 – жидкости, начиная с С17Н32 — твердые вещества.
Алкины плохо растворимы в воде и хорошо растворимы в органических растворителях.
Строение алкинов
Рассмотрим особенности строения алкинов на примере ацетилена.
В молекуле ацетилена присутствуют химические связи C–H и С≡С.
Связь C–H ковалентная слабополярная одинарная σ-связь. Связь С≡С – тройная, ковалентная неполярная, одна из связей σ, еще две: π-связи. Атомы углерода при тройной связи образуют по две σ-связи и две π-связи. Следовательно, гибридизация атомов углерода при тройной связи в молекулах алкинов – sp:
При образовании σ-связи между атомами углерода происходит перекрывание sp-гибридных орбиталей атомов углерода:
При образовании π-связи между атомами углерода происходит перекрывание негибридных орбиталей атомов углерода:
Две sp-гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому две гибридные орбитали атомов углерода при тройной связи в алкинах направлены в пространстве под углом 180о друг к другу:
Изображение с сайта orgchem.ru
Это соответствует линейному строению молекулы.
Например, молекуле ацетилена C2H2 соответствует линейное строение.
Изображение с сайта orgchem.ru
Молекулам алкинов с большим числом атомов углерода соответствует пространственное строение.
Например, в молекуле пропина присутствует атом углерода в sp3-гибридном состоянии, в составе метильного фрагмента СН3. Такой фрагмент имеет тетраэдрическое строение.
Изомерия алкинов
Для алкинов характерна структурная и пространственная изомерия.
Структурная изомерия
Для алкинов характерна изомерия углеродного скелета, изомерия положения кратной связи и межклассовая изомерия.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета отличаются строением углеродного скелета.
Изомеры с различным углеродным скелетом и с формулой С4Н6 — бутин-1 и бутадиен-1,3
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Алкины являются межклассовыми изомерами с алкадиенами. Общая формула алкинов и алкадиенов — CnH2n-2.
Межклассовые изомеры с общей формулой С4Н6 — бутин-1 и бутадиен
Изомеры с различным положением тройной связи отличаются положением тройной связи в углеродном скелете.
Изомеры положения тройной связи, которые соответствуют формуле С5Н8 — пентин-1 и пентин-2
Пространственная изомерия
Для алкенов также характерна оптическая изомерия.
Алкины, которые обладают достаточно большим углеродным скелетом, могут существовать в виде оптических изомеров. В молекуле алкина должен присутствовать асимметрический атом углерода (атом углерода, связанный с четырьмя различными заместителями).
Цис-транс-изомерия для алкинов не характерна, так как по тройной связи вращение возможно.
Номенклатура алкинов
В названиях алкинов для обозначения тройной связи используется суффикс -ИН.
Например, алкин на рисунке называется бутин-2
Для простейших алкинов применяются также исторически сложившиеся (тривиальные) названия:
| Название алкина | Формула алкина |
| Ацетилен | CH≡CH |
| Пропин | CH≡C−CH3 |
| Бутин-1 | CH≡C−СH2−CH3 |
Радикалы, содержащие тройную связь, также носят тривиальные названия:
| Формула радикала | Тривиальное название |
| CH≡C− | этинил |
| CH≡C−CH2− | пропаргил |
Химические свойства алкинов
Алкины – непредельные углеводороды, в молекулах которых есть одна тройная связь. Строение и свойства тройной связи определяют характерные химические свойства алкинов. Химические свойства алкинов схожи с химическими свойствами алкенов из-за наличия кратной связи в молекуле.
Для алкинов характерны реакции окисления. Окисление алкинов протекает преимущественно по тройной связи, хотя возможно и жесткое окисление (горение).
1. Реакции присоединения
Тройная связь состоит из σ-связи и двух π-связей. Сравним характеристики одинарной связи С–С, тройной связи С≡С и связи С–Н:
| Энергия связи, кДж/моль | Длина связи, нм | |
| С–С | 348 | 0,154 |
| С≡С | 814 | 0,120 |
| С–Н | 435 | 0,107 |
Таким образом, тройная связь С≡С короче, чем одинарная связь С–С, поэтому π-электроны тройной связи прочнее удерживаются ядрами атомов углерода и обладают меньшей поляризуемостью и подвижностью. Реакции присоединения по тройной связи к алкинам протекают сложнее, чем реакции присоединения по двойной связи к алкенам.
Для алкинов характерны реакции присоединения по тройной связи С≡С с разрывом π-связей.
1.1. Гидрирование
Гидрирование алкинов протекает в присутствии катализаторов (Ni, Pt) с образованием алкенов, а затем сразу алканов.
Например, при гидрировании бутина-2 в присутствии никеля образуется сначала бутен-2, а затем бутан.
При использовании менее активного катализатора (Pd, СaCO3, Pb(CH3COO)2) гидрирование останавливается на этапе образования алкенов.
Например, при гидрировании бутина-1 в присутствии палладия преимущественно образуется бутен-1.
1.2. Галогенирование алкинов
Присоединение галогенов к алкинам происходит даже при комнатной температуре в растворе (растворители — вода, CCl4).
При взаимодействии с алкинами красно-бурый раствор брома в воде (бромная вода) обесцвечивается. Это качественная реакция на тройную связь.
Например, при бромировании пропина сначала образуется 1,2-дибромпропен, а затем — 1,1,2,2-тетрабромпропан.
Аналогично алкины реагируют с хлором, но обесцвечивания хлорной воды при этом не происходит, потому что хлорная вода и так бесцветная)
Реакции протекают в присутствии полярных растворителей по ионному (электрофильному) механизму.
1.3. Гидрогалогенирование алкинов
Алкины присоединяют галогеноводороды. Реакция протекает по механизму электрофильного присоединения с образованием галогенопроизводного алкена или дигалогеналкана.
Например, при взаимодействии ацетилена с хлороводородом образуется хлорэтен, а затем 1,1-дихлорэтан.
При присоединении галогеноводородов и других полярных молекул к симметричным алкинам образуется, как правило, один продукт реакции, где оба галогена находятся у одного атома С.
При присоединении полярных молекул к несимметричным алкинам образуется смесь изомеров. При этом выполняется правило Марковникова.
Правило Марковникова: при присоединении полярных молекул типа НХ к несимметричным алкинам водород преимущественно присоединяется к наиболее гидрогенизированному атому углерода при двойной связи.
Например, при присоединении хлороводорода HCl к пропину преимущественно образуется 2-хлорпропен.
1.4. Гидратация алкинов
Гидратация (присоединение воды) алкинов протекает в присутствии кислоты и катализатора (соли ртути II).
Сначала образуется неустойчивый алкеновый спирт, который затем изомеризуется в альдегид или кетон.
Например, при взаимодействии ацетилена с водой в присутствии сульфата ртути образуется уксусный альдегид.
Гидратация алкинов протекает по ионному (электрофильному) механизму.
Для несимметричных алкенов присоединение воды преимущественно по правилу Марковникова.
Например, при гидратации пропина образуется пропанон (ацентон).
1.5. Димеризация, тримеризация и полимеризация
Присоединение одной молекулы ацетилена к другой (димеризация) протекает под действием аммиачного раствора хлорида меди (I). При этом образуется винилацетилен:
Тримеризация ацетилена (присоединение трех молекул друг к другу) протекает под действием температуры, давления и в присутствии активированного угля с образованием бензола (реакция Зелинского):
Алкины также вступают в реакции полимеризации — процесс многократного соединения молекул низкомолекулярного вещества (мономера) друг с другом с образованием высокомолекулярного вещества (полимера).
nM → Mn (M – это молекула мономера)
Например, при полимеризации ацетилена образуется полимер линейного или циклического строения.
… –CH=CH–CH=CH–CH=CH–…
2. Окисление алкинов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
2.1. Горение алкинов
Алкины, как и прочие углеводороды, горят с образованием углекислого газа и воды.
Уравнение сгорания алкинов в общем виде:
CnH2n-2 + (3n-1)/2O2 → nCO2 + (n-1)H2O + Q
Например, уравнение сгорания пропина:
C3H4 + 4O2 → 3CO2 + 2H2O
2.2. Окисление алкинов сильными окислителями
Алкины реагируют с сильными окислителями (перманганаты или соединения хрома (VI)). При этом происходит окисление тройной связи С≡С и связей С-Н у атомов углерода при тройной связи. При этом образуются связи с кислородом.
При окислении трех связей у атома углерода в кислой среде образуется карбоксильная группа СООН, четырех — углекислый газ СО2. В нейтральной среде — соль карбоновой кислоты и карбонат (гидрокарбонат) соответственно.
Таблица соответствия окисляемого фрагмента молекулы и продукта:
| Окисляемый фрагмент | KMnO4, кислая среда | KMnO4, H2O, t |
| R-C≡ | R-COOH | -COOMe |
| CH≡ | CO2 | Me2CO3 (MeHCO3) |
При окислении бутина-2 перманганатом калия в среде серной кислоты окислению подвергаются два фрагмента СН3–C≡, поэтому образуется уксусная кислота:
При окислении 3-метилпентина-1 перманганатом калия в серной кислоте окислению подвергаются фрагменты R–C и H–C , поэтому образуются карбоновая кислота и углекислый газ:
При окислении алкинов сильными окислителями в нейтральной среде углеродсодержащие продукты реакции жесткого окисления (кислота, углекислый газ) могут реагировать с образующейся в растворе щелочью в соотношении, которое определяется электронным балансом с образованием соответствующих солей.
Например, при окислении бутина-2 перманганатом калия в воде при нагревании окислению подвергаются два фрагмента R–C≡, поэтому образуется соль уксусной кислоты – ацетат калия
Аналогичные органические продукты образуются при взаимодействии алкинов с хроматами или дихроматами.
Окисление ацетилена протекает немного иначе, σ-связь С–С не разрывается, поэтому в кислой среде образуется щавелевая кислота:
В нейтральной среде образуется соль щавелевой кислоты – оксалат калия:
Обесцвечивание раствора перманганата калия — качественная реакция на тройную связь.
3. Кислотные свойства алкинов
Связь атома углерода при тройной связи (атома углерода в sp-гибридизованном состоянии) с водородом значительно более полярная. чем связь С–Н атома углерода при двойной или одинарной связи (в sp2 и sp3-гибридном состоянии соответственно). Это обусловлено большим вкладом s-орбитали в гибридизованное состояние.
| Гибридизация: | sp | sp2 | sp3 |
| Число s-орбиталей | 1 | 1 | 1 |
| Число p-орбиталей | 1 | 2 | 3 |
| Доля s-орбитали | 50% | 33% | 25% |
Повышенная полярность связи С–Н у атомов углерода при тройной связи в алкинах приводит к возможности отщепления протона Н+, т.е. приводит к появлению у алкинов с тройной связью на конце молекулы (алкинов-1) кислотных свойств.
Ацетилен и его гомологи с тройной связью на конце молекулы R–C≡C–H проявляют слабые кислотные свойства, атомы водорода на конце молекулы могут легко замещаться на атомы металлов.
Алкины с тройной связью на конце молекулы взаимодействуют с активными металлами, гидридами, амидами металлов и т.д.
Например, ацетилен взаимодействует с натрием с образованием ацетиленида натрия.
Например, пропин взаимодействует с амидом натрия с образованием пропинида натрия.
Алкины с тройной связью на конце молекулы взаимодействуют с аммиачным раствором оксида серебра (I) или аммиачным раствором хлорида меди (I).
При этом образуются нерастворимые в воде ацетилениды серебра или меди (I):
Алкины с тройной связью на конце молекулы взаимодействуют с аммиачным раствором оксида серебра или аммиачным раствором хлорида меди (I) с образованием белого или красно-коричневого осадка соответственно. Это качественная реакция на алкины с тройной связью на конце молекулы.
Соответственно, алкины, в которых тройная связь расположена не на конце молекулы, не реагируют с аммиачными растворами оксида серебра или хлорида меди (I).
Получение алкинов
1. Дегидрирование алканов
При дегидрировании алканов, содержащих от двух до трех атомов углерода в молекуле, образуются двойные и тройные связи.
Например, при дегидрировании этана может образоваться этилен или ацетилен:
2. Пиролиз метана
Пиролиз метана – это промышленный способ получения ацетилена.
Реакцию проводят, очень быстро пропуская метан между электродами (электродуговой способ) — примерно 0,1-0,01 секунды при температуре 1500оС.
Если процесс проводить дольше, то метан разлагается на углерод и водород:
3. Гидролиз карбида кальция
Лабораторный способ получения ацетилена – водный или кислотный гидролиз карбида кальция CaC2.
СаС2 + 2Н2О = Са(ОН)2 + С2Н2
В кислой среде образуется ацетилен и соответствующая соль:
CaC2 + 2HCl = CaCl2 + C2H2
Карбид кальция можно получить, нагревая оксид кальция с углеродом:
СаО + 3С (изб) → СаС2 + СО
4. Дегидрогалогенирование дигалогеналканов
Дигалогеналканы, в молекулах которых два атома галогена расположены у одного, либо у соседних атомов углерода, реагируют с избытком спиртового раствора щелочей с образованием алкинов.
Например, 1,2-дихлорпропан реагирует со спиртовым раствором гидроксида натрия
1,1-дихлорпропан реагирует со спиртовым раствором щелочи с образованием пропина.
5. Алкилирование соединений алкинов с металлами
Ацетилениды, пропиниды и прочие соединения алкинов с металлами реагируют с галогеналканами с образованием гомологов алкинов. При этом происходит удлиннение исходной молекулы алкина.
Например, пропинид натрия реагирует с бромэтаном с образованием пентина-2
-
Типы задач в задании С5.
-
Необходимые теоретические сведения.
-
Определение формул веществ по массовым долям атомов, входящих в его состав.
-
Определение формул веществ по продуктам сгорания.
-
Определение формул веществ по химическим свойствам.
-
Задачи для самостоятельного решения.
-
Часть 1. Определение формулы вещества по составу.
-
Часть 2. Определение формулы вещества по продуктам сгорания.
-
Часть 3. Определение формулы вещества по химическим свойствам.
-
Ответы и комментарии к задачам для самостоятельного решения.
Задачи на определение формулы органического вещества бывают нескольких видов. Обычно решение этих задач не представляет особых сложностей, однако часто выпускники теряют баллы на этой задаче. Причин бывает несколько:
- Некорректное оформление;
- Решение не математическим путем, а методом перебора;
- Неверно составленная общая формула вещества;
- Ошибки в уравнении реакции с участием вещества, записанного в общем виде.
к оглавлению ▴
Типы задач в задании С5.
- Определение формулы вещества по массовым долям химических элементов или по общей формуле вещества;
- Определение формулы вещества по продуктам сгорания;
- Определение формулы вещества по химическим свойствам.
Необходимые теоретические сведения.
- Массовая доля элемента в веществе.
Массовая доля элемента — это его содержание в веществе в процентах по массе.
Например, в веществе состава С2Н4 содержится 2 атома углерода и 4 атома водорода. Если взять 1 молекулу такого вещества, то его молекулярная масса будет равна:
Мr(С2Н4) = 2 • 12 + 4 • 1 = 28 а.е.м. и там содержится 2 • 12 а.е.м. углерода.Чтобы найти массовую долю углерода в этом веществе, надо его массу разделить на массу всего вещества:
ω(C) = 12 • 2 / 28 = 0,857 или 85,7%.
Если вещество имеет общую формулу СхНуОz, то массовые доли каждого их атомов так же равны отношению их массы к массе всего вещества. Масса х атомов С равна — 12х, масса у атомов Н — у, масса z атомов кислорода — 16z.
Тогда
ω(C) = 12 • х / (12х + у + 16z)Если записать эту формулу в общем виде, то получится следующее выражение:
Массовая доля атома Э в веществе = Атомная масса атома Э • число атомов Э в молекуле Аr(Э) • z —————— Mr(вещ.) Молекулярная масса вещества - Молекулярная и простейшая формула вещества.Молекулярная (истинная) формула — формула, в которой отражается реальное число атомов каждого вида, входящих в молекулу вещества.
Например, С6Н6 — истинная формула бензола.
Простейшая (эмпирическая) формула — показывает соотношение атомов в веществе.
Например, для бензола соотношение С:Н = 1:1, т.е. простейшая формула бензола — СН.
Молекулярная формула может совпадать с простейшей или быть кратной ей.Примеры.
Вещество Молекулярная формула Соотношение атомов Простейшая формула Этанол С2Н6О С:Н:О = 2:6:1 С2Н6О Бутен С4Н8 С:Н = 1:2 СН2 Уксусная кислота С2Н4О2 С:Н:О = 1:2:1 СН2О Если в задаче даны только массовые доли элементов, то в процессе решения задачи можно вычислить только простейшую формулу вещества. Для получения истинной формулы в задаче обычно даются дополнительные данные — молярная масса, относительная или абсолютная плотность вещества или другие данные, с помощью которых можно определить молярную массу вещества.
- Относительная плотность газа Х по газу У — DпоУ(Х).
Относительная плотность D — это величина, которая показывает, во сколько раз газ Х тяжелее газа У. Её рассчитывают как отношение молярных масс газов Х и У:
DпоУ(Х) = М(Х) / М(У)
Часто для расчетов используют относительные плотности газов по водороду и по воздуху.
Относительная плотность газа Х по водороду:
Dпо H2 = M(газа Х) / M(H2) = M(газа Х) / 2
Воздух — это смесь газов, поэтому для него можно рассчитать только среднюю молярную массу. Её величина принята за 29 г/моль (исходя из примерного усреднённого состава).
Поэтому:
Dпо возд. = М(газа Х) / 29 - Абсолютная плотность газа при нормальных условиях.Абсолютная плотность газа — это масса 1 л газа при нормальных условиях. Обычно для газов её измеряют в г/л.
ρ = m(газа) / V(газа)
Если взять 1 моль газа, то тогда:
ρ = М / Vm,
а молярную массу газа можно найти, умножая плотность на молярный объём. - Общие формулы веществ разных классов.
Часто для решения задач с химическими реакциями удобно пользоваться не обычной общей формулой, а формулой, в которой выделена отдельно кратная связь или функциональная группа.Класс органических веществ Общая молекулярная формула Формула с выделенной кратной связью и функциональной группой Алканы CnH2n+2 — Алкены CnH2n CnH2n+1–CH=CH2 Алкины CnH2n−2 CnH2n+1–C≡CH Диены CnH2n−2 — Гомологи бензола CnH2n−6 С6Н5–СnH2n+1 Предельные одноатомные спирты CnH2n+2O CnH2n+1–OH Многоатомные спирты CnH2n+2Ox CnH2n+2−x(OH)x Предельные альдегиды CnH2nO Кетоны CnH2nO O // CnH2n+1– C– O–CmH2m+1 Фенолы CnH2n−6O С6Н5(СnH2n)–OH Предельные карбоновые кислоты CnH2nO2 Сложные эфиры CnH2nO2 O // CnH2n+1– C– O–CmH2m+1 Амины CnH2n+3N СnH2n+1NH2 Аминокислоты (предельные одноосновные) CnH2n+1NO2 O // NH2– CH– C– OH C nH 2n+1
к оглавлению ▴
Определение формул веществ по массовым долям атомов, входящих в его состав.
Решение таких задач состоит из двух частей:
- сначала находят мольное соотношение атомов в веществе — оно соответствует его простейшей формуле. Например, для вещества состава АхВу соотношение количеств веществ А и В соответствует соотношению числа их атомов в молекуле:
х : у = n(A) : n(B); - затем, используя молярную массу вещества, определяют его истинную формулу.
-
Пример 1.
Определить формулу вещества, если оно содержит 84,21% С и 15,79% Н и имеет относительную плотность по воздуху, равную 3,93.
Решение примера 1.
- Пусть масса вещества равна 100 г. Тогда масса С будет равна 84,21 г, а масса Н — 15,79 г.
- Найдём количество вещества каждого атома:
ν(C) = m / M = 84,21 / 12 = 7,0175 моль,
ν(H) = 15,79 / 1 = 15,79 моль. - Определяем мольное соотношение атомов С и Н:
С : Н = 7,0175 : 15,79 (сократим оба числа на меньшее) = 1 : 2,25 (домножим на 4) = 4 : 9.
Таким образом, простейшая формула — С4Н9. - По относительной плотности рассчитаем молярную массу:
М = D(возд.) • 29 = 114 г/моль.
Молярная масса, соответствующая простейшей формуле С4Н9 — 57 г/моль, это в 2 раза меньше истинно молярной массы.
Значит, истинная формула — С8Н18.
Есть гораздо более простой метод решения такой задачи, но, к сожалению, за него не поставят полный балл. Зато он подойдёт для проверки истинной формулы, т.е. с его помощью вы можете проверить своё решение.
Метод 2: Находим истинную молярную массу (114 г/моль), а затем находим массы атомов углерода и водорода в этом веществе по их массовым долям.
m(C) = 114 • 0,8421 = 96; т.е. число атомов С 96/12 = 8
m(H) = 114 • 0,1579 = 18; т.е число атомов Н 18/1 = 18.
Формула вещества — С8Н18.
Ответ: С8Н18.
-
Пример 2.
Определить формулу алкина с плотностью 2,41 г/л при нормальных условиях.
Решение примера 2.
Общая формула алкина СnH2n−2
Как, имея плотность газообразного алкина, найти его молярную массу? Плотность ρ — это масса 1 литра газа при нормальных условиях.
Так как 1 моль вещества занимает объём 22,4 л, то необходимо узнать, сколько весят 22,4 л такого газа:
M = (плотность ρ) • (молярный объём Vm) = 2,41 г/л • 22,4 л/моль = 54 г/моль.
Далее, составим уравнение, связывающее молярную массу и n:
14 • n − 2 = 54, n = 4.
Значит, алкин имеет формулу С4Н6.
Ответ: С4Н6.
-
Пример 3.
Определить формулу предельного альдегида, если известно, что 3•1022 молекул этого альдегида весят 4,3 г.
Решение примера 3.
В этой задаче дано число молекул и соответствующая масса. Исходя из этих данных, нам необходимо вновь найти величину молярной массы вещества.
Для этого нужно вспомнить, какое число молекул содержится в 1 моль вещества.
Это число Авогадро: Na = 6,02•1023 (молекул).
Значит, можно найти количество вещества альдегида:
ν = N / Na = 3•1022 / 6,02•1023 = 0,05 моль,
и молярную массу:
М = m / n = 4,3 / 0,05 = 86 г/моль.
Далее, как в предыдущем примере, составляем уравнение и находим n.
Общая формула предельного альдегида СnH2nO, то есть М = 14n + 16 = 86, n = 5.
Ответ: С5Н10О, пентаналь.
-
Пример 4.
Определить формулу дихлоралкана, содержащего 31,86 % углерода.
Решение примера 4.
Общая формула дихлоралкана: СnH2nCl2, там 2 атома хлора и n атомов углерода.
Тогда массовая доля углерода равна:
ω(C) = (число атомов C в молекуле) • (атомная масса C) / (молекулярная масса дихлоралкана)
0,3186 = n • 12 / (14n + 71)
n = 3, вещество — дихлорпропан.
Ответ: С3Н6Cl2, дихлорпропан.
к оглавлению ▴
Определение формул веществ по продуктам сгорания.
В задачах на сгорание количества веществ элементов, входящих в исследуемое вещество, определяют по объёмам и массам продуктов сгорания — углекислого газа, воды, азота и других. Остальное решение — такое же, как и в первом типе задач.
-
Пример 5.
448 мл (н. у.) газообразного предельного нециклического углеводорода сожгли, и продукты реакции пропустили через избыток известковой воды, при этом образовалось 8 г осадка. Какой углеводород был взят?
Решение примера 5.
- Общая формула газообразного предельного нециклического углеводорода (алкана) — CnH2n+2
Тогда схема реакции сгорания выглядит так:
CnH2n+2 + О2 → CO2 + H2O
Нетрудно заметить, что при сгорании 1 моль алкана выделится n моль углекислого газа.
Количество вещества алкана находим по его объёму (не забудьте перевести миллилитры в литры!):
ν(CnH2n+2) = 0,488 / 22,4 = 0,02 моль. - При пропускании углекислого газа через известковую воду Са(ОН)2 выпадает осадок карбоната кальция:
СО2 + Са(ОН)2 = СаСО3 + Н2О
Масса осадка карбоната кальция — 8 г, молярная масса карбоната кальция 100 г/моль.
Значит, его количество вещества
ν(СаСО3) = 8 / 100 = 0,08 моль.
Количество вещества углекислого газа тоже 0,08 моль. - Количество углекислого газа в 4 раза больше чем алкана, значит формула алкана С4Н10.
Ответ: С4Н10.
-
Пример 6.
Относительная плотность паров органического соединения по азоту равна 2. При сжигании 9,8 г этого соединения образуется 15,68 л углекислого газа (н. у) и 12,6 г воды. Выведите молекулярную формулу органического соединения.
Решение примера 6.
Так как вещество при сгорании превращается в углекислый газ и воду, значит, оно состоит из атомов С, Н и, возможно, О. Поэтому его общую формулу можно записать как СхНуОz.
- Схему реакции сгорания мы можем записать (без расстановки коэффициентов):
СхНуОz + О2 → CO2 + H2O
Весь углерод из исходного вещества переходит в углекислый газ, а весь водород — в воду. - Находим количества веществ CO2 и H2O, и определяем, сколько моль атомов С и Н в них содержится:
ν(CO2) = V / Vm = 15,68 / 22,4 = 0,7 моль.
На одну молекулу CO2 приходится один атом С, значит, углерода столько же моль, сколько CO2.ν(C) = 0,7 моль
ν(Н2О) = m / M = 12,6 / 18 = 0,7 моль.В одной молекуле воды содержатся два атома Н, значит количество водорода в два раза больше, чем воды.
ν(H) = 0,7 • 2 = 1,4 моль. - Проверяем наличие в веществе кислорода. Для этого из массы всего исходного вещества надо вычесть массы С и Н.
m(C) = 0,7 • 12 = 8,4 г, m(H) = 1,4 • 1 = 1,4 г
Масса всего вещества 9,8 г.
m(O) = 9,8 − 8,4 − 1,4 = 0, т.е.в данном веществе нет атомов кислорода.
Если бы кислород в данном веществе присутствовал, то по его массе можно было бы найти количество вещества и рассчитывать простейшую формулу, исходя из наличия трёх разных атомов. - Дальнейшие действия вам уже знакомы: поиск простейшей и истинной формул.
С : Н = 0,7 : 1,4 = 1 : 2
Простейшая формула СН2. - Истинную молярную массу ищем по относительной плотности газа по азоту (не забудьте, что азот состоит из двухатомных молекул N2 и его молярная масса 28 г/моль):
Mист. = Dпо N2 • M(N2) = 2 • 28 = 56 г/моль.
Истиная формула СН2, её молярная масса 14.
56 / 14 = 4.
Истинная формула С4Н8.
Ответ: С4Н8.
-
Пример 7.
Определите молекулярную формулу вещества, при сгорании 9 г которого образовалось 17,6 г CO2, 12,6 г воды и азот. Относительная плотность этого вещества по водороду — 22,5. Определить молекулярную формулу вещества.
Решение примера 7.
- Вещество содержит атомы С,Н и N. Так как масса азота в продуктах сгорания не дана, её надо будет рассчитывать, исходя из массы всего органического вещества.
Схема реакции горения:
СхНуNz + O2 → CO2 + H2O + N2 - Находим количества веществ CO2 и H2O, и определяем, сколько моль атомов С и Н в них содержится:
ν(CO2) = m / M = 17,6 / 44 = 0,4 моль.
ν(C) = 0,4 моль.
ν(Н2О) = m / M = 12,6 / 18 = 0,7 моль.
ν(H) = 0,7 • 2 = 1,4 моль. - Находим массу азота в исходном веществе.
Для этого из массы всего исходного вещества надо вычесть массы С и Н.m(C) = 0,4 • 12 = 4,8 г,
m(H) = 1,4 • 1 = 1,4 гМасса всего вещества 9,8 г.
m(N) = 9 − 4,8 − 1,4 = 2,8 г ,
ν(N) = m /M = 2,8 / 14 = 0,2 моль. - C : H : N = 0,4 : 1,4 : 0,2 = 2 : 7 : 1
Простейшая формула — С2Н7N.
Истинная молярная масса
М = Dпо Н2 • М(Н2) = 22,5 • 2 = 45 г/моль.
Она совпадает с молярной массой, рассчитанной для простейшей формулы. То есть это и есть истинная формула вещества.
Ответ: С2Н7N.
-
Пример 8.
Вещества содержит С, Н, О и S. При сгорании 11 г его выделилось 8,8 г CO2, 5,4 г Н2О, а сера была полностью переведена в сульфат бария, масса которого оказалась равна 23,3 г. Определить формулу вещества.
Решение примера 8.
Формулу заданного вещества можно представить как CxHySzOk. При его сжигании получается углекислый газ, вода и сернистый газ, который затем превращают в сульфат бария. Соответственно, вся сера из исходного вещества превращена в сульфат бария.
- Находим количества веществ углекислого газа, воды и сульфата бария и соответствующих химических элементов из исследуемого вещества:
ν(CO2) = m/M = 8,8/44 = 0,2 моль.
ν(C) = 0,2 моль.
ν(Н2О) = m / M = 5,4 / 18 = 0,3 моль.
ν(H) = 0,6 моль.
ν(BaSO4) = 23,3 / 233 = 0,1 моль.
ν(S) = 0,1 моль. - Рассчитываем предполагаемую массу кислорода в исходном веществе:
m(C) = 0,2 • 12 = 2,4 г
m(H) = 0,6 • 1 = 0,6 г
m(S) = 0,1 • 32 = 3,2 г
m(O) = mвещества − m(C) − m(H) − m(S) = 11 − 2,4 − 0,6 − 3,2 = 4,8 г,
ν(O) = m / M = 4,8 / 16 = 0,3 моль - Находим мольное соотношение элементов в веществе:
C : H : S : O = 0,2 : 0,6 : 0,1 : 0,3 = 2 : 6 : 1 : 3
Формула вещества C2H6SO3.
Надо отметить, что таким образом мы получили только простейшую формулу.
Однако, полученная формула является истинной, поскольку при попытке удвоения этой формулы (С4Н12S2O6) получается, что на 4 атома углерода, помимо серы и кислорода, приходится 12 атомов Н, а это невозможно.
Ответ: C2H6SO3.
к оглавлению ▴
Определение формул веществ по химическим свойствам.
-
Пример 9.
Определить формулу алкадиена, если г его могут обесцветить 80 г 2%-го раствора брома.
Решение примера 9.
- Общая формула алкадиенов — СnH2n−2.
Запишем уравнение реакции присоединения брома к алкадиену, не забывая, что в молекуле диена две двойные связи и, соответственно, в реакцию с 1 моль диена вступят 2 моль брома:
СnH2n−2 + 2Br2 → СnH2n−2Br4 - Так как в задаче даны масса и процентная концентрация раствора брома, прореагировавшего с диеном, можно рассчитать количества вещества прореагировавшего брома:
m(Br2) = mраствора • ω = 80 • 0,02 = 1,6 г
ν(Br2) = m / M = 1,6 / 160 = 0,01 моль. - Так как количество брома, вступившего в реакцию, в 2 раза больше, чем алкадиена, можно найти количество диена и (так как известна его масса) его молярную массу:
0,005 0,01 СnH2n−2 + 2Br2 → СnH2n−2Br4 Мдиена = m / ν = 3,4 / 0,05 = 68 г/моль.
- Находим формулу алкадиена по его общей формул, выражая молярную массу через n:
14n − 2 = 68
n = 5.Это пентадиен С5Н8.
Ответ: C5H8.
-
Пример 10.
При взаимодействии 0,74 г предельного одноатомного спирта с металлическим натрием выделился водород в количестве, достаточном для гидрирования 112 мл пропена (н. у.). Что это за спирт?
Решение примера 10.
- Формула предельного одноатомного спирта — CnH2n+1OH. Здесь удобно записывать спирт в такой форме, в которой легко составить уравнение реакции — т.е. с выделенной отдельно группой ОН.
- Составим уравнения реакций (нельзя забывать о необходимости уравнивать реакции):
2CnH2n+1OH + 2Na
→
2CnH2n+1ONa + H2
C3H6 + H2→
C3H8
- Можно найти количество пропена, а по нему — количество водорода. Зная количество водорода, по реакции находим количество вещества спирта:
ν(C3H6) = V / Vm = 0,112 / 22,4 = 0,005 моль => ν(H2) = 0,005 моль,
νспирта = 0,005 • 2 = 0,01 моль. - Находим молярную массу спирта и n:
Mспирта = m / ν = 0,74 / 0,01 = 74 г/моль,
14n + 18 = 74
14n = 56
n = 4.Спирт — бутанол С4Н7ОН.
Ответ: C4H7OH.
-
Пример 11.
Определить формулу сложного эфира, при гидролизе 2,64 г которого выделяется 1,38 г спирта и 1,8 г одноосновной карбоновой кислоты.
Решение примера 11.
- Общую формулу сложного эфира, состоящего из спирта и кислоты с разным числом атомов углерода можно представить в таком виде:
CnH2n+1COOCmH2m+1
Соответственно, спирт будет иметь формулу
CmH2m+1OH,
а кислота
CnH2n+1COOH.
Уравнение гидролиза сложного эфира:
CnH2n+1COOCmH2m+1 + H2O → CmH2m+1OH + CnH2n+1COOH - Согласно закону сохранения массы веществ, сумма масс исходных веществ и сумма масс продуктов реакции равны.
Поэтому из данных задачи можно найти массу воды:mH2O = (масса кислоты) + (масса спирта) − (масса эфира) = 1,38 + 1,8 − 2,64 = 0,54 г
νH2O = m / M = 0,54 / 18 = 0,03 мольСоответственно, количества веществ кислоты и спирта тоже равны моль.
Можно найти их молярные массы:Мкислоты = m / ν = 1,8 / 0,03 = 60 г/моль,
Мспирта = 1,38 / 0,03 = 46 г/моль.Получим два уравнения, из которых найдём m и n:
MCnH2n+1COOH = 14n + 46 = 60, n = 1 — уксусная кислота
MCmH2m+1OH = 14m + 18 = 46, m = 2 — этанол.Таким образом, искомый эфир — это этиловый эфир уксусной кислоты, этилацетат.
Ответ: CH3COOC2H5.
-
Пример 12.
Определить формулу аминокислоты, если при действии на 8,9 г её избытком гидроксида натрия можно получить 11,1 г натриевой соли этой кислоты.
Решение примера 12.
- Общая формула аминокислоты (если считать, что она не содержит никаких других функциональных групп, кроме одной аминогруппы и одной карбоксильной):
NH2–CH(R)–COOH.
Можно было бы записать её разными способами, но для удобства написания уравнения реакции лучше выделять в формуле аминокислоты функциональные группы отдельно. - Можно составить уравнение реакции этой аминокислоты с гидроксидом натрия:
NH2–CH(R)–COOH + NaOH → NH2–CH(R)–COONa + H2O
Количества вещества аминокислоты и её натриевой соли — равны. При этом мы не можем найти массу какого-либо из веществ в уравнении реакции. Поэтому в таких задачах надо выразить количества веществ аминокислоты и её соли через молярные массы и приравнять их:M(аминокислоты NH2–CH(R)–COOH) = 74 + МR
M(соли NH2–CH(R)–COONa) = 96 + МR
νаминокислоты = 8,9 / (74 + МR),
νсоли = 11,1 / (96 + МR)
8,9 / (74 + МR) = 11,1 / (96 + МR)
МR = 15Легко увидеть, что R = CH3.
Можно это сделать математически, если принять, что R — CnH2n+1.
14n + 1 = 15, n = 1.
Это аланин — аминопропановая кислота.
Ответ: NH2–CH(CH3)–COOH.
к оглавлению ▴
Задачи для самостоятельного решения.
Часть 1. Определение формулы вещества по составу.
1–1. Плотность углеводорода при нормальных условиях равна 1,964 г/л. Массовая доля углерода в нем равна 81,82%. Выведите молекулярную формулу этого углеводорода.
1–2. Массовая доля углерода в диамине равна 48,65%, массовая доля азота равна 37,84%. Выведите молекулярную формулу диамина.
1–3. Относительная плотность паров предельной двухосновной карбоновой кислоты по воздуху равна 4,07. Выведите молекулярную формулу карбоновой кислоты.
1–4. 2 л алкадиена при н.у. имеет массу, равную 4,82 г. Выведите молекулярную формулу алкадиена.
1–5. (ЕГЭ–2011) Установите формулу предельной одноосновной карбоновой кислоты, кальциевая соль которой содержит 30,77 % кальция.
к оглавлению ▴
Часть 2. Определение формулы вещества по продуктам сгорания.
2–1. Относительная плотность паров органического соединения по сернистому газу равна 2. При сжигании 19,2 г этого вещества образуется 52,8 г углекислого газа (н.у.) и 21,6 г воды. Выведите молекулярную формулу органического соединения.
2–2. При сжигании органического вещества массой 1,78 г в избытке кислорода получили 0,28 г азота, 1,344 л (н.у.) СО2 и 1,26 г воды. Определите молекулярную формулу вещества, зная, что в указанной навеске вещества содержится 1,204•1022 молекул.
2–3. Углекислый газ, полученный при сгорании 3,4 г углеводорода, пропустили через избыток раствора гидроксида кальция и получили 25 г осадка. Выведите простейшую формулу углеводорода.
2–4. При сгорании органического вещества, содержащего С, Н и хлор, выделилось 6,72 л (н.у.) углекислого газа, 5,4 г воды, 3,65 г хлороводорода. Установите молекулярную формулу сгоревшего вещества.
2–5. (ЕГЭ–2011) При сгорании амина выделилось 0,448 л (н.у.) углекислого газа, 0,495 г воды и 0,056 л азота. Определить молекулярную формулу этого амина.
к оглавлению ▴
Часть 3. Определение формулы вещества по химическим свойствам.
3–1. Определить формулу алкена, если известно, что он 5,6 г его при присоединении воды образуют 7,4 г спирта.
3–2. Для окисления 2,9 г предельного альдегида до кислоты потребовалось 9,8 г гидроксида меди (II). Определить формулу альдегида.
3–3. Одноосновная моноаминокислота массой 3 г с избытком бромоводорода образует 6,24 г соли. Определить формулу аминокислоты.
3–4. При взаимодействии предельного двухатомного спирта массой 2,7 г с избытком калия выделилось 0,672 л водорода. Определить формулу спирта.
3–5. (ЕГЭ–2011) При окислении предельного одноатомного спирта оксидом меди (II) получили 9,73 г альдегида, 8,65 г меди и воду. Определить молекулярную формулу этого спирта.
к оглавлению ▴
Ответы и комментарии к задачам для самостоятельного решения.
1–1. С3Н8
1–2. С3Н6(NH2)2
1–3. C2H4(COOH)2
1–4. C4H6
1–5. (HCOO)2Ca — формиат кальция, соль муравьиной кислоты
2–1. С8Н16О
2–2. С3Н7NO
2–3. С5Н8 (массу водорода находим, вычитая из массы углеводорода массу углерода)
2–4. C3H7Cl (не забудьте, что атомы водорода содержатся не только в воде, но и в HCl)
2–5. C4H11N
3–1. С4Н8
3–2. С3Н6О
3–3. С2Н5NO2
3–4. C4H8(OH)2
3–5. C4H9OH
Спасибо за то, что пользуйтесь нашими статьями.
Информация на странице «Химия, часть С. Задача С5. Определение формул органических веществ.» подготовлена нашими редакторами специально, чтобы помочь вам в освоении предмета и подготовке к экзаменам.
Чтобы успешно сдать нужные и поступить в высшее учебное заведение или колледж нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими статьями из разделов нашего сайта.
Публикация обновлена:
08.05.2023
- Подробности
- Категория: ЕГЭ — химия
Метод определения молекулярной формулы алкина
Задача 2.3.
Определите молекулярную формулу ацетиленового углеводорода, если молярная масса продукта его реакции с избытком бромоводорода в 4 раза больше, чем молярная масса исходного углеводорода.
Дано:
отношение масс бромпроизводного к исходному углеводороду:
Найти: молекулярную формулу ацетиленового углеводорода.
Решение:
Общая формула ацетиленого углеводорода имеет вид:
СnH2n–2.
Все углеводороды данного ряда содержат одну тройную связь и при избытке бромоводорода присоединяют 4 атома. Запишем химическую реакцию:
СnH2n–2 + 2HBr ⇒ СnH2nBr2
Запишем выражения для молярных масс исходного углеводорода и продукта реакции с использованием молярных масс элементов:
M(СnH2n–2) = 12n + 2n — 2 = (14n — 2) г/моль,
M(СnH2nBr2) = 12n + 2n + (80 .2)= (14n + 160) г/моль.
Разделим выражение для молярной массы продукта реакции на выражение для молярной массы исходного вещества и приравняем это отношение к значению, указанному в условии:
Получили математическое уравнение с одним неизвестным. Решая его, получаем n = 4. Следовательно, формула исходного углеводорода: С4Н6.
Ответ: С4Н6 (бутин).
Обучение
решения задач по химии по нахождению формулы вещества (методические
рекомендации)
Автор:
учитель химии МБОУ Школа № 2 г. Ленска Республики Саха (Якутия)
Суянко
Татьяна Алексеевна
Задачи
по данной теме решаются в 8-11 классах, как в программном материале, так и
встречаются в заданиях ЕГЭ, но ещё более усложненные.
Задачи на
определение формулы органического вещества бывают нескольких видов. Обычно
решение этих задач не представляет особых сложностей, однако часто обучающиеся затрудняются
в решении задач по нахождению формулы вещества. Причин бывает несколько:
1.
Некорректное оформление;
2.
Решение не математическим
путем, а методом перебора;
3.
Неверно составленная общая
формула вещества;
4.
Ошибки в уравнении реакции с
участием вещества, записанного в общем виде.
Типы задач на
нахождение формулы вещества.
1.
Определение формулы вещества по
массовым долям химических элементов или по общей формуле вещества;
2.
Определение формулы вещества по
продуктам сгорания;
3.
Определение формулы вещества по
химическим свойствам.
Для решения задач необходимы теоретические
сведения.
- Для решения задач необходимо знать что такое:
- Массовая доля элемента в веществе.
Массовая доля элемента — это его
содержание в веществе в процентах по массе. Например, в веществе состава С2Н4 чтобы найти массовую долю углерода в этом
веществе, надо его массу разделить на массу всего вещества: ω(C) = 12 • 2 / 28 = 0,857 (от
единицы) или 85,7%. Если
записать эту формулу в общем виде, то получится следующее выражение:
|
Массовая доля |
Атомная масса атома Э |
• |
число атомов Э в |
молекуле |
|
Аr (Э) • n |
||||
|
—————— |
||||
|
Mr(вещ.) |
||||
|
Молекулярная масса вещества |
- Молекулярная и простейшая формула вещества.
Молекулярная (истинная) формула —
формула, в которой отражается реальное число атомов каждого вида, входящих в
молекулу вещества. Например, С6Н6 — истинная формула бензола. Простейшая
(эмпирическая) формула — показывает соотношение атомов в
веществе. Например, для бензола соотношение С:Н = 1:1, т.е. простейшая
формула бензола — СН.
- Относительная плотность газа Х по газу У — DпоУ(Х).
Относительная плотность обозначается D — это
величина, которая показывает, во сколько раз газ Х тяжелее газа У. Её
рассчитывают как отношение молярных масс газов Х и У: DпоУ(Х) = М(Х) / М(У) Часто для расчетов используют относительные
плотности газов по водороду и по воздуху.
4.
Абсолютная плотность газа
это масса 1 л газа при нормальных условиях. Обычно для
газов её измеряют в г/л. ρ = m(газа) / V(газа) Если взять 1 моль газа, то тогда: ρ = М / Vm, а молярную массу газа можно найти, умножая плотность
на молярный объём.
- Общие формулы веществ разных классов.
Часто для решения задач с химическими реакциями удобно
пользоваться не обычной общей формулой, а формулой, в которой выделена отдельно
кратная связь или функциональная группа.
|
Класс органических веществ |
Общая молекулярная формула |
Формула с выделенной кратной связью и функциональной |
|||||||||||||||||
|
Алканы |
CnH2n+2 |
||||||||||||||||||
|
Алкены |
CnH2n |
CnH2n+1–CH=CH2 |
|||||||||||||||||
|
Алкины |
CnH2n−2 |
CnH2n+1–C≡CH |
|||||||||||||||||
|
Диены |
CnH2n−2 |
— |
|||||||||||||||||
|
Гомологи бензола |
CnH2n−6 |
С6Н5–СnH2n+1 |
|||||||||||||||||
|
Предельные одноатомные спирты |
CnH2n+2O |
CnH2n+1–OH |
|||||||||||||||||
|
Многоатомные спирты |
CnH2n+2Ox |
CnH2n+2−x(OH)x |
|||||||||||||||||
|
Предельные альдегиды |
CnH2nO |
||||||||||||||||||
|
Кетоны |
CnH2nO |
|
|||||||||||||||||
|
Фенолы |
CnH2n−6O |
С6Н5(СnH2n)–OH |
|||||||||||||||||
|
Предельные карбоновые кислоты |
CnH2nO2 |
||||||||||||||||||
|
Сложные эфиры |
CnH2nO2 |
|
|||||||||||||||||
|
Амины |
CnH2n+3N |
СnH2n+1NH2 |
|||||||||||||||||
|
Аминокислоты (предельные одноосновные) |
CnH2n+1NO2 |
|
6. Определение формул веществ по
массовым долям атомов, входящих в его состав.
Решение таких задач состоит из двух частей:
·
сначала находят мольное
соотношение атомов в веществе — оно соответствует его простейшей формуле.
Например, для вещества состава АхВу соотношение количеств веществ А и В соответствует
соотношению числа их атомов в молекуле: х : у = n(A) : n(B);
·
затем, используя молярную массу
вещества, определяют его истинную формулу.
Пример 1. Определить формулу вещества, если оно содержит
84,21% С и 15,79% Н и имеет относительную плотность по воздуху, равную 3,93.
Решение:
1.
По относительной плотности
рассчитаем молярную массу: М = D(возд.) • 29 = 114 г/моль. Молярная масса, соответствующая простейшей
формуле С4Н9— 57 г/моль, это в
2 раза меньше истинно молярной массы. Значит, истинная формула — С8Н18.
2.
По формуле нахождения массовой
доли элемента найдём количество атомов элемента
n=
Mr(вещ.)*w/ Аr (э); n(С) : n(Н) = 144*0,8421/12 : 144*0,1579/1 = 8:18
формула вещества С8Н18
Пример 2. Определить
формулу алкина с плотностью 2,41 г/л при нормальных условиях.
Решение:
Найдем молярную массу алкина
по формуле
M = (плотность ρ) • (молярный объём Vm) = 2,41
г/л • 22,4 л/моль = 54 г/моль
Зная общую формулу алкина, составим уравнение:
14 • n − 2 = 54, n = 4. Значит, алкин имеет формулу С4Н6.
Пример 3. Определить формулу предельного альдегида, если
известно, что 3•1022 молекул этого альдегида весят 4,3 г.
Решение:
Находим количество вещества альдегида:
ν = N / Na = 3•1022 / 6,02•1023 = 0,05 моль, и молярную массу:
М = m / n = 4,3 г / 0,05 моль = 86 г/моль.
Далее, как в предыдущем примере, составляем уравнение и
находим n.
Общая формула предельного альдегида СnH2nO, то есть М = 14n + 16 = 86, n = 5.
Формула альдегида С5Н10О
Пример 4. Определить
формулу дихлоралкана, содержащего 31,86 % углерода.
Решение:
Зная общую формулу алкана СnH 2n+2 Cl2 и формулу
нахождения массовой доли элемента w(С) = (число
атомов C в молекуле) • (атомная масса C) / (молекулярная масса дихлоралкана) 0,3186 = n • 12 / (14n + 71) n = 3, вещество — дихлорпропан.
Пример 5
- Определить
формулу аминокислоты, если известно, что она содержит 15,73% азота.
Решение:
Написать общую
формулу и выразить относительную молекулярную массу вещества через n
а)
общая формула аминокислот СnH2n(NH2)COOH
б)
выразим через n относительную молекулярную массу :
Mr(СnH2n(NH2)COOH)
= 12n + 2n + 16 + 45 = 14n + 61
в) подставим данные в формулу:
0,1573=(14*1) / 14n + 61
г) решим уравнение: 2,2022n + 9,5953 = 14; n = 2. Ответ: С2Н4(NH2)COOH
7. Определение формул веществ по
продуктам сгорания.
В решении задач
с применением понятия моль учащиеся используют умения, сформированные в 10
классе; расчет количества вещества и элемента по их массам (объемам) и
определении их отношения в составе соединения.
Эти действия
четко прослеживаются в обобщенной схеме решения задач на нахождение
молекулярной формул.
Пример 1: При сжигании 0,29 г газообразного вещества получили 448 мл
углекислого газа (н.у.) и 0,45 г воды. Относительная плотность неизвестного
вещества по водороду равна 29. Определите молекулярную формулу вещества.
Решение:
Найдём
количество вещества углекислого газа и воды и перейдем к нахождению их масс:
1. ν =mM
m= ν *M
ν (CO2)
ν (C)
m (C)
2ν (H2O) ν (H) m(H)
m(в-ва) = m(C) + m(H) < m(в-ва)
углеводород вещество содержит
кислород (или другие элементы)
Составляем
отношение количества вещества элементов:
2. ν (в-ва) : ν (C) : ν (C) : ν (H) : ν (O) расчет количественного
состава вещества.
Решение:
Мr = 29*D(н2); Мr
= 29*2 = 58; М = 58гмоль.
ν (в-ва) = mM; ν (в-ва) = 0,2958 = 0,005(моль);
ν (CO2) = ν ν m; ν (CO2)
= 0,44822,4 = 0,02(моль); ν (C) = ν (CO2)=
0,02(моль)
m(C) = 0,02*12 = 0,24(г)
ν (H2O) = 0,4518 = 0,025(моль); ν (H) = 2 ν (H2O) = 0,05 моль;
m(H) = 0,05*1 = 0,05(г)
m(в-ва) = 0,24г +
0,05г = 0,29г, следовательно, вещество состоит из водорода и
углерода(углеводород)
ν (в-ва) : ν (C) : ν (H) = 0,005 : 0,02 : 0,05 = 1 : 4 : 10.
Итак, в 1 моль
вещества содержит 4 моль углерода и 10 моль водорода.
Ответ: С4 Н10 (бутан)
8. Определение формул веществ по
химическим свойствам.
Пример 9. Определить
формулу алкадиена, если 3,4 г его могут обесцветить 80 г 2%-го раствора брома.
Решение
1.
Общая формула алкадиенов
— СnH2n−2. Запишем уравнение реакции присоединения брома к
алкадиену: СnH2n−2 + 2Br2 → СnH2n−2Br4
2.
рассчитаем количества вещества
прореагировавшего брома:
m(Br2) = mраствора • ω = 80 • 0,02 = 1,6 г ν(Br2) = m / M = 1,6 / 160 = 0,01 моль.
3.
Найдём количество вещества
диена, и (так как известна его масса) его молярную массу:
|
0,005 |
0,01 |
|
|
СnH2n−2 |
+ 2Br2 → |
СnH2n−2Br4 |
4.
Мдиена = m / ν = 3,4 / 0,05 = 68 г/моль.
5.
Находим формулу алкадиена по
его общей формул, выражая молярную массу через n:
14n − 2 = 68 n =
5.
Это
пентадиен С5Н8.
Пример 10. При взаимодействии 0,74 г предельного одноатомного
спирта с металлическим натрием выделился водород в количестве, достаточном для
гидрирования 112 мл пропена (н. у.). Что это за спирт?
Решение
1.
Формула предельного
одноатомного спирта — CnH2n+1OH.
2.
Составим уравнения реакций:
2CnH2n+1OH +
2Na → 2CnH2n+1ONa + H2
C3H6 + H2 → C3H8
3.
Найдём количество пропена, а
по нему — количество водорода и количество вещества спирта:
ν(C3H6) = V / Vm =
0,112 / 22,4 = 0,005 моль => ν(H2) = 0,005 моль, νспирта =
0,005 • 2 = 0,01 моль
4.
Находим молярную массу спирта и
n:
- Задачи для самостоятельного решения:
1. Массовая доля водорода в алкане составляет
0,1579. Определить формулу алкана.
- Массовая доля углерода в алкине 87,8%.
Определить формулу алкина. - Массовая доля кислорода в аминокислоте равна
35,95%. Найти молекулярную формулу аминокислоты. - Массовая доля хлора в хлоралкане 55,04%.
Найти молекулярную формулу хлоралкана. - Найдите
молекулярную формулу углеводорода, массовая доля углерода в котором 83,3%.
Относительная плотность паров этого вещества по водороду равна 36. - Найдите
молекулярную формулу углеводорода, массовая доля углерода в котором 81,8%.
Относительная плотность вещества по азоту 1,57. - При сжигании
углеводорода массой 29 г. Образовалось 88 г оксида углерода и 45 г воды.
Относительная плотность вещества по воздуху равна 2. Найдите молекулярную
формулу углеводорода. - При сгорании 31,2
г углеводорода образовалось 105,6 г оксида углерода и вода. Относительная
плотность паров этого углеводорода по аргону равна 1,95. Найдите
молекулярную формулу углеводорода. - При сжигании 8,8
г органического соединения образовалось 14,4 г воды и 13,44 л оксида
углерода. Относительная плотность паров этого углеводорода по аммиаку
равна 2,588. Найдите молекулярную формулу углеводорода. - Массовая доля
углерода в предельном одноатомном спирте равна 0,6818. Найдите
молекулярную формулу спирта. - Предельный
альдегид содержит 18,60% кислорода. Найдите молекулярную формулу
альдегида.
Литература:
- ЕГЭ. Химия. Самостоятельная подготовка к
ЕГЭ/Р.А.Лидин- М.: Издательство «Экзамен», 2015. – 351, (1) с. (Серия
«ЕГЭ. Полный курс») - ЕГЭ. 1000заданий с ответами и решениями по
химии. Все задания части 1 и 2 / М.А.Рябов. – М. : Издательство
«Экзамен», 2017. – 399, (1) с. (Серия «ЕГЭ. Банк заданий») - Химия 11 класс. Задачник для учащихся
общеобразовательных организаций. 2-е издание, переработанное. Москва
Издательский центр «Вентана-Граф» 2014. ФГОС. А.Н.Лёвкин, Н.Е.Кузнецова - М.А.Рябов Сборник задач и упражнений и
тестов по химии. К учебнику Г.Е. Рудзитиса, Ф.Г.Фельдмана «Химия.10
класс» Издательство «Экзамен». - Химия Практикум по общей химии 10-11 классы.
Составитель Тулина Н.И., 2006, Издательство «Учитель»
План урока:
Алкадиены или диены
Алкины
Алкадиены или диены
Алкадиены (их также называют диенами) – это углеводороды, которые имеют в своем составе 2 двойных связи.
Строение и номенклатура алкадиенов
Рассмотрим более подробно, что из себя представляют молекулы диенов, какой они имеют атомный состав, узнаем подробнее их структуру и изомерию.
Молекулярная формула диенов
Для начала определим: как связаны между собой число атомов углерода и водорода в молекуле диена. Общая формула алкадиенов выглядит так:
Из уроков про алканы и алкены мы знаем, что n – число атомов углерода в молекуле, и задается любое. Так как в молекуле диена присутствуют две двойных связи, то минимальное число атомов углерода должно быть 3, т.е. 3 атома углерода будут связаны между собой только двойными связями, как показано формулой ниже:
Для примера воспользуемся формулой, чтобы узнать молекулярный состав диенов, у которых 3, 4 или 7 атомов углерода.
Подставляем эти числа в формулу, и получаем молекулярные составы:
Теперь, зная молекулярный состав молекул, разберемся с их структурой.
Структурное строение молекул диенов
Всего существует 3 варианта расположение двойных связей, от которого будет зависеть гибридизация атомов углерода.
Рассмотрим каждый из них.
- Кумулированные связи. Что же означает это сложное слово? Кумулированные – это двойные связи, которые стоят у соседних атомов углерода, например у 1 и 2. Для наглядности посмотрим на рисунок ниже. У 1 и 3 атома углеродов тип гибридизации –sp2, и это означает, что у них есть 1 p-орбиталь, имеющая свою обычную форму в виде восьмерки. Только у 1 атома эта восьмерка расположена «горизонтально», а у 3 – «вертикально» (показано на рисунке 1).
У 2 атома углерода тип гибридизации – sp, и у него есть 2 p-орбитали с обычной формой – одна расположена «вертикально», а вторая «горизонтально» (смотрим на 2 атом углерода на рисунке 1).
Между первым и вторым атомом углерода образуются σ-связь (при перекрывании гибридных орбиталей, выделена синей линией) и π-связь (от перекрывания «горизонтальных» p-орбиталей, выделено зеленой линией). Между вторым и третьим также образуются σ-связь (от перекрывания гибридных орбиталей, выделена синей линией) и π-связь (от перекрывания «вертикальных» p-орбиталей, выделена зеленой линией).
Рисунок 1. – Образование кумулированных двойных связей
- Сопряженные связи. Если между двумя двойными связями есть одна одинарная связь, то такие связи называются сопряженными. Все 4 атома углерода, которые участвуют в образовании этих связей, имеют sp2-гибридизацию. При этом негибридизованные p-орбитали образуют так называемую пи-систему кратных связей, что представлено на рисунке 2. Пример структурной формулы диена с сопряженными кратными связями представлен ниже.
Рисунок 2. – Образование сопряженных кратных связей на примере бутадиена-1,3.
- Изолированные связи. Такой вид связей можно увидеть, если между двойными связями будут находиться несколько одинарных. Гибридизация атомов углерода при двойных связях, как мы уже знаем из первого и третьего уроков – sp2. Пример диена с изолированными связями представлен ниже.
Изомерия диенов
Рассмотрим структурные формулы разных веществ, которые имеют одинаковый атомный состав, (если вспомним, то это ни что иное, как определение «изомерии») на примере диена с названием пентадиен-1,3. Внимательно посмотрим на рисунок ниже и порассуждаем:
- Двойные связи в молекуле могут расположиться у разных атомов углерода. Например, у 1 и 3 или у 1 и 2, а как известно, у соединений с разным строением будут и разные свойства. Не забываем, что такой вид изомерии называется изомерией положения связей (стрелочка 1).
- Предположим, что кратные связи остались у 1 и 3 атома углеродов, но длина углеродного скелета теперь не 5, а 4 атома углерода, но зато есть метил-радикал. Если посчитаем число атомов углерода и водорода в полученном соединении (которое имеет название 2-метилбутадиен-1,3) и пентадиене-1,3, то выяснится, что их количество одинаково. Помним, что такой вид изомерии называется структурной (стрелочка 2).
- Сделаем так, что теперь в соединении вообще не будет никаких двойных связей, но зато будет 1 тройная. Посчитаем атомы углеродов и водородов. Получилось, что их ровно столько же, сколько и в пентадиене-1,3. Углеводород с 1 тройной связью – это один из отдельных классов углеводородов. А теперь вспомним, как называется вид изомерии, когда вещества относятся к разным классам, но имеют одинаковый состав? Если забыли, то ответ: межклассовая изомерия (стрелочка 3).
- Теперь немного поиграем с расположением атомов водорода и у атомов при одной из двойных связей. Если оба атома водорода будут, например, только снизу, то это цис-пентадиен-1,3. Если один атом водорода снизу, а второй сверху относительно двойной связи, то это транс-пентадиен-1,3. Такая изомерия называется пространственной (стрелочки 4 и 5).
Номенклатура алкадиенов
Выше уже были даны названия некоторым диенам, например пентадиен-1,3, 2-метилбутадиен-1,3 и другие. Почему их называют именно так? Есть ли какие-то закономерности? Если внимательно присмотримся к строению диенов и вспомним уроки 2 и 3, где рассказывалось про номенклатуры алканов и алкенов, то сразу станет понятно, что названия даются таким образом, чтобы учесть число атомов в самой длинной углеродной цепочке, наличие заместителей, и расположение кратных связей.
Сравним известный нам из третьего урока пентен-1 и пентадиен-1,3. Структурные формулы этих соединений выглядят так:
Что видим общего? И там и там атомы пронумерованы с того конца, где расположение кратных связей ближе. В углеродных цепочках по 5 атомов углерода (а из второго урока помним, что 5 – это корень пент-..). Названия оканчиваются суффиксом –ен, и через дефис в конце указывается, от каких атомов углерода берет начало двойная связь.
Какие видим различия? То, что в названии диена перед –ен стоит частичка ди, и корень не просто пент-, а пента-.
В органической химии, если в соединении несколько кратных связей, то в названии прописывается их количество, но только не по-русски, а по-древнегречески. Вспомним, что тоже самое делалось, когда давалось название сложному алкану, у которого было много одинаковых заместителей и нужно было указать их число (например 2,5,6,7-тетраметилдекан).
Точно также указывается количество двойных связей, но не перед корнем, а перед суффиксом. В алкадиенах их всегда две, а значит и все названия диенов будут оканчиваться одинаково: вот-такой диен. И обязательно указать, у каких атомов берут начало кратные связи в конце названия через запятые. Например: октадиен-1,2; гептадиен-2,5 илинонадиен-4,8.
Номенклатура диенов с заместителями строится по такому же принципу, как и у алкенов с заместителями, но только нужно помнить про разницу, указанную выше. Если забыли эту тему – срочно открывайте третий урок по органической химии, а если помним, то смотрим таблицу с номенклатурой алкадиенов для закрепления знаний.
Таблица 1. — Номенклатура алкадиенов
Физические свойства алкадиенов
Пропадиен и бутудиен по агрегатному состоянию – газы.
Диены, в составе которых от 5 до 17 атомов углерода, относятся к легкокипящим бесцветным жидкостям, температуры кипения и плавления некоторых представлены в таблице ниже. Выше 18 атомов углерода – твердые вещества.
Получение сопряженных алкадиенов
В органической химии большой интерес вызывают диены с сопряженными кратными связями, строение которых рассматривалось выше. Поэтому ниже будет повествование о способах синтеза и химических свойствах соединениях именно этого типа.
Рассмотрим способы получения алкадиенов
- Реакция Лебедева С.В. В 1928 году в мире наступала эпоха, когда люди хотели получать резину не из природных материалов, а с помощью химических превращений из дешевых реагентов. Такой интерес был вызван тем, что началось развитие машиностроения, и необходимо было добывать материалы, которые использовались бы для создания шин. Изначально такие материалы делались только в странах, где росло особое дерево – гевея, сок которого отверждался на воздухе и превращался в гибкий материал (рисунок 3). Но такое дерево может расти не везде, а кататься на машинах хотелось всем, вот и придумали особый способ получения вещества, которое впоследствии превращалось в резину.
Такой способ включает в себя одновременно 2 реакции: дегидрирование и дегидратацию (что это за реакции было подробно рассказано на 2 и 3 уроках).
Реакция Лебедева записывается следующим образом:
Рисунок 3. – Добыча сока гивеи.
- Дегидратация гликолей в присутствии серной кислоты.
Чтобы получить сопряженный диен данным методом, необходимо подобрать правильно гликоль.
На представленном ниже рисунке видно, какая у него должна быть структурная формула: фрагмент углеродной цепи, где позже будут находиться сопряженные двойные связи, должен содержать 4 атома углерода (каждый из них пронумерован), причем ОН-группы стоят именно у 1 и 4 атомов углерода. Помимо этого, у 2 и 3 атомов углерода обязательно должны стоять атомы водородов (хотя бы по 1 штуке).
При протекании реакции у 1 и 4 атомов углерода разрушаются связи С-ОН, а у 2 и 3 разрушаются связи С-Н, что видно на рисунке ниже.
После этого начинают образовываться связи между 1 и 2, 3 и 4 атомами углерода, а также между атомами водорода и ОН-группами, что показано на рисунке ниже.
Вещество Н-ОН – это не что иное, как Н2О, т.е. молекула воды, которая является побочным продуктом данной реакции.
Если совместим первый и последний рисунки, добавим условия реакции, то получим схему образования диена с помощью дегидратации гликолей:
- Получение из дигалогеналканов.
Теперь рассмотрим схему получения сопряженных диенов из дигалогеналканов, которая изображена вверху рисунка, который представлен ниже. Как и в случае с гликолями, фрагмент углеродной цепочки, где будут двойные связи, должен содержать 4 атома углерода, только теперь вместо ОН-групп у 1 и 4 атомов углеродов стоят заместители-галогены (хлор, бром или иод).При протекании реакции происходит разрыв связей между атомами галогена и углерода, а также водорода и углерода (как показано на нижнем рисунке).
Затем происходит образование двойных связей и образование молекул галогенводородов (в данном случае хлороводорода НСl). Галогенводород взаимодействует с щелочью, в результате чего получается соль и вода.
Химические свойства сопряженных алкадиенов
Рассмотрим некоторые химические реакции сопряженных диенов: присоединения, горения и полимеризации.
Реакции присоединения сопряженных диенов
Один вариант присоединений выглядит следующим образом: в диене есть 2 двойные связи, и между ними находится одинарная. После протекания реакции там, где были двойные связи(т.е. между 1 и 2, 3 и 4 атомами углерода), появляются одинарные, а там, где стояла одинарная (т.е. между 2 и 3 атомами углерода) – появляется двойная. Вещество А-Б распадается на 2 части (на частичку А и частичку Б), которые присоединяются к 1 и 4 атомам углерода, как это показано на рисунке ниже.
Рассмотрим, как к молекуле диена присоединяются галогены, водород и вода.
- Качественная реакция диенов – галогенирование. Аналогично, как и алкены, диены могут взаимодействовать с бромной водой, обесцвечивая ее. Но в этом уроке рассмотрим взаимодействие диена с чистым хлором.
- Гидрирование. На платиновом или никелевом катализаторе диен превращается в алкен. Можно правильно заметить, что получившийся алкен также может подвергаться реакции гидрирования, образуя насыщенный углеводород.
- Гидратация. Эта реакция проходит в кислой среде, например в присутствии серной кислоты. Молекула воды разрывается по связи Н-ОН на 2 частички, которые присоединяются к диену в соответствии с вышеупомянутым правилом.
Также есть еще один вариант протекания реакций присоединения: в этом случае вещество А-Б присоединяется только к 1 из кратных связей, как показано на схеме ниже. Такой вариант присоединения на практике хоть и встречается, но очень редко (например, при взаимодействии 10 молекул бутадиена с бромом, 8 молекул превратятся в 1,4-дибромбутен-2, и только 2 молекулы в 3,4-дибромбутен-1).
Реакции полимеризации и горения
При полимеризации сопряженных диенов происходит тоже самое, что и при реакциях присоединения: одинарная связь между кратными превращается в двойную, а кратные становятся одинарными. Рассмотрим пример образования полимера из диена. Условия реакции – использование катализатора (например, хлороводородной кислоты) и повышенной температуры. Помним, что n – большое число молекул, например 200 или даже 1000.
При горении диенов в кислороде образуются углекислый газ и вода. Общая формула горения диенов выглядит так:
Воспользуемся формулой и определим коэффициенты в реакции горения гептадиена-1,5:
Применение алкадиенов
Основная область применения диенов – органический синтез, цель которого получить каучуки с определенным набором свойств. Каучуки – это полимерные материалы, обладающие упругостью, из которых впоследствии делают резину.
Алкины
На данный момент были рассмотрены почти все возможные углеводороды ациклического строения. Рассматривались соединения только с одинарными связями, с одной двойной связью и даже с двумя двойными. И остался еще один тип углеводородов – такие, которые содержат в своем составе 1 тройную связь между атомами углерода – алкины.
Общая формула алкинов, как и у диенов:
Однако, в отличии от них, минимальное число атомов углерода в составе алкина – 2 (т.к. тройная связь может образоваться между 2 атомов углерода). А вот и пример – молекула ацетилена:
Тройная связь образуется между рядом стоящими атомами углерода, находящихся в sp-гибридизации по схеме, изображенной на рисунке 4.
Рисунок 4. Перекрывание «горизонтальных» и «вертикальных» негибридных p-орбиталей при образовании двух π-связей (желтые и синие), и перекрывание гибридных орбиталей при образовании σ-связи (серые) Источник
Номенклатура алкинов
Правила и алгоритмы названия алкинов идентичны алкенам, с той лишь разницей, что суффикс используется не –ен, а –ин. По точно такому же принципу даются названия и алкинам с заместителями.
Изомерия алкинов
Подробно про некоторые виды изомерии рассказывалось в первой части урока и чтобы не повторяться, просто перечислим слева направо, какие виды изомерии характерны для алкинов, на примере пентина-1:
- Углеродного скелета,
- Положение кратной связи,
- Межклассовая.
Физические свойства алкинов
По своим физическим свойствам алкины схожи с алкенами, у которых такой же структурный состав, однако имеют более высокие температуры плавления и кипения, что отражено в таблице.
Таблица сравнения температуры кипения и плавления алкинов и соответствующих алкенов
Агрегатное состояние алкинов меняется от газообразного до твердого, в зависимости от содержания атомов углерода в них.
C2H2-C4H6 бесцветные газы, не имеющие запаха
C5H8-C15H28 жидкости
С C16H30 твердые вещества
Алкины плохо растворяются в воде и хорошо растворяются в органических растворителях.
Способы получение алкинов
Рассмотрим некоторые реакции получения алкинов.
Общие способы получения алкинов
- Взаимодействие дигалогеналканов со спиртовым раствором щелочи. В этой реакции обязательно условие, чтобы атомы галогенов были заместителями у 1 и 2 или 2 и 3, или 3 и 4 и т.д, другими словами: у двух соседних атомов углерода.
- Взаимодействием металлорганического соединения, содержащего тройную связь, с алкилгалогенидом. В этой реакции происходит разрыв связи между атомами галогена и углерода в алкилгалогениде, и разрыв связи между атомом металла и углерода в металлорганическом соединении. После этого образовавшиеся радикалы соединяются между собой, а металл соединяется с галогеном, образуя соль.
Способы получения этина
Для получения этина можно использовать некоторые уникальные реакции.
- Дегидрирование метана. При 1500 °С метан превращается в этин.
- Гидролиз карбида кальция. Раньше среди детских забав была одна опасная игра – найти где-нибудь карбид кальция и бросить его в лужу. В результате гидролиза выделялся прозрачный газ, который хулиганы поджигали, и смотрели за тем, как «горит лужа». Повторять такие «уличные» опыты нельзя, т.к. для этого есть специальные лаборатории, где почти полностью исключена возможность получить опасные травмы.
Химические свойства алкинов
Для алкинов характерны реакции присоединения, окисления, горения тримеризации и «серебряного зеркала». Ниже рассмотрим, как протекают эти реакции и разберемся, что такое тримеризация и «серебряное зеркало».
Реакции присоединения
Как и в алкенах или диенах, присоединение веществ происходит по кратной связи. Изначально при присоединении образуется алкен, который дальше также может вступать с присоединяемым веществом в реакцию, в результате чего получаются алканы различного состава. Рассмотрим схематично, как происходит присоединение к молекулам алкинов галогенов, водорода, галогенводородов и воды.
- Галогенирование. Стоит отметить, что этот тип реакций является качественным на алкины. Еще раз разберемся, что такое качественная реакция. Предположим, что учительница Ванечки, Зинаида Алексеевна, дала ему две пробирки с бесцветными жидкостями и сказала: «Ванечка, вот в одной пробирке есть алкан, а в другой – диен. Как узнать, в какой пробирке какое вещество?». Что сделает Ванечка? Он возьмет бромную воду, которая коричневого цвета, и добавит в каждую пробирку. В одной пробирке бромная вода станет прозрачной, а в другой цвет ее не изменится. Это будет означать, что в одной пробирке реакция прошла, а в другой нет.
Как мы помним, алканы не взаимодействуют с бромной водой, и с ней взаимодействуют только соединения с кратными связями. Реакции, которые характерны только для определенных веществ называются качественными.
На бумаге протекание реакции можно изобразить следующим образом:
- Гидрирование в присутствии палладия:
- Гидрогалогенирование. Здесь следует помнить про правило Марковникова и правильно располагать водород и галоген у атомов углерода.
- Реакция Кучерова. Гидролиз алкинов в присутствии солей ртути в кислой среде позволяет получать кетоны – кислородсодержащие соединения, о которых поговорим подробнее через несколько уроков.Для понимания на данный момент уясним, что кетоны – это такие органические вещества, в которых атом углерода соединен двойной связью с кислородом. Оба водорода от молекулы воды присоединяются к гидрированному атому углерода, а кислород – к менее гидрированному. Отличительная особенность от гидролиза углеводородов с двойными связями: там молекула воды распадалась на Н и ОН частицы.
Некоторые другие реакции
Рассмотрим еще некоторые химические реакции алкинов, и поймем, что такое тримеризация и странные «серебряные зеркала».
Реакции окисления
При взаимодействии с окислителем алкин превращается в карбоновую кислоту. Реакция протекает в кислой среде. При окислении происходят окислительно-восстановительные процессы с переносом электронов между атомами, и, основываясь на этом, можно составлять полноценные химические уравнения с расстановкой коэффициентов.
Реакция тримеризации
А вот и первое непонятное слово. Тримеризация – это реакция взаимодействия между собой трех молекул алкена, из которых получается одна молекула, которая называется бензол.
Реакция серебряного зеркала
Как и галогенирование, эта реакция является качественной на алкины. Почему же ее так назвали? Все дело в том, что для ее проведения используется особый реагент – аммиачный раствор оксида серебра. При взаимодействии этого реагента с алкином выделяется серебристо-белый осадок, который покрывает равномерным слоем внутреннюю поверхность посуды, в которой проводился опыт. Если присмотреться, то в таком осадке можно увидеть свое отражение, как в зеркале.
Источник
Реакция горения
Алкины горят в присутствии кислорода, и для описания этой реакции можно воспользоваться формулой, которую уже встречали у диенов:
Как и при горении многих других органических веществ, основными продуктами реакции будут СО2 и Н2О.
Применение алкинов
Алкины нашли свое применение в качестве исходных материалов при синтезе различных полимеров, таких как: каучуки, пленки и пластмассы. Также из алкинов синтезируют клеющие вещества.
Но стоит помнить: алкины – ядовитые вещества, которые могут вызывать наркотический эффект или судороги. Поэтому обращаться с ними следует очень осторожно.